PALM/STORM
개요
PALM (Photoactivated Localization Microscopy)과 STORM (Stochastic Optical Reconstruction Microscopy)은 SMLM (Single-Molecule Localization Microscopy)의 두 가지 주요 방법으로, 동일한 일반 원리를 공유하지만 서로 다른 형광 probes를 사용한다. 두 방법 모두 약 20 nm의 resolution을 달성할 수 있다.
PALM과 STORM의 차이
PALM (Photoactivated Localization Microscopy)
원래 사용: Photoswitchable fluorescent proteins 특징: Genetically encoded, 살아있는 세포에서 사용 가능 개발: 형광 단백질의 photoswitching 특성 활용
STORM (Stochastic Optical Reconstruction Microscopy)
원래 사용: Photoswitchable dyes 특징: 화학적 염료, 일반적으로 더 밝음 개발: 합성 photoswitchable dyes의 특성 활용
현재 상황
일반 원리는 동일: 두 방법 모두 sequential activation과 localization 사용 Probes 교환 가능: STORM은 이제 photoswitchable fluorescent proteins도 사용 가능, PALM도 photoswitchable dyes 사용 가능 용어: 일반적으로 single-molecule localization microscopy (SMLM)로 통칭
Figure 9-33: 여러 구조의 Multicolor Imaging
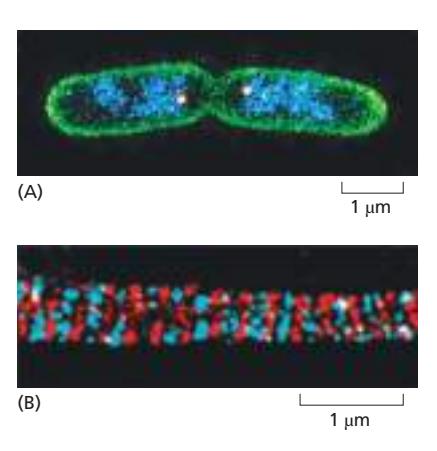
(A) Escherichia coli Cells - STORM
표본: 최근 분열한 두 개의 E. coli cells Resolution: 약 20 nm 사용된 세 가지 Switchable Fluorescent Labels:
- Membrane: 녹색으로 표지
- DNA molecules: 파란색으로 표지 (최근 분리됨)
- Chromosome ends: 두 개의 밝은 흰색 점으로 보임 (복제된 chromosomes의 ends)
의의: 단일 세포 내에서 여러 구조를 동시에 superresolution으로 가시화
(B) Nerve Cell - Multi-color SMLM
구조: Axon의 cytoskeletal framework Periodicity: 약 190 nm 주기 (diffraction limit 바로 아래)
관찰된 구조:
- Actin: 빨간색으로 표지, axon 둘레를 감싸는 균일한 간격의 ring-like structures
- Spectrin: 파란색으로 표지, actin rings 사이에 유사하게 간격을 둔 structures
생물학적 의의: 이 주기적인 actin-spectrin cytoskeletal framework는 nerve cells의 길고 얇은 axons를 지지하는 데 도움을 준다.
기술적 의의: 이러한 이미지들은 새로운 매우 빠르게 switching하고 극도로 밝은 형광 probes의 개발에 크게 의존한다.
PALM/STORM의 작동 원리
Sequential Activation
- Sparse Subset Activation: 한 번에 소수의 분리된 분자들만 활성화
- Imaging: 각 활성화된 분자가 수천 개의 photons 방출
- Bleaching: 형광이 quench됨
- Repetition: 과정을 수만~수십만 번 반복
Localization
각 분자의 위치: Blurred image의 수학적 중심 계산 정밀도: 일반적으로 10-20 nm 누적: 모든 위치를 하나의 superresolution 이미지로 결합
Multicolor Imaging
여러 Probes: 서로 다른 색상의 photoswitchable labels 동시 또는 순차적: Channel에 따라 imaging 방식 선택 색상 분리: Spectral properties나 sequential activation으로 구분
PALM/STORM의 주요 특징
1. Multicolor Capability
여러 구조 동시 가시화: Figure 9-33A의 membrane, DNA, chromosome ends Color Coding: 각 구조를 다른 색으로 구분 Complex Systems: 여러 단백질 간 상호작용 연구
2. 생물학적 구조 연구
Periodic Structures: Figure 9-33B의 actin-spectrin cytoskeleton Nanoscale Organization: Diffraction limit 이하의 patterns Molecular Architecture: Protein complexes의 상세 배열
3. Probe의 다양성
Fluorescent Proteins: PALM에서 주로 사용, genetically encoded Chemical Dyes: STORM에서 주로 사용, 더 밝고 안정적 현재: 두 방법 모두 양쪽 probe types 사용 가능
PALM/STORM의 장점
1. 극도로 높은 Resolution
~20 nm: Conventional microscopy의 10배 향상 실제 크기: Molecular dimensions을 정확히 반영 Periodic Patterns: 190 nm 주기도 명확히 분해 (Figure 9-33B)
2. Multicolor Imaging
여러 Targets: 동시에 여러 분자 종류 관찰 Colocalization: 분자들의 공간적 관계 Interaction Studies: Protein-protein interactions
3. Quantitative Analysis
Molecule Counting: 개별 분자 수 정량 Stoichiometry: Complex 내 분자 비율 Clustering: Spatial distribution patterns
4. Wide-field Imaging
넓은 영역: 한 번에 큰 영역 관찰 가능 Multiple Cells: 여러 세포 동시 분석 Statistics: 더 많은 데이터 수집
PALM/STORM의 한계
1. 긴 Acquisition Time
수분~수시간: 수만~수십만 frames 필요 Live Cell 제약: 동적 과정 관찰 어려움 Photobleaching: 장시간 노출로 인한 손상
2. 특수 Probes 필요
Photoswitchable Properties: 특수한 switching 특성 필요 밝기와 안정성: 충분한 photon 수와 안정성 비용: 특수 probes는 비쌀 수 있음
3. Dense Labeling 요구
충분한 밀도: Nyquist criterion 만족 필요 균일한 분포: 불균일하면 artifacts 발생 Labeling Efficiency: 높은 효율 필요
4. 2D 제약 (기본)
주로 2D: 표준 PALM/STORM은 2D 3D 변형 존재: 특수 설정으로 3D 가능하지만 복잡 Z-resolution: XY보다 Z 방향 resolution 낮음
기술적 발전
Improved Probes
더 밝은 Dyes: 더 많은 photons per switching cycle 빠른 Switching: 더 짧은 acquisition time 안정성: Reduced photobleaching, 더 많은 cycles
3D PALM/STORM
Astigmatism: Cylindrical lens로 z-information Biplane: 두 focal planes 동시 imaging PSF Engineering: Engineered point spread functions
Live-cell PALM/STORM
빠른 Variants: Reduced frame numbers Lower Light Levels: Phototoxicity 감소 Dynamic Processes: 일부 동적 과정 관찰 가능
응용 분야
Bacterial Cell Biology
E. coli Structure: Membrane, nucleoid, chromosome organization (Figure 9-33A) Division Machinery: FtsZ ring, division proteins Flagellar Motors: Nanoscale architecture
Neuroscience
Synaptic Proteins: Receptor organization, scaffolding proteins Axonal Cytoskeleton: Actin-spectrin periodic structure (Figure 9-33B) Dendritic Spines: Morphology와 protein distribution
Membrane Biology
Receptor Clustering: Nanoscale domains Lipid Rafts: Organization과 dynamics Membrane Proteins: Oligomerization states
Nuclear Organization
Chromatin Structure: Nanoscale packaging Transcription Sites: RNA polymerase clusters Nuclear Bodies: PML bodies, Cajal bodies
데이터 분석
Localization Analysis
Precision Calculation: Localization uncertainty Drift Correction: Long acquisition 중 stage drift 보정 Artifact Removal: 잘못된 localizations 제거
Cluster Analysis
Ripley’s K-function: Spatial clustering 분석 DBSCAN: Density-based clustering Pair Correlation: Molecular interactions
Quantification
Molecule Counting: 각 구조의 분자 수 Density Maps: Spatial distribution Colocalization: 여러 species 간 관계
실험적 고려사항
Sample Preparation
고정: 일반적으로 fixed samples 사용 Labeling Density: 충분한 probe 밀도 Mounting Medium: Appropriate imaging buffer
Imaging Parameters
Laser Powers: Activation과 excitation 최적화 Frame Rate: Detection sensitivity와 균형 Total Frames: 충분한 molecules 검출
Image Reconstruction
Localization Algorithms: Gaussian fitting, maximum likelihood Filtering: Background, precision-based filtering Rendering: Final image generation parameters
PALM/STORM vs 다른 기술
vs SIM: SIM은 ~100 nm, 빠름 (~초-분), 모든 dyes. PALM/STORM은 ~20 nm이지만 느림 (~분-시간), 특수 probes.
vs STED: 둘 다 ~20 nm. STED는 scanning 기반, 비교적 빠름. PALM/STORM은 wide-field, 느리지만 더 넓은 영역.
vs SMLM (Single-Molecule Localization Microscopy): PALM/STORM은 SMLM의 specific implementations. SMLM은 더 넓은 umbrella term.
요약
핵심 원리: Photoswitchable labels의 sequential activation과 single-molecule localization으로 회절 한계 극복 PALM: 원래 photoswitchable fluorescent proteins 사용 STORM: 원래 photoswitchable dyes 사용 현재: 두 방법 모두 양쪽 probe types 사용 가능, 일반적으로 SMLM (Single-Molecule Localization Microscopy)로 통칭 Resolution: 약 20 nm 주요 장점: Multicolor imaging, wide-field, quantitative analysis 주요 한계: 긴 acquisition time, 특수 probes 필요, 주로 fixed samples 응용: Bacterial cell structure, neuronal cytoskeleton, membrane organization, nuclear architecture
참고 문헌
Chapter 9: Visualizing Cells and Their Molecules, Section: “Single-Molecule Localization Microscopy Also Delivers Superresolution”, Related Figures: 9-33, Related concepts: SMLM (Single-Molecule Localization Microscopy), deconvolution, Structured Illumination Microscopy, Stimulated Emission Depletion