Construction of Intermediate Filament
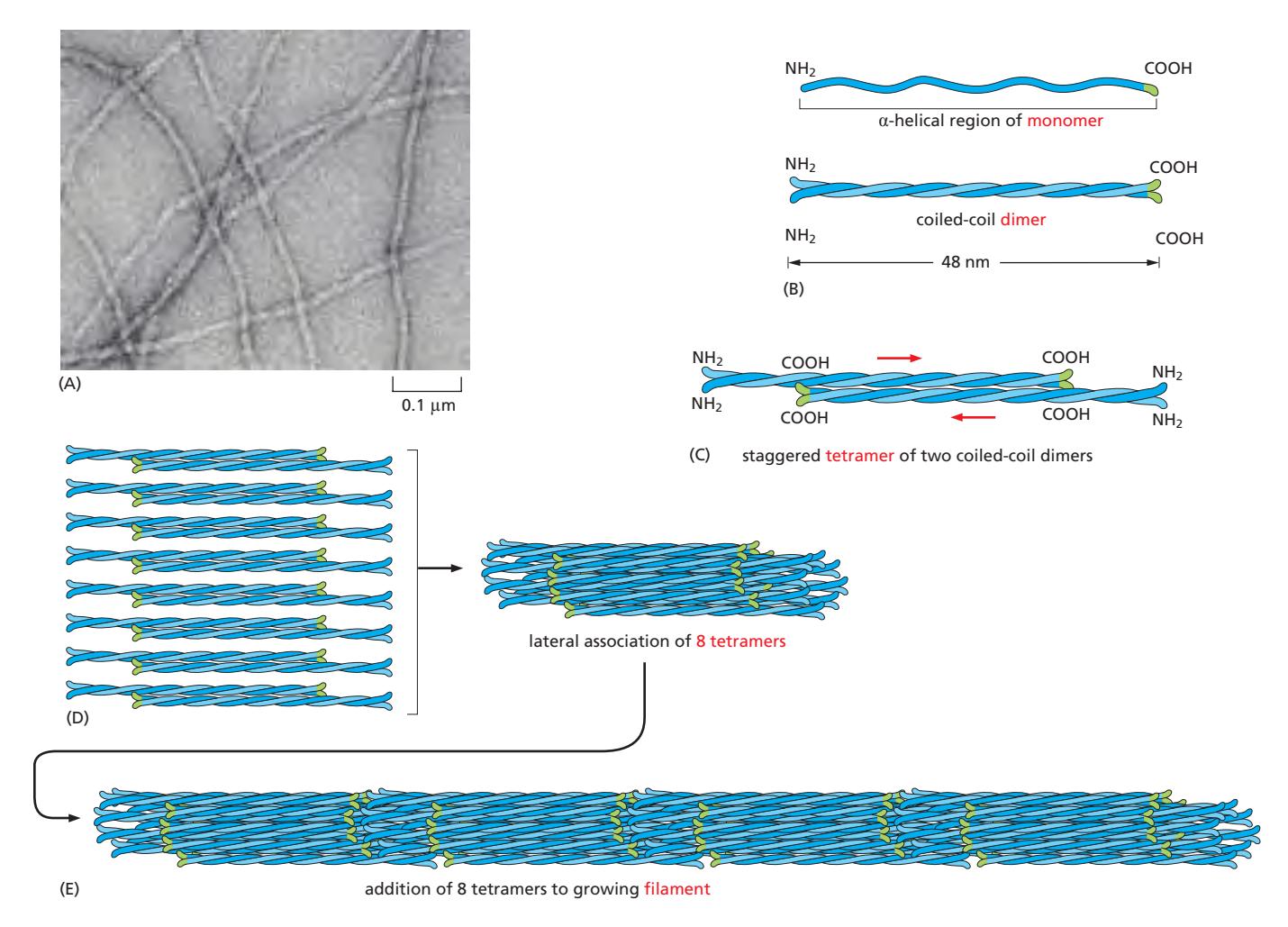 Fig 16–62. Intermediate filament 조립 모델. (A) 전자현미경 이미지. (B) Monomer. (C) 두 monomer가 평행하게 coiled-coil 이합체 형성. (D) 두 dimer가 역평행으로 staggered tetramer 형성. (E) Tetramer들이 packing되어 10 nm 직경 필라멘트 완성.
Fig 16–62. Intermediate filament 조립 모델. (A) 전자현미경 이미지. (B) Monomer. (C) 두 monomer가 평행하게 coiled-coil 이합체 형성. (D) 두 dimer가 역평행으로 staggered tetramer 형성. (E) Tetramer들이 packing되어 10 nm 직경 필라멘트 완성.
모든 intermediate filament protein family는 N- 및 C-terminal domain은 다르지만, 약 40개의 heptad repeat motif로 이루어진 보존된 central α-helical domain을 공유한다.
조립 단계
-
Monomer → Coiled-coil dimer: 두 monomer가 평행하게 정렬되어 central rod domain끼리 coiled-coil을 형성한다.
-
Dimer → Antiparallel staggered tetramer: 두 dimer가 역방향(antiparallel)으로 엇갈리게 결합하여 4-chain tetramer를 형성한다. 이 tetramer가 soluble subunit이다.
-
Tetramer → 10 nm 필라멘트: Tetramer들이 측면으로 packing되어 8개의 parallel protofilament를 이루고, 최종 필라멘트는 단면에 16개의 dimer(32개의 coiled-coil)를 갖는다.
중요한 특성
Intermediate filament subunit은 ATP나 GTP 결합 부위가 없다.1 또한 tetramer subunit은 두 dimer가 반대 방향을 향해 구성되므로 양 끝이 동일하다. 따라서 assembled intermediate filament는 극성(polarity)이 없다 — actin filament나 microtubule과 근본적으로 다른 점이다.2
Intermediate filament는 쉽게 구부러지지만(persistence length < 1 μm) 끊기가 매우 어렵고, 원래 길이의 3배 이상 늘어날 수 있다. 이는 rope-like 구조에서 비롯된 기계적 특성이다.
Assembly/disassembly는 actin이나 microtubule보다 덜 이해되어 있다. 단백질 인산화가 분해를 조절하는 것으로 보이며, mitosis 시 nuclear lamin 분해가 대표적 예이다. Vimentin처럼 일부 intermediate filament는 세포 내에서 매우 dynamic하게 remodeling된다.
Footnotes
-
2025 기말 21번 — Intermediate filament가 ATP를 이용하지 않음(ATP-driven motor 없음, 인산화/탈인산화로 조절)이 정답 ④의 근거로 활용됨. ↩
-
2022 기말 5번 — ①번 선지: coiled-coil tetramer 8개로 조립되는 cytoskeleton 중 방향성(polarity)이 없는 것이 intermediate filament임을 확인하는 문장. ↩