Biological Specimen Preparation for Electron Microscopy
개요
Electron microscopy 초기에는 생물학적 재료에 적용하면서 세포 내에서 이전에 상상하지 못했던 많은 구조들이 드러났다. 그러나 이러한 발견이 이루어지기 전에, electron microscopists는 조직을 embedding, cutting, staining하기 위한 새로운 절차를 개발해야 했다.
Specimen의 기본 요구사항
Vacuum 환경
문제: Specimen이 electron microscope에서 매우 높은 vacuum에 노출됨 결과: 살아있는 조직은 일반적으로 killed되고 보존되어야 함
Penetration 한계
Electrons의 제한적 penetrating power: 고정된 조직은 일반적으로 매우 얇은 sections으로 잘라야 함 두께: 25-100 nm thick (단일 세포 두께의 약 1/200)
Chemical Fixation
고정제 (Fixatives)
일반적인 fixative: Glutaraldehyde 작용 메커니즘:
- Proteins의 free amino groups와 covalent bonds 형성
- Proteins를 cross-linking하여 안정화
- 제자리에 고정
효과: 세포 내 구조를 보존하고 안정화
Embedding 과정
필요성
조직이 chemical fixation 후에도 일반적으로 soft하고 fragile함. 따라서 sectioning 전에 frozen되거나 supporting medium에 embedded되어야 함.
Embedding Media
일반적인 media: Waxes 또는 resins
과정:
- Liquid form: Media가 고정된 조직을 permeate하고 surround함
- Hardening: Cooling 또는 polymerization으로 단단한 block 형성
- Sectioning: Block이 microtome으로 쉽게 section될 수 있음
Figure 9-8: Tissue Sections 제작

Microtome: Steel 또는 glass blade를 가진 기계로 meat slicer처럼 작동 Sections: 일반적으로 0.5-10 μm thick Glass slide: Sections를 glass microscope slide의 표면에 평평하게 놓음
Alternative method: 매우 빠르게 frozen된 samples도 section 가능하며, 이는 native state의 세포 구조를 더 잘 보존함
Ultrathin Sections
특성
두께: 25-100 nm 상태:
- 물과 다른 휘발성 용매가 없음 (free of water and other volatile solvents)
- 작은 metal grid로 지지됨
목적
Microscope에서 보기 위한 준비
Figure 9-41: Specimen Support
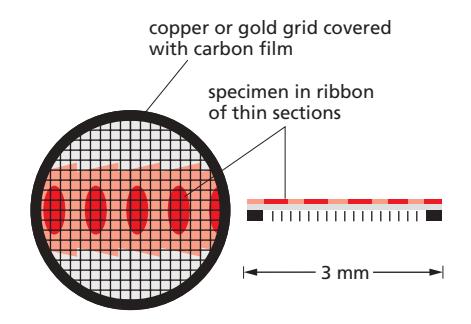
Metal grid: Transmission electron microscope에서 specimen의 thin sections를 지지 구조: 작은 구멍들이 있는 grid로 electron beam이 통과할 수 있음
Specimen 준비의 도전과제
신뢰성 문제
핵심 질문: 고정, 탈수, resin-embedding된 specimen의 이미지가 살아있는 세포의 섬세한 수성 생물학적 시스템과 어떤 관계가 있는가?
우려사항:
- 일부 세포 구성 요소가 손실될 수 있음
- 준비 과정 중 distortion 가능성
- Artifacts 생성 위험
해결책: Rapid Freezing
현재 이 문제에 대한 최선의 접근법은 rapid freezing에 의존한다.
Rapid Freezing (Vitrification)
원리
충분히 빠르고 낮은 온도로 냉각: Aqueous system이 재배열하거나 얼음으로 결정화할 시간이 없음 결과: 물이 “glass”라고 불리는 rigid하지만 non-crystalline state로 supercooled됨 - vitreous ice
방법
Rapid freezing 수행:
- Liquid ethane 같은 coolant에 sample을 plunging
- 또는 매우 높은 압력에서 cooling
Vitrified Specimens의 검사
직접 검사
일부 rapidly frozen specimens는 특수 cooled specimen holder를 사용하여 electron microscope에서 직접 검사 가능
Fracturing
Frozen block을 fracture하여:
- Interior cell surfaces 노출
- 또는 surrounding ice를 sublimate하여 external surfaces 노출
Freeze Substitution
목적: Thin sections를 검사하고자 할 때
과정:
- Rapidly freeze tissue
- 물을 organic solvents로 교체
- Tissue를 plastic resin에 embed
- Sections 절단
장점: 조직을 원래 살아있는 상태에 매우 가깝게 안정화하고 보존
Figure 9-42: Freeze Substitution

표본: 매우 빠르게 frozen되고 vitreous ice가 organic solvents로, 그 다음 plastic resin으로 교체된 yeast cell의 thin section
관찰 가능한 구조:
- Nucleus: 명확히 보임
- Mitochondria: 세부 구조 보존
- Cell wall: 잘 보존됨
- Golgi stacks: 식별 가능
- Ribosomes: 모두 쉽게 볼 수 있음
상태: 가능한 한 lifelike한 상태로 추정됨
Specimen 준비의 복잡성
단계들
Electron microscopy를 위한 생물학적 재료 준비에 필요한 단계들:
- Chemical fixation (또는 rapid freezing)
- Dehydration
- Embedding
- Sectioning
- Staining (다음 섹션에서 논의)
주의사항
각 단계에서:
- 구조 보존 최대화
- Artifacts 최소화
- 원래 구조와의 충실도 유지
준비 방법 비교
Chemical Fixation + Embedding
장점:
- 표준화된 프로토콜
- 비교적 간단
- 많은 샘플 처리 가능
단점:
- 구조 변형 가능성
- 일부 구성 요소 손실
- Artifacts 위험
Rapid Freezing (Vitrification)
장점:
- 원래 구조 최상 보존
- Artifacts 최소화
- Native state에 가장 가까움
단점:
- 기술적으로 어려움
- 특수 장비 필요
- 샘플 크기 제한
Freeze Substitution
장점:
- Vitrification의 장점 + sectioning 가능
- 우수한 구조 보존
- 표준 sectioning 가능
단점:
- 복잡한 과정
- 시간 소요
- 기술적 전문성 필요
응용 분야
세포 구조 연구
Organelles: Mitochondria, Golgi, ER의 상세 구조 Membranes: Membrane ultrastructure Cytoskeleton: Filaments, microtubules
바이러스학
Virus particles: 구조와 assembly Infection process: 세포 내 바이러스
발생 생물학
Embryonic tissues: 발달 과정의 세포 변화 Differentiation: 세포 분화 중 구조 변화
기술적 고려사항
Fixation Quality
Critical factors:
- Fixative 농도와 시간
- Buffer 조성
- 온도
- Penetration rate
Freezing Rate
Vitrification을 위한 요구사항:
- 매우 빠른 cooling rate (>10,000°C/sec)
- 작은 샘플 크기 (<200 μm)
- Cryoprotectants 사용 가능
Section Quality
중요 요소:
- Knife sharpness
- Sectioning speed
- Section thickness uniformity
- Compression artifacts 최소화
요약
핵심 과제: Electron microscopy를 위한 생물학적 specimen 준비는 구조 보존과 기술적 요구사항 사이의 균형 주요 방법: Chemical fixation + embedding, rapid freezing (vitrification), freeze substitution 최선의 접근: Rapid freezing과 freeze substitution이 원래 살아있는 상태에 가장 가까운 구조 보존 제공 Trade-offs: 각 방법은 구조 보존 품질, 기술적 난이도, 처리량 사이에서 trade-offs 존재 중요성: 적절한 specimen 준비는 electron microscopy에서 신뢰할 수 있는 결과를 얻는 데 필수적
참고 문헌
Chapter 9: Visualizing Cells and Their Molecules, Section: “Biological Specimens Require Special Preparation for Electron Microscopy”, Related Figures: 9-8, 9-41, 9-42