ATP Synthesis
ATP Hydrolysis의 자유에너지 변화
ATP는 세포의 보편적 에너지 화폐이다. ATP의 유용성은 가수분해 반응이 매우 비자발적인 평형으로부터 멀리 유지된다는 데 있다.
그러나 세포 내 실제 조건(ATP가 ADP, Pᵢ보다 훨씬 높은 농도)에서는:
 Figure 14-30: ATP 가수분해 반응의 자유에너지와 평형 간 관계.
Figure 14-30: ATP 가수분해 반응의 자유에너지와 평형 간 관계.
- ΔG (실제 자유에너지 변화) = ΔG° + RT ln([ADP][Pᵢ]/[ATP])
- 세포는 높은 [ATP]/([ADP]·[Pᵢ]) 비율을 유지하여 ATP hydrolysis를 평형에서 매우 멀리 유지
- 이 큰 음수의 ΔG가 많은 세포 반응을 driving하는 원동력
산화적 인산화에서의 ATP 생산
NADH, FADH₂로부터 ATP 수율 (산화적 인산화)
| 전자 공여체 | 원천 | ATP yield (pair당) |
|---|---|---|
| NADH (미토콘드리아) | Citric acid cycle, pyruvate oxidation 등 | ~2.5 ATP |
| FADH₂ / NADH (세포질) | Succinate dehydrogenase, glycolysis | ~1.5 ATP |
- FADH₂와 cytosolic NADH는 Complex I을 우회하므로 더 적은 ATP 생산
Glucose 1분자 완전 산화 시 총 ATP
| 단계 | 위치 | 생산물 |
|---|---|---|
| Glycolysis | 세포질 | 2 ATP + 2 NADH |
| Pyruvate oxidation | 미토콘드리아 matrix | 2 NADH |
| Citric acid cycle | 미토콘드리아 matrix | 6 NADH + 2 FADH₂ + 2 GTP |
| 산화적 인산화 | 미토콘드리아 inner membrane | ~26 ATP |
| 합계 | ~30 ATP |
Palmitoyl CoA 1분자 산화 시 → Net result of energy metabolism 참조
하루 ATP 회전량
- 일반 성인: 하루 ~50 kg ATP 회전
- 마라톤 선수: 수백 kg까지 증가
- 즉, ATP 분자 자체는 재사용 — 합성·가수분해 사이클을 수천 번 반복
Proton-motive force와 ATP synthesis 연결
Chemiosmotic coupling에서 설명하듯, ETC가 형성한 electrochemical proton gradient (~180 mV)가 ATP synthase를 구동한다.
- ΔG for H⁺ translocation = 구동력
- ΔG for ATP synthesis = 피구동 반응
- 두 반응이 allosteric coupling을 통해 연결
ATP/ADP Transport
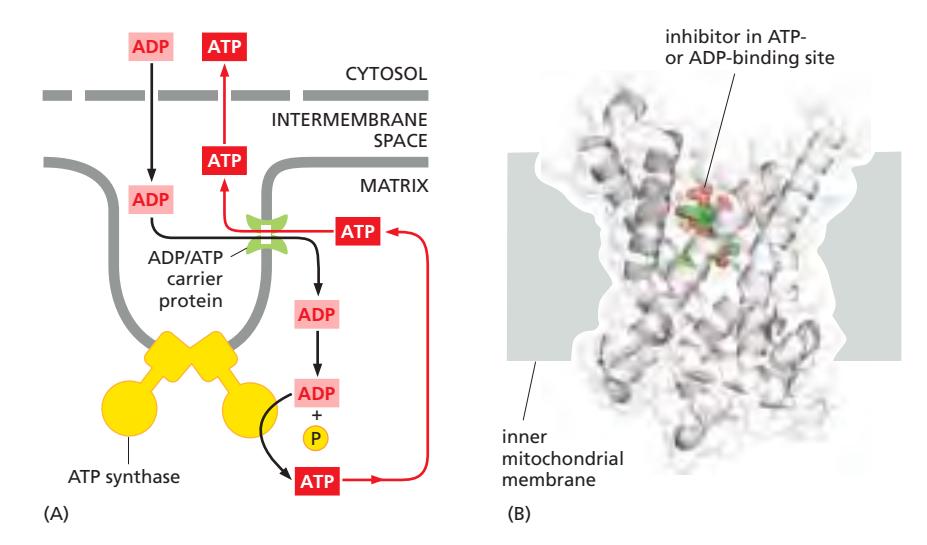 Figure 14-35: ADP/ATP carrier protein. Matrix의 ATP를 intermembrane space로 내보내고, ADP를 matrix 안으로 수입.
Figure 14-35: ADP/ATP carrier protein. Matrix의 ATP를 intermembrane space로 내보내고, ADP를 matrix 안으로 수입.
- ADP/ATP carrier protein (mitochondrial carrier family): inner membrane 통해 ATP와 ADP를 교환
- ATP⁴⁻ → matrix 밖으로 (electrochemical gradient에 의해 구동: ATP가 더 음전하)
- ADP³⁻ → matrix 안으로
- 합성된 ATP가 세포질로 빠져나가 에너지 수요 충족
관련 노트
- Complex V (ATP synthase) — 분자 구조와 rotary catalysis 메커니즘
- Chemiosmotic coupling
- Net result of energy metabolism