Structure and Function of Cadherin
Extracellular 구조
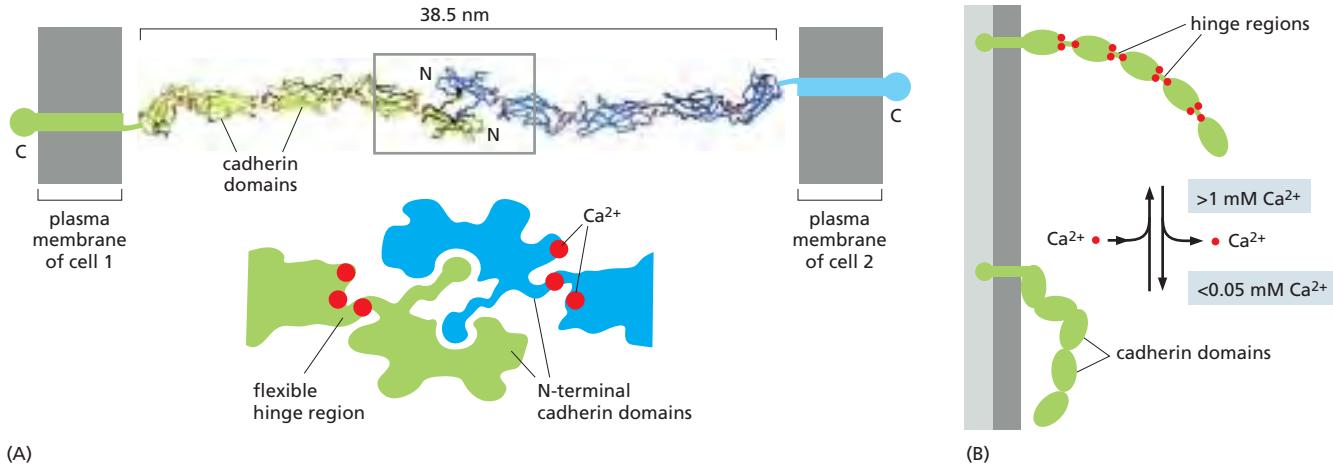 Figure 19-6. (A) Classical cadherin의 extracellular region에는 5개의 EC domain이 있으며, 각 hinge 근처에 Ca²⁺(붉은 점)가 결합하여 구조를 경직시킨다. Homophilic binding은 N-terminal tip의 EC domain 사이에서 발생한다—한 분자의 knob이 상대 분자의 pocket에 삽입되는 방식이다. (B) Ca²⁺가 제거되면 hinge가 유연해져 분자가 흐물흐물해지고 결합 능력을 잃는다. (C) 세포-세포 junction에서 cadherin 분자들은 Velcro처럼 측면-측면 배열(side-to-side)로 촘촘히 연결되어 강한 부착을 형성한다.
Figure 19-6. (A) Classical cadherin의 extracellular region에는 5개의 EC domain이 있으며, 각 hinge 근처에 Ca²⁺(붉은 점)가 결합하여 구조를 경직시킨다. Homophilic binding은 N-terminal tip의 EC domain 사이에서 발생한다—한 분자의 knob이 상대 분자의 pocket에 삽입되는 방식이다. (B) Ca²⁺가 제거되면 hinge가 유연해져 분자가 흐물흐물해지고 결합 능력을 잃는다. (C) 세포-세포 junction에서 cadherin 분자들은 Velcro처럼 측면-측면 배열(side-to-side)로 촘촘히 연결되어 강한 부착을 형성한다.
각 cadherin은 extracellular cadherin (EC) domain 여러 개로 구성된다. Classical cadherin은 5개의 EC domain을 가지며, 각 domain은 다소 경직된 단위를 이루고, 인접 domain 사이는 hinge로 연결된다.
Ca²⁺의 역할: Ca²⁺가 각 hinge 근처에 결합하면 hinge가 구부러지지 않아 전체 cadherin 분자가 경직된 약간 곡선형 막대처럼 행동한다. Ca²⁺가 제거되면 hinge가 유연해지고 N-terminal 쪽의 conformation이 변화하여 homophilic binding 능력이 약화된다.
Homophilic Binding 기전
Homophilic binding은 cadherin 분자의 N-terminal tip(막에서 가장 먼 EC domain)에서 발생한다. 각 N-terminal EC domain은 knob과 pocket을 형성하며, 반대 세포의 cadherin 분자와 knob-into-pocket 방식으로 결합한다 (→ Homophilic vs heterophilic binding).1
Velcro 원리
개별 cadherin-cadherin 결합의 친화도는 낮다. 강한 부착은 많은 약한 결합이 병렬로 형성될 때 나타난다. 같은 세포의 cadherin 분자들은 측면-측면(side-to-side) 상호작용으로 집합화되어, 반대 세포의 수직 배열과 결합하는 촘촘한 2차원 배열을 이룬다. 이 구조는 Velcro처럼 전체적으로는 강하지만, 순차적으로 분리하면 쉽게 분해할 수 있다.
Footnotes
-
2023 기말 24번 — cadherin intracellular domain에 직접 결합하는 단백질로 β-catenin과 p120-catenin이 정답 근거로 활용됨. ↩