3 Energy Sources for Import
미토콘드리아 단백질 수입은 세 가지 에너지원을 네 곳에서 사용한다. 모든 precursor 단백질이 이 세 가지 에너지를 모두 필요로 하지는 않는다.123
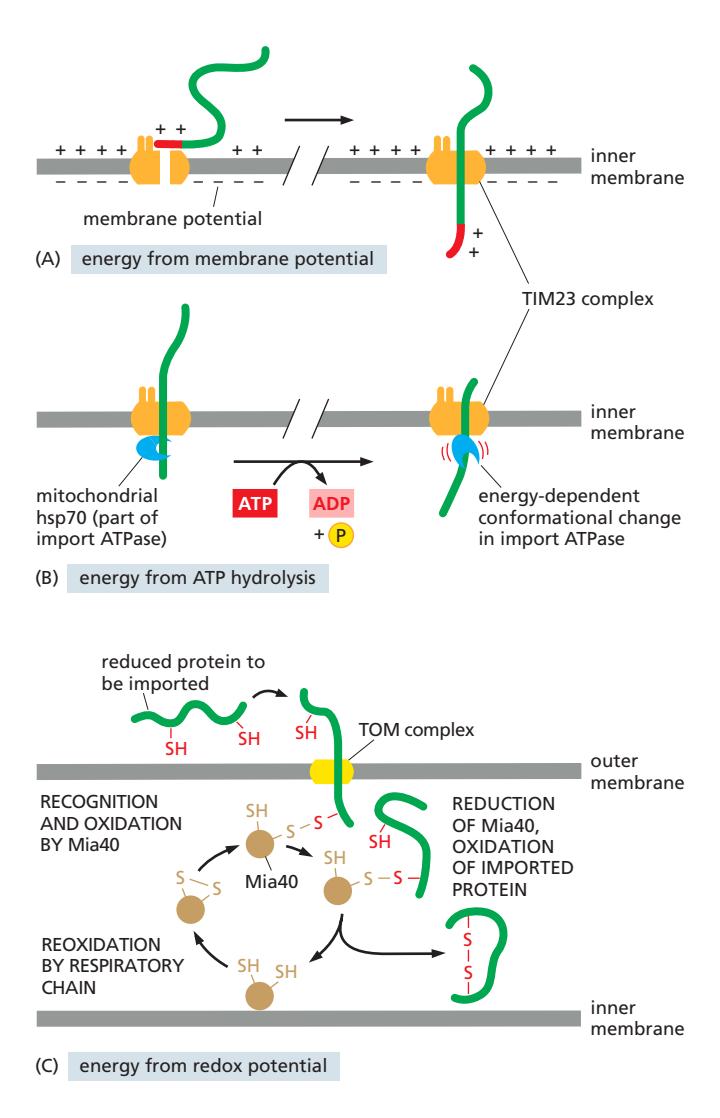 Fig 12-50. 미토콘드리아 단백질 수입에 관여하는 세 에너지원. (A) Inner membrane의 막전위가 signal sequence의 matrix 방향 수송을 구동. (B) Mitochondrial hsp70이 ATP 가수분해를 이용해 단백질을 matrix로 끌어당김. (C) Mia40이 cysteine에 disulfide 결합을 형성해 backsliding을 방지하며, 이 과정은 전자 전달계의 산화환원 전위에 의해 재생됨.
Fig 12-50. 미토콘드리아 단백질 수입에 관여하는 세 에너지원. (A) Inner membrane의 막전위가 signal sequence의 matrix 방향 수송을 구동. (B) Mitochondrial hsp70이 ATP 가수분해를 이용해 단백질을 matrix로 끌어당김. (C) Mia40이 cysteine에 disulfide 결합을 형성해 backsliding을 방지하며, 이 과정은 전자 전달계의 산화환원 전위에 의해 재생됨.
1. ATP 가수분해 — Cytosolic hsp70 (수입 전)
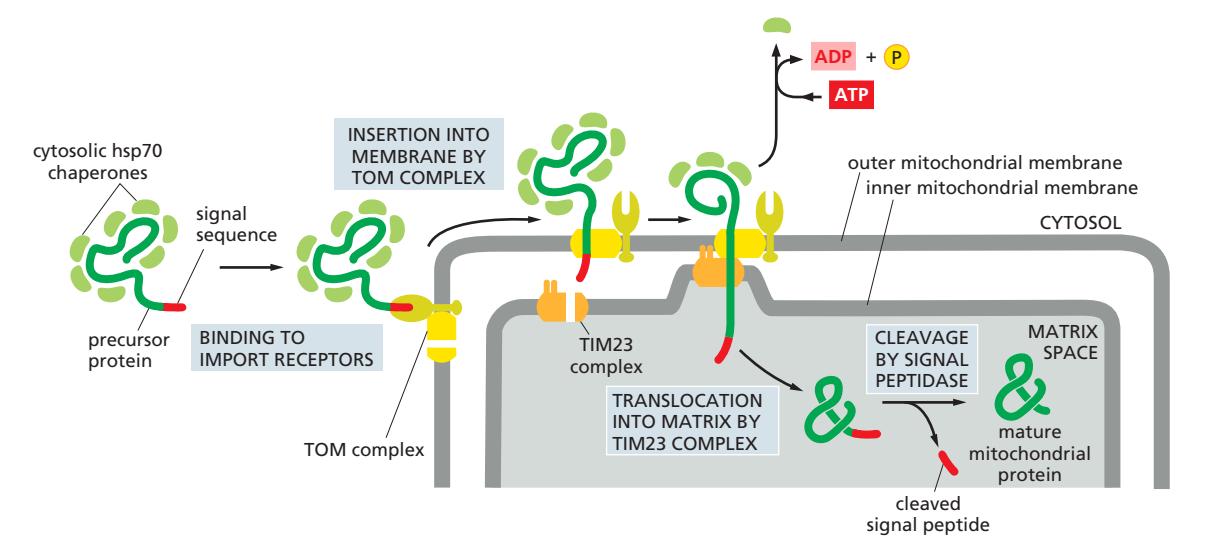
- 위치: Cytosol
- 역할: Precursor protein을 unfolded 상태로 유지
- Cytosolic hsp70 chaperone이 ATP 결합·가수분해 사이클을 통해 precursor 단백질과 결합/해리를 반복4
- Chaperone과의 결합이 단백질의 조기 폴딩이나 aggregation을 방지
- TOM complex에 결합할 때 chaperone이 해리됨
cytosolic hsp70의 ATP hydrolysis도 protein의 mitochondrial import를 구동하는 동력이라고 봐도 되나??
2. 막전위 (Membrane Potential) — TIM23 통과 구동
- 위치: Inner mitochondrial membrane을 가로지르는 전기화학적 H⁺ 기울기
- 역할: Signal sequence의 TIM23 복합체 통과를 구동
- Inner membrane을 통해 H⁺을 matrix에서 intermembrane space로 퍼냄으로써 막전위(양전하가 intermembrane space 쪽에 더 높음)가 형성됨 (→ 전자 전달계에 의해 유지)
- Precursor protein의 N-terminal signal sequence에 있는 양전하 아미노산이 이 막전위에 의해 electrophoresis 방식으로 matrix 방향으로 끌려들어감4
- 이 막전위는 ATP synthase가 대부분의 세포 ATP를 합성하는 데 사용하는 동일한 H⁺ 기울기이기도 함
3a. ATP 가수분해 — Mitochondrial hsp70 (Matrix 내에서 끌어당김)
- 위치: Matrix (TIM23 복합체의 matrix 쪽에 결합)
- 역할: Translocator를 통해 단백질을 끌어당김
- TIM23에서 polypeptide chain의 N-terminal 부분이 matrix에 노출되면 mitochondrial hsp70이 결합
- ATP 가수분해에 의한 구조 변화가 단백질을 matrix 방향으로 당기는 힘을 발생, 동시에 unfolding 유지됨
- 결합 → 당기기 → 해리의 사이클이 완전히 수입될 때까지 반복 (ratchet 메커니즘)
- Matrix 수입 완료 후 많은 단백질은 mitochondrial hsp60으로 넘겨져 폴딩이 완성됨
3b. 산화환원 전위 (Redox Potential) — Intermembrane space 단백질
- 위치: Intermembrane space 및 inner membrane의 전자 전달계
- 역할: Cysteine을 가진 intermembrane space 단백질의 수입에 사용
- **TOM**을 통해 intermembrane space로 진입한 단백질이 Mia40과 일시적인 disulfide 결합을 형성
- 이 공유결합이 단백질이 cytosol 방향으로 backslide하는 것을 방지
- 결국 단백질 내에 intrachain disulfide 결합이 형성되면서 폴딩됨, 안정화 → intermembrane space에 갇힘
- Mia40 재생: 환원된 Mia40이 전자를 전자 전달계에 전달하여 재산화됨
Footnotes
-
2021 중간 20번 — 세포질→미토콘드리아 단백질 수송 3가지 경로: ① Matrix (TOM+TIM23, Δψ+ATP), ② Inner membrane (TOM+TIM22, Δψ), ③ IMS (MIA 경로, disulfide 형성) ↩
-
2021 중간 미상D번 — 미토콘드리아 Matrix 단백질 수입 3단계: 1) TOM 통과(에너지 불필요), 2) TIM23 통과(막전위 Δψ), 3) mtHsp70 완전 수입(ATP) ↩
-
2023 중간 ver2 39번 — 세포질→미토콘드리아 matrix 단백질 수입 과정 단계별 에너지원: TOM 통과(불필요), TIM23 통과(막전위 Δψ), mtHsp70 완전 수입(ATP) ↩
-
2025 중간 16번 — ② 옳음: 세포질 hsp70이 unfolded 상태 유지, TOM/TIM23 통과. ③ 옳음: 막전위(ΔΨ)와 mtHsp70 ATP 가수분해로 완전 수입. ⑤ 틀림: matrix targeting sequence는 MPP에 의해 절단됨. ↩ ↩2