Spontaneous and Non-Spontaneous Reactions
자유에너지 (Free Energy, G)
반응의 자발성은 **자유에너지 변화 (ΔG)**로 판단한다.
- ΔG < 0: 자발적 반응 (spontaneous) — 에너지 방출
- ΔG > 0: 비자발적 반응 (non-spontaneous) — 에너지 필요
- ΔG = 0: 평형 (equilibrium)
표준 자유에너지 변화 (ΔG°)
- ΔG°: 모든 반응물/생성물의 농도가 1 M일 때의 자유에너지 변화
- 생물학에서는 pH 7 기준으로 ΔG°’ 사용 (수소이온 농도 10⁻⁷ M)
연계 반응 (Coupled Reactions)
비자발적 반응(ΔG > 0)은 자발적 반응(ΔG < 0)과 coupling하여 진행될 수 있다.1
예시: ATP 가수분해(ΔG = −46 ~ −54 kJ/mol)를 이용해 에너지 비용이 드는 반응 구동.
→ ATP가 세포에서 이 역할을 담당.
Redox Reactions의 자발성
전자 전달 반응의 자발성은 **redox potential 차이 (ΔE’₀)**로 판단:
- n: 전달되는 전자 수
- ΔE’₀ (mV): 전자 수용체 E’₀ − 전자 공여체 E’₀
- ΔE’₀ > 0 이면 ΔG° < 0 → 자발적 전자 전달
예시: NADH → O₂
- NADH/NAD⁺ E’₀ = −320 mV
- H₂O/O₂ E’₀ = +820 mV
- ΔE’₀ = 1140 mV → 매우 자발적 (ΔG° ≈ −219 kJ/mol for 2e⁻)
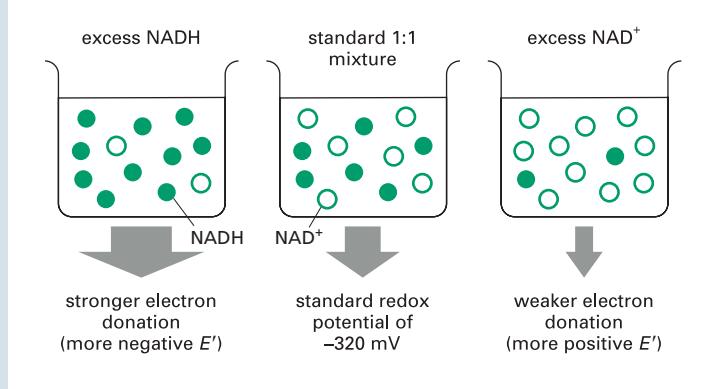 Panel 14-1: Redox potential 측정 방법과 ΔG 계산.
Panel 14-1: Redox potential 측정 방법과 ΔG 계산.
관련 개념
Footnotes
-
2023 기말 1번 — ③번 선지: ATP 가수분해(exergonic)와 비자발적 반응(endergonic)을 coupling하면 전체 반응을 자발적으로 만들 수 있다 → 옳은 선지. ↩