Fluorescent Biosensors for Cell Signaling
개요
Extracellular signals(세포외 신호)는 세포가 반응하는 방식에 중요한 역할을 하는 intracellular signaling molecules(세포내 신호 분자)의 농도에 빠르고 일시적인 변화를 일으킨다. 그러나 이러한 역동적이고 빠른 변화를 보고 측정하는 것은 여전히 과제로 남아 있다.
기존 방법의 한계와 발전
Simple Ion-sensitive Indicators
일부 분자의 경우:
- Ca²⁺ ions와 같은 일부 신호 분자는 simple ion-sensitive indicators 사용 가능
- Light emission이 local Ca²⁺ ion concentration을 반영 (Figure 9-21, Figure 15-31 참조)
한계: 제한된 종류의 분자에만 적용 가능, 특이성과 감도의 제약
Genetically Encoded Biosensors
개념
가장 민감한 indicators: 다양한 genetically encoded biosensors, 형광 단백질의 growing family에 기반
주요 장점
- 세포 특이적 합성: 관심 있는 특정 세포에서 합성 가능
- Targeting 용이성: Protein tags와 쉽게 융합, 세포 내 특정 목적지로 targeting
- Molecular informants: 세포 내 특정 위치에서 일시적 signaling events 보고
Biosensor의 구성 요소
Signaling molecule 수준의 변화를 관찰 가능한 형광 강도 변화로 전환하려면:
- Sensing Component(감지 구성 요소): Target signaling event에 반응, 신호 분자 감지
- Reporting Component(보고 구성 요소): 감지 반응을 가시적이고 정량화 가능한 output으로 변환
Biosensor의 작동 원리
FRET-based Biosensors
구성: 두 개의 연결된 형광 단백질, Förster resonance energy transfer를 겪을 수 있을 만큼 가까이 접근 가능
메커니즘: Connecting sensor module이 두 형광 단백질을 가까이 모으거나 멀리 떨어뜨림
Sensor Module
특성: 일반적으로 protein 또는 protein domain, target molecule에 결합 시 큰 conformational change 거침
기능: Target 분자 결합 감지 → 형광 단백질의 거리 변화 유도 → FRET 효율 변화
정량적 측정
Ratiometric Measurement
측정 방법: Biosensor의 두 형광 단백질이 방출하는 빛의 강도 비율 측정 → Target molecule 농도의 정량적 측정 제공
장점: 절대 형광 강도가 아닌 비율 사용, 더 정확하고 신뢰할 수 있는 측정, 조명 강도 변화에 덜 민감
Figure 9-21: Ca²⁺ 농도 시각화
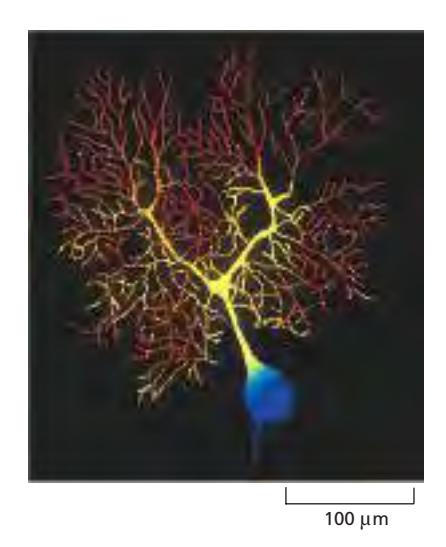
표본: 소뇌의 Purkinje cell (기니피그 뇌)
- Dendrites: 가지치는 수형 구조, 다른 neurons로부터 100,000개 이상의 synapses 수용
- 출력 경로: 단일 axon을 통해 세포 출력 전달
측정 방법:
- Indicator: Ca²⁺-sensitive fluorescent indicator fura-2, Low-light camera로 촬영
- 색상 코딩: 빨간색(가장 높은 농도) ~ 파란색(가장 낮은 농도)
관찰 결과: 가장 높은 Ca²⁺ levels는 수천 개의 dendritic branches에 존재
Figure 9-22: Genetically Encoded Fluorescent Biosensors

(A) Calcium Ion Biosensor 구축 전략
Sensor: Calmodulin (Figure 15-34 참조), Ca²⁺ 결합 시 큰 conformational change
구조: Blue fluorescent protein - Calmodulin sensor - Yellow fluorescent protein
작동 메커니즘:
- Ca²⁺이 calmodulin에 결합 → Conformational change
- Blue와 yellow fluorescent proteins 가까이 접근 → FRET 발생
- Violet excitation light 반응 → Fluorescence emission이 yellow로 변화
측정: 두 파장(blue와 yellow) 형광 강도 비율 측정 → Free Ca²⁺ 농도 정확히 측정
(B) cAMP Biosensor 구축
Sensor: cAMP-regulated guanine nucleotide exchange factor
작동: cAMP 결합 → Conformational change → 두 형광 단백질 멀어짐 → FRET 소멸 → Yellow에서 blue로 전환
차이점: Ca²⁺ sensor는 단백질 가까워짐(yellow 증가), cAMP sensor는 단백질 멀어짐(blue 증가)
(C) Arabidopsis Seedling의 Calcium Biosensor
실험: Shoot apical meristem 측면 epidermis 세포를 유리 needle로 찌름 → Calcium 유입 → 전체 meristem 표면에 걸쳐 calcium 파동으로 전파
생물학적 의의: Mechanical signals가 식물 형태형성 패턴화, 일시적 calcium responses가 cell polarity에 영향
다양한 Biosensors
Small Molecules
Ca²⁺, cAMP, IP₃, NADPH(redox state), H⁺ ions(pH), Neurotransmitters(acetylcholine, glutamate)
Enzyme Activity
Kinases, Phosphatases, Active caspases
기타
Temperature
현황: 수백 가지의 biosensors 생성, 계속 새로운 biosensors 개발 중
Biosensors의 장점
- 특이성: Target-specific, 높은 선택성, 다른 유사 분자와 구별
- 감도: 낮은 농도 감지, 빠른 변화 포착, 일시적 신호 감지
- 시공간적 해상도: 세포 내 특정 위치 targeting, 국소적 농도 변화 측정, 실시간 모니터링, Millisecond 단위 측정
- 비침습적: 세포 손상 최소화, 장기간 관찰, 정상적 세포 기능 유지
- 정량적 분석: Ratiometric measurement, 정확한 농도 측정, 비율 기반으로 artifacts 감소
응용 분야
Neuroscience: Synaptic signaling, Ca²⁺ dynamics, Neurotransmitter release, Synaptic plasticity
Cell Signaling: Signal transduction, Second messengers, Kinase cascades, Phosphatase activity
Metabolism: NADPH/NADP⁺ ratio, ATP levels, Metabolic switching, Energy homeostasis
Development: Morphogen gradients, Cell fate decisions, Mechanical signaling, Pattern formation
Disease Research: Cancer signaling, Neurodegenerative diseases, Metabolic disorders, Cardiovascular diseases
기술적 고려사항
Biosensor 설계: Sensor의 dynamic range, 결합 친화도, Conformational change 크기, 형광 단백질 선택
발현 수준: 너무 높으면 세포 기능 방해, 너무 낮으면 신호 약함, 내재 단백질과의 경쟁 고려
Calibration: In situ calibration, 최대/최소 신호 확인, 농도 변환 곡선
Biosensors vs 기존 방법
vs 화학적 Indicators:
- 화학적: 세포 내 로딩 필요, 특이성 제한적, Compartment targeting 어려움
- Genetically encoded: 유전적 발현, 높은 특이성, 정확한 targeting
vs 생화학적 분석:
- 생화학적: 세포 용해 필요, Population average, 시간적 해상도 낮음
- Biosensors: 살아있는 세포, 단일 세포 수준, 실시간 dynamics
미래 발전 방향
개선된 Sensors: 더 큰 dynamic range, 더 빠른 반응, 더 밝은 형광, 더 안정적 신호
Multiplexing: 여러 신호 분자 동시 모니터링, 신호 경로 상호작용 연구, Systems biology 접근
New Targets: 더 많은 신호 분자, Protein-protein interactions, Post-translational modifications, Lipid signaling
요약
핵심 원리: Genetically encoded fluorescent biosensors, FRET-based mechanism, Ratiometric measurement, 실시간 신호 분자 모니터링
주요 구성: Sensing component(target 감지), Reporting component(형광 변환), 두 형광 단백질(FRET 쌍)
측정 항목: Small molecules(Ca²⁺, cAMP, IP₃, NADPH, H⁺), Enzyme activities(kinases, phosphatases, caspases), Neurotransmitters, Temperature
생물학적 의의: Cell signaling dynamics, Neurotransmission, Metabolic regulation, Developmental processes, Disease mechanisms
참고 문헌
- Chapter 9: Visualizing Cells and Their Molecules, Section: “Fluorescent Biosensors Can Monitor Cell Signaling”
- Related Figures: 9-21, 9-22, 15-31, 15-34
- Related techniques: FRET, Fluorescent Protein Tagging in Living Cells