α-helix의 구조
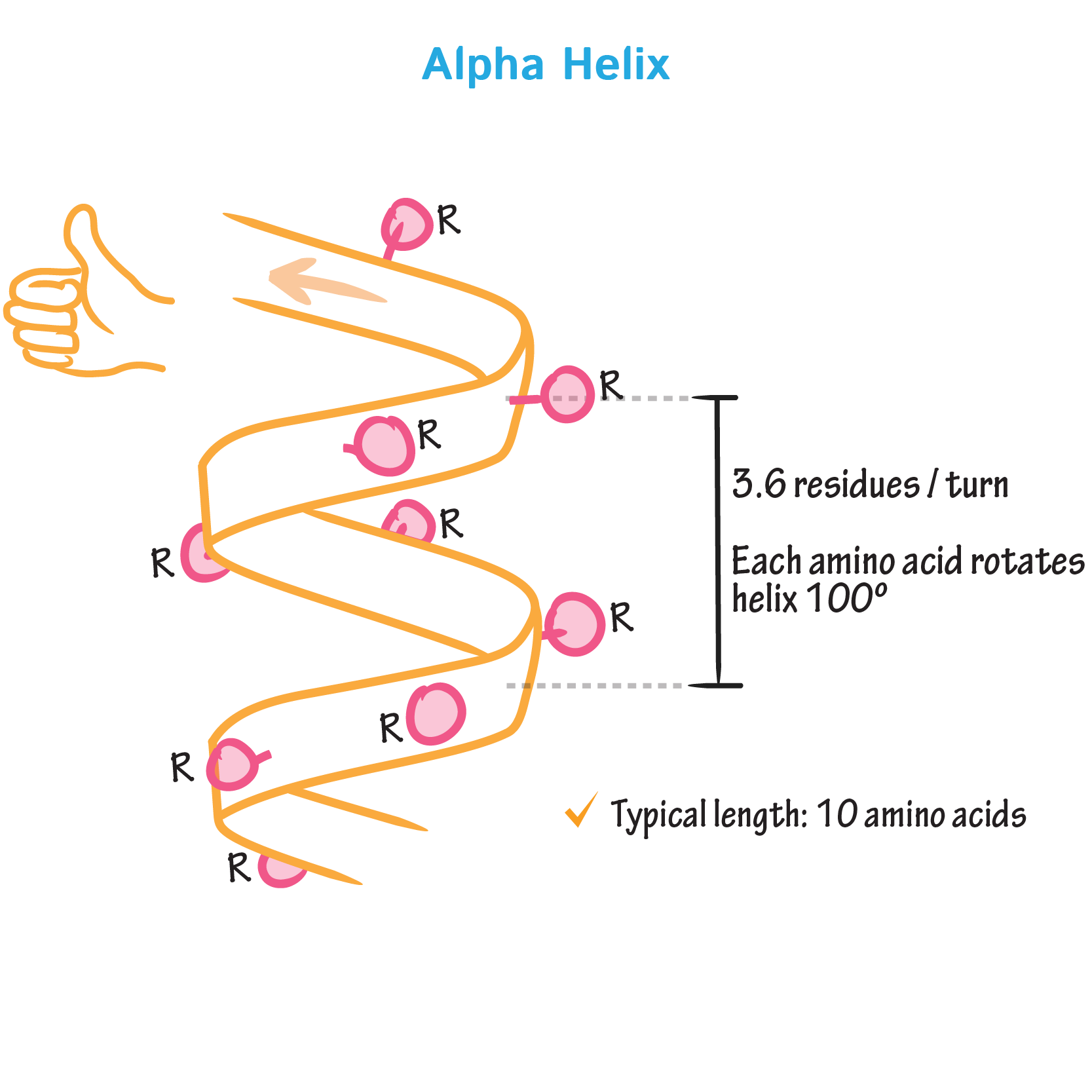 한 바퀴(360°) 완전히 회전하는 데 약 3.6개의 아미노산이 필요. 대략 아미노산 1개 = 100°
한 바퀴(360°) 완전히 회전하는 데 약 3.6개의 아미노산이 필요. 대략 아미노산 1개 = 100°
막 관통 α-helix
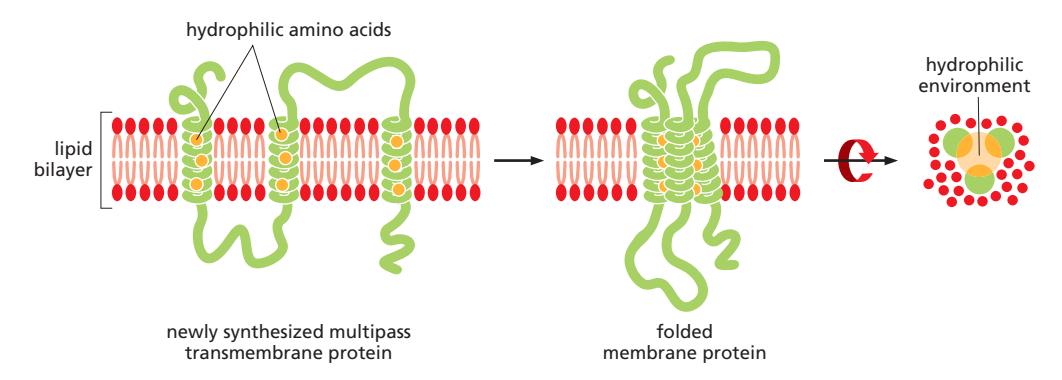
- 펩타이드 결합 자체는 친수성이지만
- 20-30개의 소수성 아미노산의 연속적 배치로 lipid에 박을 수 있다.
- hydropathy plot에서 +값이 나옴
막에 여러 helix가 연달아 붙어 있을 때
모든 아미노산 잔기가 소수성일 필요 없음. 다른 alphahelix와 맞닿은 부분이나 pore의 중심 부분은 hydrophobic할 이유 없음. 특히 pore는 중앙부는 친수성이어야 함. 따라서 이때 hydropathy plot으로 alpha helix의 관통 개수를 측정할 수는 없음.
Pore 형성을 위한 amphiphilic helix conformation
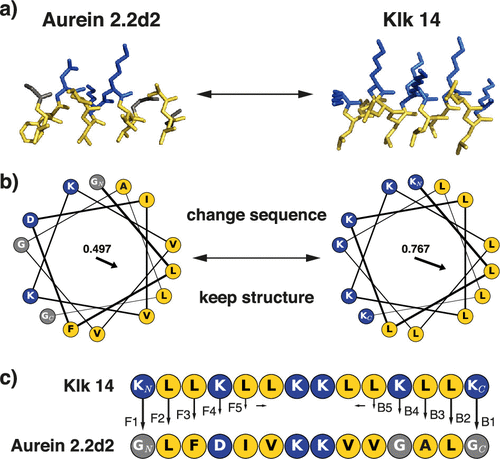 Pore 형성을 위한 헬릭스는 한쪽 면은 친수성, 반대쪽 면 (lipid와 접촉하는 쪽)은 소수성
Ex> 1번 아미노산: 구멍 안쪽(친수성)
2번 아미노산: 100° 회전 (여전히 안쪽 또는 측면)
3번 아미노산: 또 100° 회전 (이제 바깥쪽 지질을 향하기 시작함 - 소수성)
4번 아미노산: 또 100° 회전 (완전히 바깥쪽 지질 쪽 - 소수성)
3
Pore 형성을 위한 헬릭스는 한쪽 면은 친수성, 반대쪽 면 (lipid와 접촉하는 쪽)은 소수성
Ex> 1번 아미노산: 구멍 안쪽(친수성)
2번 아미노산: 100° 회전 (여전히 안쪽 또는 측면)
3번 아미노산: 또 100° 회전 (이제 바깥쪽 지질을 향하기 시작함 - 소수성)
4번 아미노산: 또 100° 회전 (완전히 바깥쪽 지질 쪽 - 소수성)
34개를 주기로 친수성, 소수성이 교대로 나타나면, 헬릭스가 계속 돌아가더라도 특정 각도 범위(예: 0°180°)에는 친수성 아미노산만, 나머지 각도(180°~360°)에는 소수성 아미노산만 모일 수 있음.
- 친소소친소소친친소소 이런식
Transmembrane α-helices는 유동적이고, 상호작용한다.
 domains나 단백질들이 lipid bilayer에서 유동적으로 움직이다가 모였을 때 기능을 하는 경우가 있음.
신호를 받고 모이는데,
domains나 단백질들이 lipid bilayer에서 유동적으로 움직이다가 모였을 때 기능을 하는 경우가 있음.
신호를 받고 모이는데,
- 신호 차단 방법 중 하나 : ligand trap할 수 있는 non-membrane protein을 투여하는 것.