Hydropathy Plot
Hydropathy plot은 protein의 amino acid sequence로부터 membrane-spanning segment를 예측하는 방법이다. X-ray crystallography와 single-particle cryo-electron microscopy의 발전으로 많은 membrane protein의 3차원 구조가 결정되었으며, 이는 amino acid sequence로부터 lipid bilayer를 확장하는 polypeptide chain 부분을 예측할 수 있음을 확인해주었다.
원리
Membrane-spanning α Helix의 특성
Transmembrane segment를 식별하기 위한 기준:
- 길이: 약 20-30 amino acid를 포함하는 segment1
- Hydrophobicity: 높은 정도의 hydrophobicity
- 구조: α helix로 lipid bilayer를 span하기에 충분한 길이
이러한 segment는 hydropathy plot에서 종종 식별될 수 있다.
방법론
Free Energy 계산
Hydropathy plot 생성 과정:
-
Segment 설정
- 고정된 크기의 segment 선택 (보통 10-20 amino acid)
- Polypeptide chain의 각 연속적인 amino acid에서 시작하여
-
Free Energy 계산
- Polypeptide chain의 연속적인 segment를 nonpolar solvent에서 물로 transfer하는데 필요한 free energy 계산
- Model compound로부터 얻은 data를 사용하여 각 segment의 amino acid 조성으로부터 계산
-
Hydropathy Index
-
결과 해석
- Amino acid sequence에서 hydrophobic segment의 위치에 peak 나타남
예시

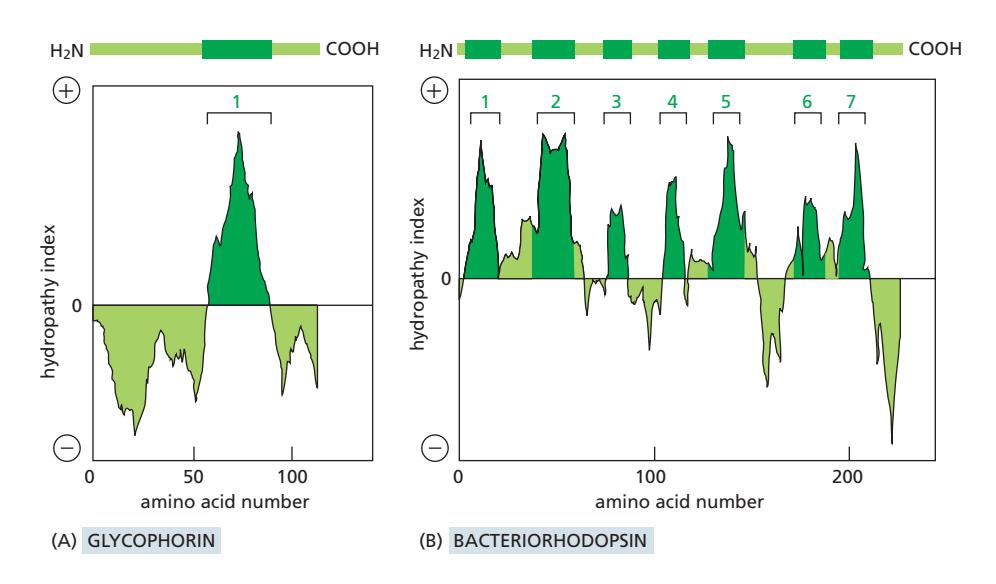
위 그림은 두 membrane protein의 hydropathy plot을 보여준다:
(A) Glycophorin
특성:
- Peak의 위치가 transmembrane segment 위치를 나타냄
- Peak의 높이가 hydrophobicity 정도를 나타냄
(B) Bacteriorhodopsin
특성:
- 각 peak가 하나의 transmembrane helix에 대응
- 7개의 distinct peak가 명확히 보임
한계
β Barrel의 경우
Hydropathy plot은 membrane-spanning β barrel의 segment를 식별할 수 없다:910
이유:
- β barrel을 횡단하는데 10개 이하의 amino acid로 충분
- Extended β strand로서
- 번갈아가며 나타나는 amino acid side chain만 hydrophobic하면 됨
- 따라서 hydropathy plot에서 명확한 peak를 형성하지 않음1112
옆의 helix와 붙어있는 경우
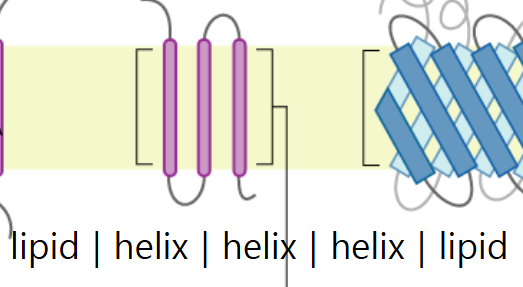 끼어있는 helix는 모든 AA가 hydrophobic일 필요가 없음.
끼어있는 helix는 모든 AA가 hydrophobic일 필요가 없음.
Partial Membrane Insertion
Multipass transmembrane protein은:
- Membrane을 완전히 span하지 않는 region도 포함 가능
- Membrane의 양쪽에서 folding하여 들어감
- Transmembrane α helix 사이의 공간으로 squeeze됨
- Bilayer의 hydrophobic core와 접촉하지 않음
이러한 region의 특성:
- 다른 polypeptide region과만 상호작용
- Hydrogen-bonding을 maximize할 필요 없음
- 다양한 secondary structure 가질 수 있음
- Partway across bilayer만 확장하는 helix 포함 가능
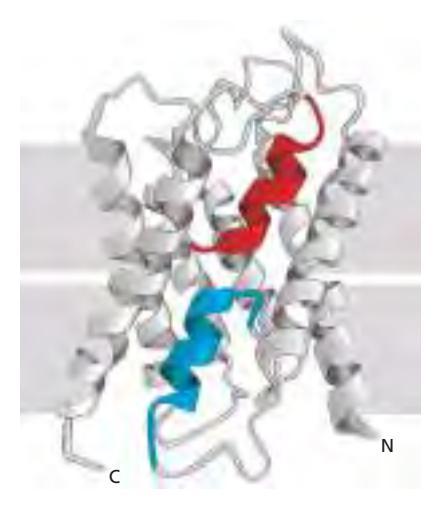
위 그림은 aquaporin water channel의 두 short α helix를 보여준다. 각각이 lipid bilayer를 halfway만 span한다. 이러한 colored helix는 protein-protein interaction에 의해 형성된 interface에 묻혀 있다.
결과:
- 이러한 region은 hydropathy plot에서 식별될 수 없음
- Protein의 3차원 구조 결정으로만 밝혀짐
- 또는 구조가 알려진 homologous protein과의 sequence alignment로
관련 개념
Footnotes
-
2025 중간 5번 — ⑤번 선지: TM α-helix는 약 20-30개의 연속 소수성 잔기가 필요 — 10개 이하로는 불충분 (오답) ↩
-
2025 중간 5번 — ②번 선지: Hydropathy plot에서 양의 값이 소수성 성질을 의미 (정답) ↩
-
2023 중간 17번 — ②번 선지: 양의 값은 소수성(물과 친화도 낮음)을 의미함 — “물과 친화도 높음”이라는 선지는 틀림 (오답) ↩
-
2023 중간 17번 — ③번 선지: (A) Glycophorin은 single membrane-spanning α helix 1개 → 3개라는 선지는 틀림 (오답) ↩
-
2025 중간 5번 — ④번 선지: (A) Glycophorin은 single α-helix로 막을 통과 — β-sheet 3개라는 선지는 틀림 (오답) ↩
-
2023 중간 17번 — Hydropathy plot에서 7개의 peak = 7개의 α-helix를 가진 7-pass transmembrane protein으로 예측할 수 있다는 내용이 정답 근거로 활용됨. 복기 불완전. (선지 미복기) ↩
-
2023 중간 17번 — ⑤번 선지: 여러 양의 peak = 여러 α-helix (β-sheet가 아님); Bacteriorhodopsin 7개 peak = 7 α-helix (오답) ↩
-
2025 중간 5번 — ①번 선지: (B) Bacteriorhodopsin은 7개의 α-helix → 4개라는 선지는 틀림 (오답) ↩
-
2023 중간 17번 — ④번 선지: β-barrel은 hydropathy plot으로 식별 불가 → “소수성으로 판단하기 쉽다”는 틀림 (오답) ↩
-
2025 중간 5번 — ③번 선지: β-barrel의 막 접촉 부분은 hydropathy plot으로 식별 불가 (오답) ↩
-
2022 중간 17번 — β-barrel transmembrane protein은 hydropathy plot으로 예측이 어렵다는 내용이 출제됨. 복기 불완전. (선지 미복기) ↩
-
2023 중간 23번 — β-barrel 막단백질은 짧은 β strand(10개 이하 아미노산)가 Extended β strand로 막을 횡단하며, 격번 아미노산의 소수성 side chain이 지질과 접촉한다는 내용이 출제됨. 복기 불완전. (선지 미복기) ↩