Membrane Protein
Lipid bilayer가 biological membrane의 기본 구조를 제공하는 반면, membrane protein은 대부분의 membrane 특정 작업을 수행하며, 각 type의 cell membrane에 특징적인 기능적 특성을 부여한다.
Membrane에서의 단백질 양
Membrane protein의 양과 type은 매우 가변적이다:
Myelin membrane:
- 주로 nerve cell axon의 electrical insulation 역할
- 25% 미만이 protein
ATP production membrane:
- Mitochondria와 chloroplast의 internal membrane
- 약 75%가 protein
전형적인 plasma membrane:
- 중간 정도
- 약 절반이 protein (mass 기준)
Lipid molecule 대비 수:
- Lipid molecule이 protein molecule보다 작기 때문에
- Cell membrane에는 항상 훨씬 더 많은 lipid molecule이 존재
- 50% protein (mass 기준)인 membrane에서도
- Protein molecule 하나당 약 50개의 lipid molecule
추정:
- 동물 genome에 encode된 protein의 약 30%가 membrane protein
- 세포 기능과 환경과의 상호작용에 필수적
Membrane Protein의 특성
Amphiphilic 특성
Lipid neighbor처럼 membrane protein도 amphiphilic이다:
- Hydrophobic region: Lipid bilayer를 통과하거나 membrane에 삽입
- Hydrophilic region: Membrane의 양쪽에 노출
Hydrophobic region:
- Membrane을 통과
- Bilayer 내부의 lipid molecule의 hydrophobic tail과 상호작용
- 물로부터 sequester됨
Hydrophilic region:
- Membrane 양쪽의 물에 노출
Membrane과의 결합 방식
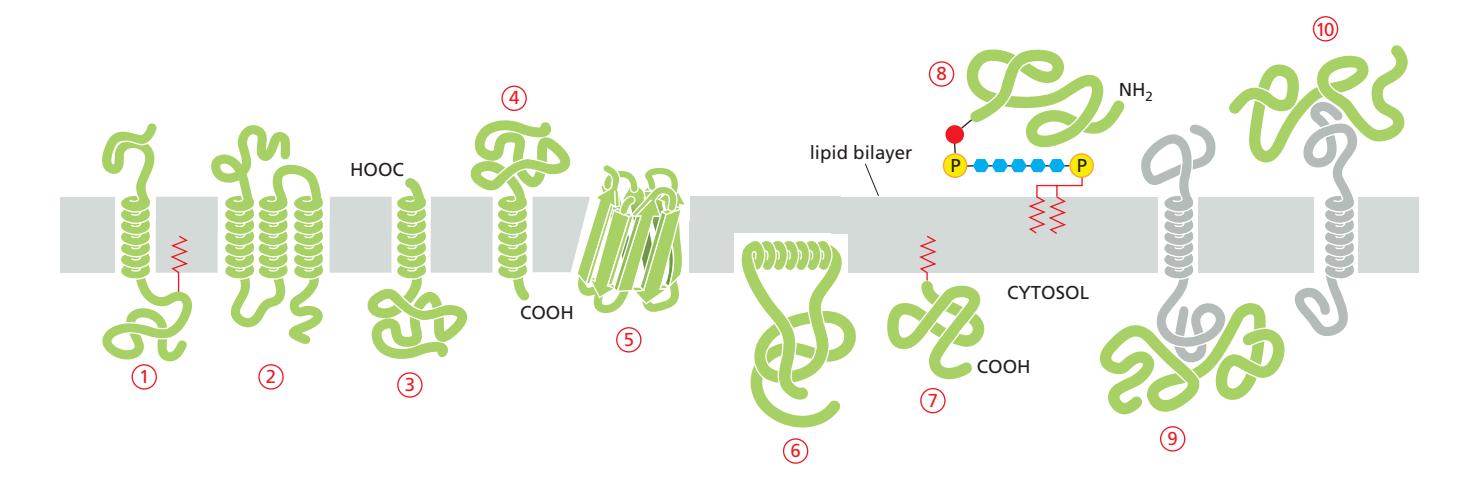
위 그림은 protein이 lipid bilayer와 결합하는 다양한 방식을 보여준다.
1. Transmembrane Protein
많은 membrane protein이 lipid bilayer를 확장하여 통과한다:
- Transmembrane protein으로 불림
- Mass의 일부가 membrane 양쪽에서 돌출
Single-pass transmembrane protein (예시 1):
- Polypeptide chain이 bilayer를 단일 α helix로 횡단
- 일부는 covalently attached fatty acid chain을 가짐
- Cytosolic lipid monolayer에 삽입됨
Multipass transmembrane protein (예시 2):
β barrel transmembrane protein (예시 5):
- Rolled-up β sheet (β barrel)로 bilayer 횡단
특정 측면 노출 (예시 3, 4):
- 일부 transmembrane protein은 membrane의 한쪽에만 주로 노출
- 예시 3: Golgi apparatus에서 glycosylation reaction을 수행하는 glycosyltransferase
- 예시 4: Membrane fusion을 촉매하는 SNARE protein
2. Lipid-anchored Protein
Cytosolic surface attachment (예시 6, 7):
- Amphiphilic α helix를 통한 부착 (예시 6)
- Helix의 hydrophobic face를 통해 cytosolic monolayer로 partition
- Covalently bound lipid chain을 통한 부착 (예시 7)
- Fatty acid chain 또는 prenyl group
- Lipid anchor 참조
Noncytosolic surface attachment (예시 8):
- Oligosaccharide linker를 통해 phosphatidylinositol에 부착
- GPI anchor로 불림
- GPI Anchor 참조
3. Membrane-associated Protein
Noncovalent interaction (예시 9, 10):
- 대신 다른 membrane protein과의 noncovalent interaction으로 결합
- Membrane 양쪽 face에 결합 가능
- 얘도 membrane protein
기능적 다양성
Membrane protein은 membrane의 거의 모든 다른 기능을 매개한다:
1. Transport
- 특정 molecule의 membrane 횡단 transport
- Multipass protein이 담당
- 작은 water-soluble molecule 전달
2. Enzymatic Activity
- Membrane-associated reaction의 촉매
- 예: ATP synthesis
3. Structural Link
Plasma membrane에서:
- Cytoskeleton과 extracellular matrix 연결
- 또는 인접 세포와 연결
- Lipid bilayer를 통과하는 transmembrane protein이 담당
4. Signal Transduction
Receptor 기능:
- 세포 환경의 chemical signal 감지 및 변환
- Cell surface에서 작동
5. Cell Recognition
- Cell-cell interaction 매개
- Cell adhesion 담당
Transmembrane Segment의 구조
α Helix 구조
대부분의 transmembrane protein에서:
- Polypeptide chain이 lipid bilayer를 α-helical conformation으로 횡단
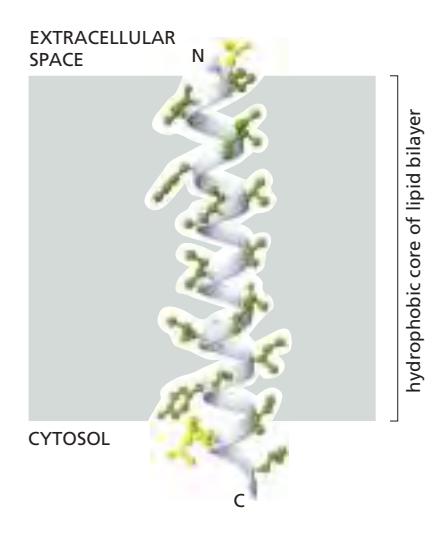
위 그림은 membrane-spanning polypeptide chain segment가 lipid bilayer를 α helix로 횡단하는 것을 보여준다. Glycophorin의 일부로 red blood cell plasma membrane에서 풍부하게 발견된다.
특성:
- 약 20-30 amino acid의 segment
- 높은 정도의 hydrophobicity
- α helix로 lipid bilayer를 span하기에 충분한 길이
- Hydropathy plot에서 확인 가능
β Barrel 구조
Multipass transmembrane protein의 또 다른 방식:
Glycosylation
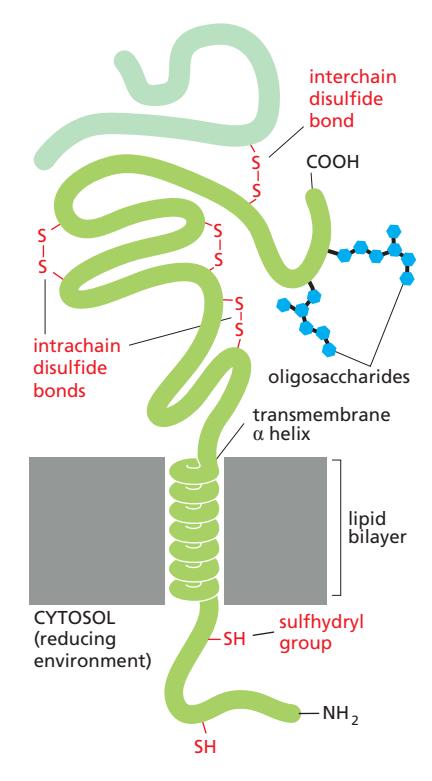
대부분의 transmembrane protein (동물 세포)은 glycosylate됨:
- Sugar residue가 ER과 Golgi apparatus의 lumen에서 추가됨
- oligosaccharyl transferase에 의해 asparagine으로 옮겨짐
- Oligosaccharide chain이 항상 membrane의 noncytosolic side에 존재56
위 그림은 single-pass transmembrane protein을 보여준다:
- Polypeptide chain이 right-handed α helix로 lipid bilayer 횡단
- Oligosaccharide chain과 disulfide bond가 모두 noncytosolic surface에 위치
- Sulfhydryl group이 disulfide bond 형성 (intrachain 또는 interchain)
- Cytosolic domain의 sulfhydryl group은 정상적으로 disulfide bond 형성 안 함57
- Reducing environment in cytosol이 이러한 group을 reduced (–SH) form으로 유지58
Membrane Protein의 이동성
많은 membrane protein이 빠르게:
그러나 세포는 특정 membrane protein을 고정시키거나 특정 domain에 국한시키는 방법을 가지고 있다.111213 Restricting domain of membrane protein 참조.
Carbohydrate Layer
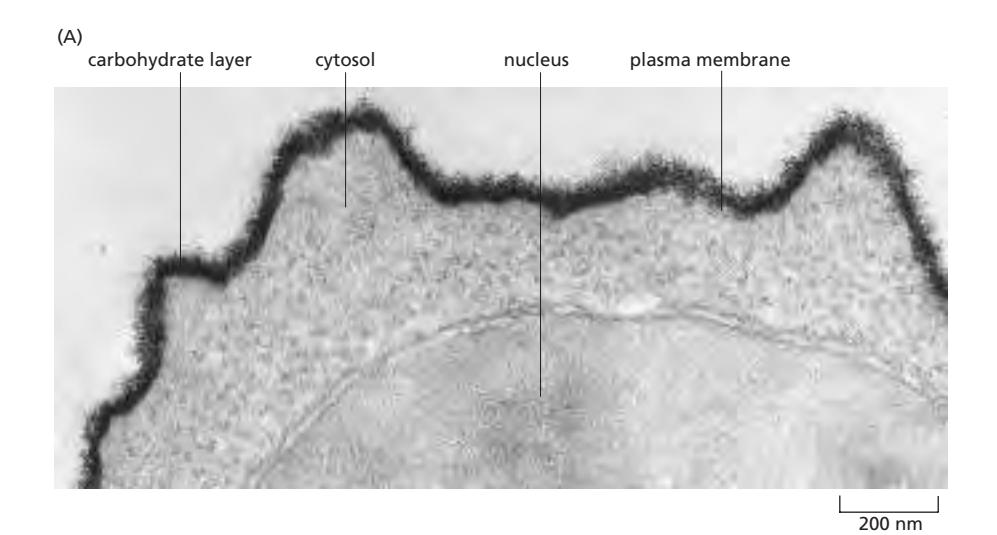 검게 염색된 부분이 당을 염색한 것.
검게 염색된 부분이 당을 염색한 것.
Glycoprotein과 Glycolipid의 carbohydrate는:
- 모든 진핵세포 표면의 carbohydrate-rich zone 형성
- Cell coat 또는 glycocalyx로 불림
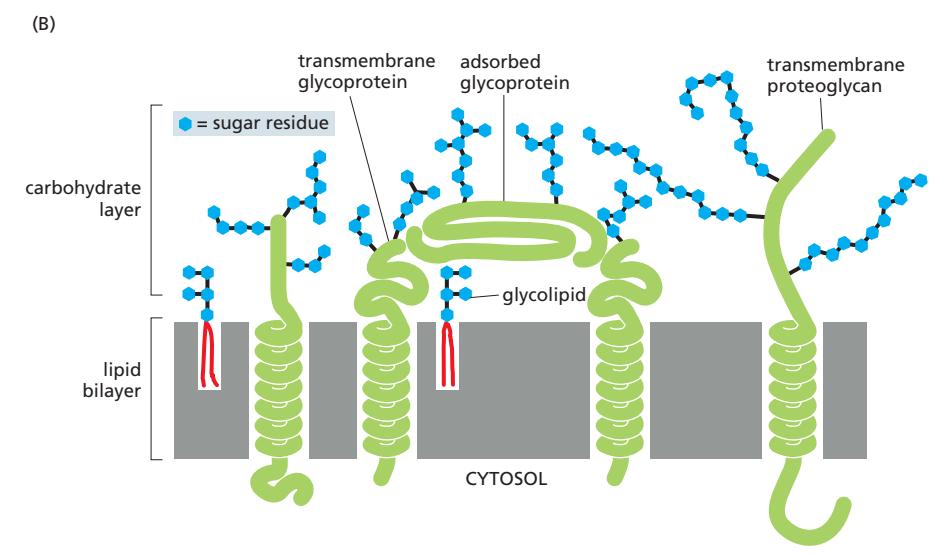
위 그림 (B)는 carbohydrate layer의 구성을 보여준다:
- Membrane glycolipid의 oligosaccharide side chain
- Membrane glycoprotein의 oligosaccharide side chain
- Membrane proteoglycan의 polysaccharide chain
- Adsorbed glycoprotein과 proteoglycan
기능:
- 기계적 및 화학적 손상으로부터 세포 보호
- 다른 세포를 거리에 유지
- 원하지 않는 cell-cell interaction 방지
관련 개념
- Lipid bilayer
- Lipid anchor
- Hydropathy plot
- Detergent
- Restricting domain of membrane protein
- Cortical cytoskeleton
- Membrane bending protein
- Glycolipid
Footnotes
-
2023 중간 17번 — Hydropathy plot의 peak 수로 α-helix 수를 예측할 수 있다는 내용이 출제됨. 복기 불완전. (선지 미복기) ↩
-
2023 중간 17번 — ①번 선지: (B) multipass transmembrane protein은 multiple α-helix로 막을 횡단 → 7개 peak = 7 α-helix 예측 가능 (정답) ↩
-
2022 중간 17번 — β-barrel 막단백질 구조에 관한 내용이 출제됨. 복기 불완전. (선지 미복기) ↩
-
2023 중간 23번 — β-barrel 막단백질에서 격번 아미노산의 소수성 side chain이 지질과 접촉하며, 짧은 β strand로 막을 횡단한다는 내용이 출제됨. 복기 불완전. (선지 미복기) ↩
-
2022 중간 18번 — 당 잔기는 ER/Golgi lumen에서 추가되어 noncytosolic side를 향함(선지 ④ 반박); cytosolic 도메인은 환원 환경으로 이황화 결합 형성 안 함(선지 ①⑤ 반박). 선지 ③(당단백질·당지질의 세포 인식 기여, 정답)은 Glycolipid/Carbohydrate layer 섹션 참조. ↩ ↩2 ↩3
-
2022 중간 18번 — ④번 선지: 당 잔기는 ER/Golgi lumen에서 추가 → noncytosolic side(세포 외부 방향)를 향함; cytosol 방향이 아님 (오답) ↩
-
2022 중간 18번 — ⑤번 선지: cytosolic domain의 sulfhydryl group은 reducing environment로 인해 이황화 결합을 형성하지 않음 (오답: cytosol 쪽 이황화결합 형성은 틀림) ↩
-
2022 중간 18번 — ①번 선지: cytosol은 reducing environment → 세포소기관 외부가 아닌 cytosol만 환원 환경 (오답: “모든 세포소기관 안쪽이 환원”은 틀림) ↩
-
2021 중간 미상E번 — 막단백질이 막 평면 내에서 lateral diffusion이 가능하다는 특성이 인간-마우스 세포융합 실험 맥락에서 출제됨. 복기 불완전. (선지 미복기) ↩
-
2023 중간 22번 — ①번 선지: 막단백질은 완전히 고정된 것이 아니라 lateral diffusion이 가능함 (오답: “이동하지 않는다”는 틀림) ↩
-
2022 중간 19번 — 막단백질은 lateral diffusion이 가능하지만, 세포는 이를 domain에 국한시키는 방법을 가짐 → 선지 ①(“자유롭게 이동”) 반박; 선지 ④(단백질-단백질 상호작용으로 고정, 정답) 근거. ↩
-
2023 중간 22번 — 막단백질은 lateral diffusion이 가능하지만 제한될 수 있음 (전반적 맥락) ↩
-
2022 중간 19번 — ①번 선지: 막단백질은 lateral diffusion이 가능하지만 자유롭게 이동하는 것은 아님 — 세포는 이를 domain에 국한시키는 방법을 가짐 (오답) ↩