Post-translational translocation
일부 단백질은 Endoplasmic Reticulum로 import되기 전에 cytosol에서 precursor로 완전히 합성되어, translocation이 항상 진행 중인 translation을 필요로 하지 않음을 보여준다.
특징
발생 빈도
효모 Endoplasmic Reticulum membrane과 진화적으로 관련된 bacterial plasma membrane을 가로지르는 post-translational 단백질 translocation이 더 흔하다. 두 경우 모두 Sec61 translocator(bacteria에서는 SecY)가 translocator로 사용된다.
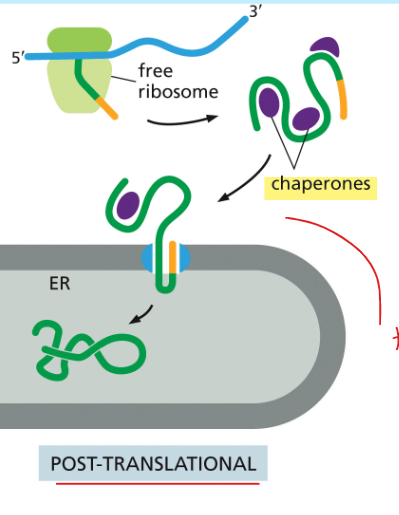
펼쳐진 상태 유지
Precursor protein은 초기 합성 후 cytosol에서 fold되지 않는다. 대신, 그들은 precursor folding 또는 응집을 방지하는 다른 cytosolic protein과 상호작용한다. 이러한 상호작용 단백질은 일반적으로 hsp70 family와 같은 일반적인 chaperone protein이며, 펼쳐진 polypeptide가 translocator를 통해 threading될 때 분리되어야 한다.
Translocator 개시
Co-translational translocation에서 논의된 것처럼, precursor의 signal peptide는 Sec61 complex에 직접 engage하여 channel을 연다. 그러나 membrane을 가로지르는 translocation의 다음 단계는 다르게 발생하며 lumenal 측면에서 polypeptide를 channel을 가로질러 당기거나 cytosol에서 channel로 공급하기 위해 세포 에너지를 사용하는 accessory protein에 의존한다.
Eukaryotic cell에서의 기전
Sec62-Sec63 complex 사용
Eukaryotic cell은 Sec61 translocator와 연결되는 Sec62-Sec63 complex라는 accessory protein을 사용하여 단백질을 Endoplasmic Reticulum lumen으로 당긴다.
BiP의 역할
Sec62-Sec63 complex는 translocation channel의 lumenal 개구부 인접 위치에 hsp70 유사 chaperone protein(BiP)을 배치한다. BiP에 의한 ATP 가수분해 구동 결합 및 방출 주기가 precursor가 Sec61 translocator에 초기 삽입된 후 단백질 import의 구동력을 제공한다.
Bacteria에서의 기전
SecA ATPase 사용
Bacteria는 에너지를 사용할 수 없는 세포 외 공간으로 직접 단백질을 수송하므로 SecA ATPase라는 cytosolic accessory protein을 사용한다. SecA는 precursor polypeptide에 결합하고 translocator의 cytosolic 측면에 부착되어 ATP 가수분해에 의해 구동되는 주기적 conformational change를 겪는다.