Sequential Use of Cleaved ER Signal and TM Segment During Membrane Protein Insertion
개요
많은 Transmembrane Protein들은 ER의 lumenal 면에 비교적 큰 N-말단 domain을 가진다. 이러한 단백질들은 **절단되는 ER signal sequence**와 **Transmembrane segment (TM segment)**를 순차적으로 사용하여 막에 올바르게 삽입된다.
이중 Signal 시스템의 필요성
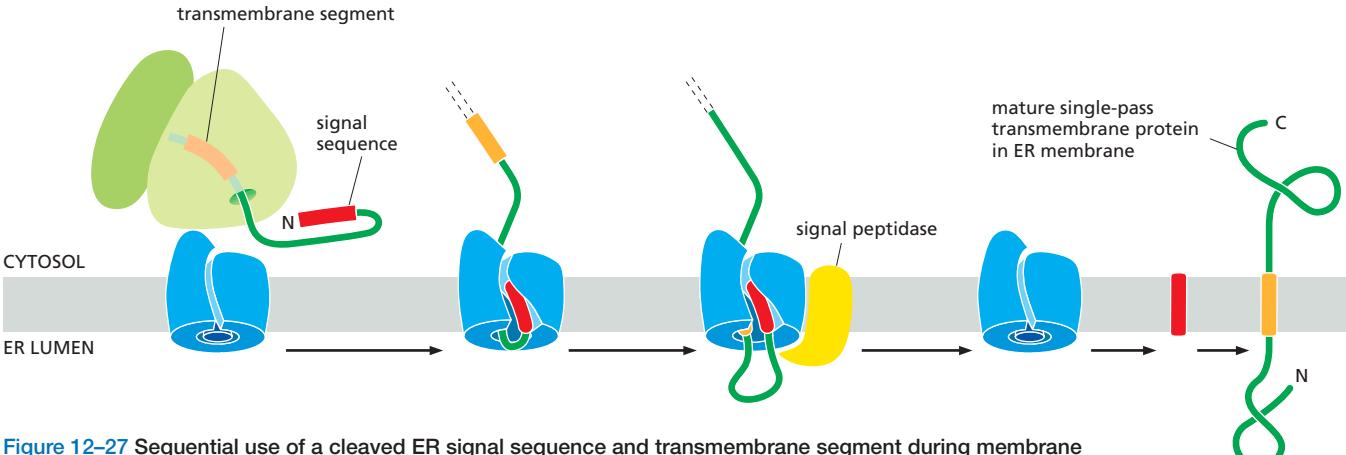
문제 상황
- N-말단 lumenal domain이 큰 경우
- 단일 Transmembrane segment만으로는 N-말단 전체를 lumen으로 이동시키기 어려움
해결책
- N-말단 ER signal sequence로 초기 translocation 개시
- 내부 Transmembrane segment로 membrane insertion 완성
막 삽입 메커니즘의 단계적 과정(N-말단 lumenal domain이 큰 경우)
1단계: ER Signal Sequence에 의한 초기 인식

Secretory protein과 동일한 과정:
- N-말단 ER signal sequence가 ribosome에서 나타남
- SRP가 signal sequence를 인식
- SRP가 SRP receptor를 통해 ribosome을 Sec61 translocator로 유도
- Signal sequence가 Sec61 translocator의 central channel에 삽입
2단계: N-말단 Domain의 Translocation
Secretory protein과 유사:
- Signal sequence가 Sec61 translocator를 열음
- N-말단 domain이 Sec61의 channel을 통해 ER lumen으로 translocation 시작
- Mature polypeptide의 N-말단이 signal sequence에 의해 ER lumen에 위치하도록 확정
3단계: Signal Sequence의 절단
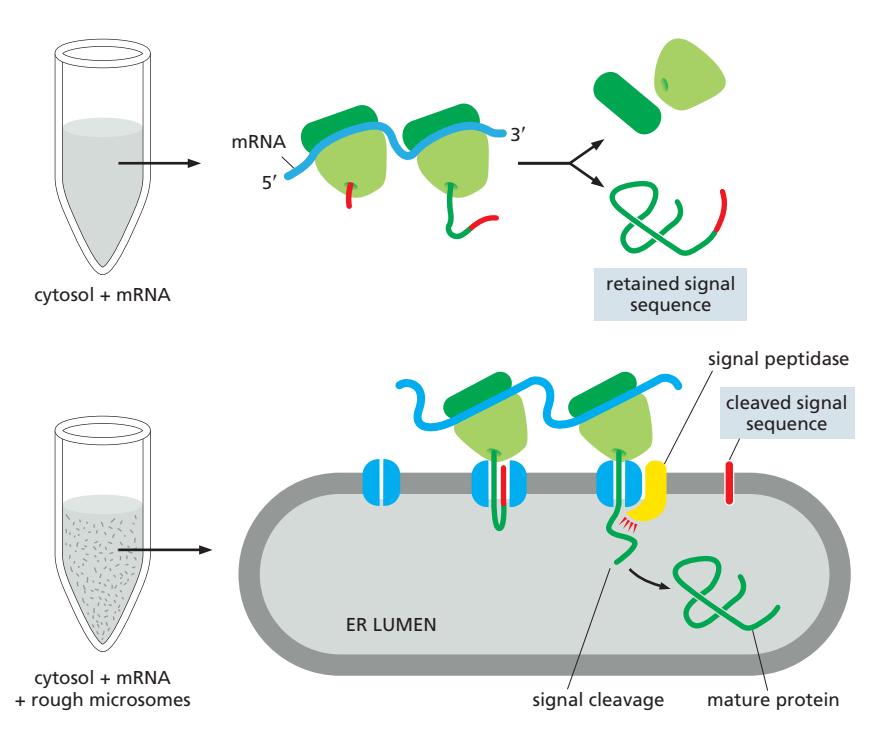
! 위 이미지는 secretory protein 가공 과정을 보여주지만 signal peptidase의 역할을 동일 ! Signal peptidase에 의한 절단:
- ER 막에 위치한 signal peptidase가 signal sequence를 인식
- Polypeptide chain이 완성되기 전에 signal sequence를 절단
- 절단된 signal sequence는:
- 막 내부로 lateral movement
- ER 막과 cytosol의 다른 protease에 의해 amino acid로 빠르게 분해됨
4단계: Transmembrane segment의 출현
Translocation 정지의 시작점:
- Polypeptide의 hydrophobic segment가 ribosome에서 나타남
- 이 segment가 Sec61 translocator로 들어감
- Sec61 translocator의 lateral gate에 삽입됨
5단계: Transmembrane segment의 막 통합

Translocation 종료 메커니즘:
- Hydrophobic segment가 lateral gate를 통해 lipid bilayer로 접근
- Hydrophobic segment는 aqueous channel보다 막에서 더 안정적임
- Lateral gate를 통해 channel을 laterally exit
- Translocation이 정지됨 이를 전이 정지(stop-transfer)라고 부름
6단계: C-말단 Domain 합성
Cytosolic 면에서의 완성:
- Transmembrane segment가 lipid bilayer에 고정된 후
- 단백질의 나머지 부분은 ER 막의 cytosolic 면에서 합성됨
- Translation이 종료될 때까지 계속됨
Membrane Protein Topology의 확립
Domain 위치 결정
최종 topology:
- N-말단 domain: ER lumen (나중에 cell exterior 또는 organelle lumen)
- Transmembrane segment: Lipid bilayer에 α-helix로 존재
- C-말단 domain: Cytosol
Topology 유지
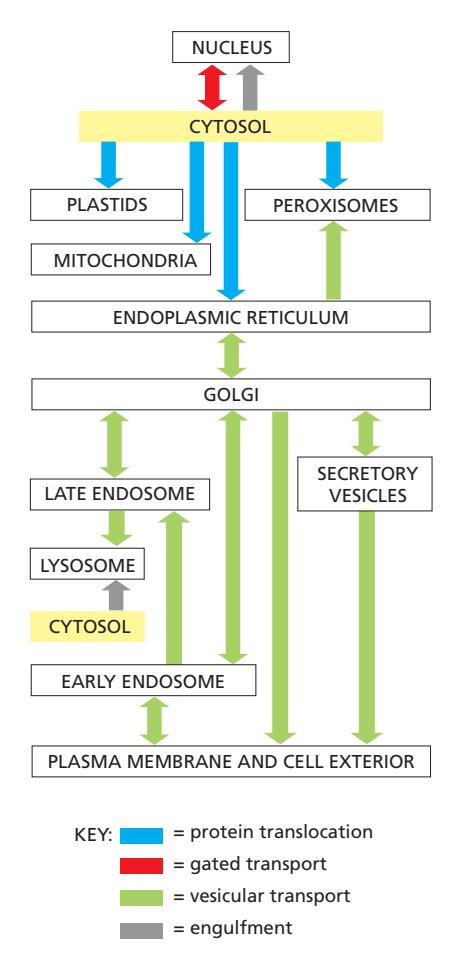
Programmed insertion:
- Membrane protein은 항상 ER의 cytosolic 면에서 삽입됨
- 이 방식으로 삽입된 단백질은 동일한 orientation을 유지
- 모든 후속 membrane transport 과정에서 topology가 보존됨
다른 막 삽입 경로와의 비교
Single-pass Transmembrane Protein (단일 TM segment만 사용)
- Transmembrane segment 자체가 signal sequence로 작용
- N-말단이 짧거나 cytosol에 위치
- Cleavable signal sequence 불필요
Multipass Transmembrane Protein Processing (여러 TM segment)
- 첫 번째 segment insertion 방식은 유사
- 후속 segment들이 순차적으로 추가됨
본 경로의 특징
- 큰 N-말단 lumenal domain에 최적화
- Signal sequence와 transmembrane segment의 기능 분리
- 복잡한 protein topology 생성 가능
기능적 의의
단백질 다양성
- 다양한 크기의 lumenal domain 수용 가능
- 복잡한 extracellular structure 형성 가능
Quality Control
- Signal sequence cleavage가 올바른 insertion의 지표
- 잘못 삽입된 단백질은 ERAD 경로로 분해
진화적 유연성
- Secretory protein과 membrane protein 사이의 evolutionary transition 용이
- Modular signal system
관련 개념
- Transmembrane Protein Insertion
- ER signal sequence
- Sec61 complex
- Signal peptidase
- lateral gate
- Single-pass Transmembrane Protein
- Membrane Protein Topology
요약
큰 N-말단 lumenal domain을 가진 membrane protein은 cleavable ER signal sequence와 transmembrane segment를 순차적으로 사용한다. N-말단 signal sequence가 초기 translocation을 개시하고 절단된 후, 내부 transmembrane segment가 Sec61 translocator의 lateral gate를 통해 lipid bilayer로 들어가 translocation을 정지시킨다. 이 mechanism은 두 signal의 기능을 분리하여 복잡한 membrane protein의 정확한 topology 확립을 가능하게 한다.