Pinching-Off
개요
Pinching-off는 budding vesicle이 donor membrane으로부터 완전히 분리되는 과정이다. 이 과정은 vesicle neck의 두 noncytosolic leaflet을 close proximity로 가져와 seal하여 완전한 vesicle을 형성한다.
Dynamin의 역할
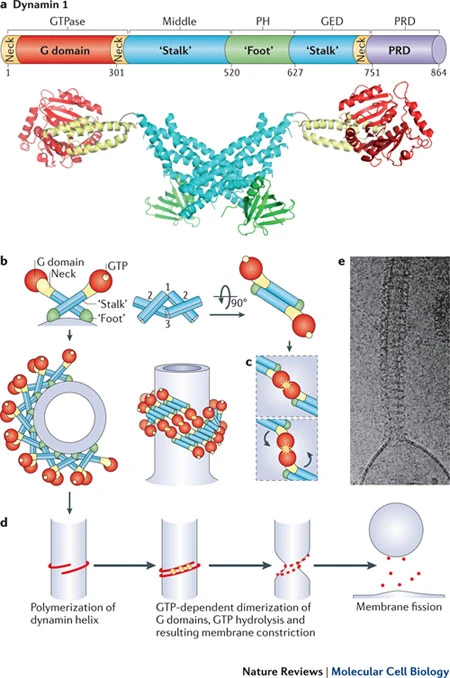
Dynamin은 주요 pinching-off protein이다:123
구조와 기능
- GTPase domain: GTP hydrolysis 조절
- PI(4,5)P2-binding domain= PH domain: cytosolic leaflet에 붙음. PI(4,5)P224
- middle domain/stalk : oligomerization
- Multiple dynamin molecule: Budding vesicle neck 주위에 spiral로 조립24
Pinching-off Mechanism
Assembly:
- Dynamin molecule들이 막의 PI(4,5)2와 결합하면서 결집하여 vesicle neck 주위에 ring 형성 24
- Ring이 spiral structure로 조립. polymer 형성24
- 동시에 자동으로 PI(4,5)2들도 모여있는 상태가 됨. 이는 머리가 큰 PI(4,5)2의 특성상 양의 곡률을 만듦.
Constriction:
- Bound GTP hydrolysis24
- Dynamin의 conformational change24
- Dynamin ring constriction24
- Underlying membrane neck도 함께 constrict
dynamin dimer란 무엇인가?
교과서에서는 stalk 부분이 붙어있는 두 dynamin을 dimer라고 부름. 수업에서는 “GTP dependent한 Dimerization”이라고 함 즉 G-domain이 서로 붙어 형성한 것도 dimer라고 할 수 있음.
G domain이 서로 붙어있을 때 GTPase활성이 크게 증가함. 4
Membrane Fusion:
- Neck 부위의 두 noncytosolic leaflet이 close proximity
- Leaflet끼리 flow together하여 seal
- Lipid-modifying enzyme recruitment하여 local lipid composition 변화로 membrane fusion 촉진
GTP Hydrolysis Cycle
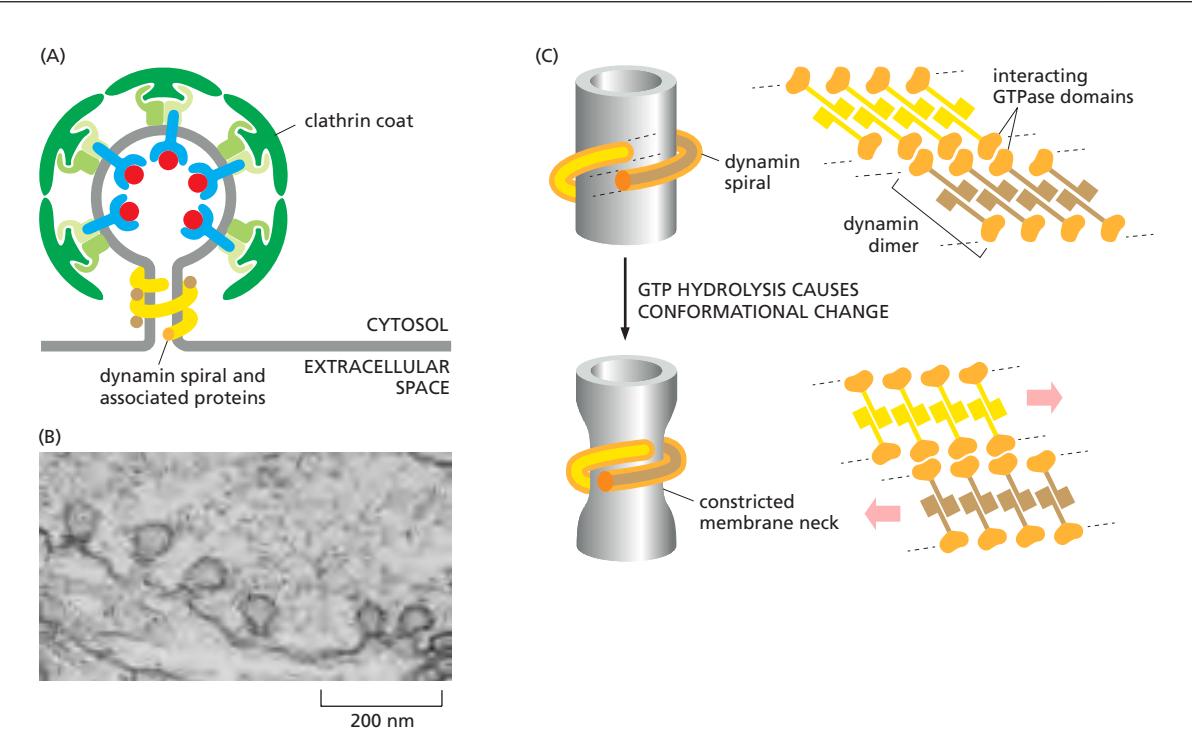 (B)는 dynamin이 제 역할을 못하는 mutation을 가진 초파리의 상태.
(B)는 dynamin이 제 역할을 못하는 mutation을 가진 초파리의 상태.
Dynamin의 작동은 GTP binding과 hydrolysis cycle을 통해 조절된다:
Stepping Model
- GTP binding: Dynamin dimer의 GTPase domain이 adjacent rung의 GTPase domain과 상호작용4
- GTP hydrolysis: Conformational change로 dynamin molecule compaction4
- Partial constriction: Dynamin spiral의 부분적 수축
- GTP loss: GTPase domain간 interaction 약화
- GTP rebinding: Dynamin이 adjacent position으로 이동
- Cycle repeat: 반복적인 compaction과 stepping으로 progressive constriction
Energy Source
- GTP hydrolysis의 energy가 membrane neck constriction을 power
- Cycle을 반복하며 점진적으로 neck 직경 감소
관련 내용
Footnotes
-
2022 중간 23번 — Dynamin의 GTPase domain, PI(4,5)P₂-binding PH domain, vesicle neck 주위 spiral 조립 후 GTP hydrolysis에 의한 constriction 메커니즘이 정답 근거로 활용됨. ↩
-
2023 중간 2번 — ①번 선지: 가수분해를 통해 polymerization을 한다 (틀림, polymerization 후 GTP 가수분해로 constriction·fission 발생, 순서 오류); ②번 선지: GTPase domain을 통해 PI(4,5)P₂에 결합한다 (틀림, PI(4,5)P₂ 결합은 PH domain 담당); ③번 선지: Membrane에 결합하지 않아도 기능을 할 수 있다 (틀림, membrane 결합 필수); ④번 선지: 가수분해를 통해 GTPase domain의 dimerization을 촉진한다 (틀림, dimerization 후 GTP 가수분해가 활성화되는 것); ⑤번 선지: 가수분해되면서 가수분해목 부분에 힘이 가해져 막이 절단되고 분리된다 (맞음, Dynamin은 neck에서 GTP 가수분해 에너지로 constriction → fission, 정답). ↩ ↩2 ↩3 ↩4 ↩5 ↩6 ↩7 ↩8
-
2025 중간 18번 — ②번 선지: Dynamin이 활성화되어 막이 폴리머화되어 분리된다 (틀림, PI(4,5)P₂가 분해되면 PH domain의 막 결합이 약화되어 Dynamin 활성 감소 → fission 저해). ↩
-
2025 중간 22번 — ①번 선지: G domain을 통해 dimer 형성 후 PI(4,5)P₂에 결합하게 된다 (틀림, PI(4,5)P₂ 결합은 PH domain 담당); ②번 선지: Dynamin은 막이 잘리는 초기 단계에서 clathrin 코트 내부에서 먼저 작용한다 (틀림, Dynamin은 neck에서 pinch-off 단계에 작용); ③번 선지: Dynamin의 polymerization을 통해 가수분해목을 하고 강하게 수축시켜 막을 분리시킨다 (틀림, polymerization 자체가 constriction 하는 것은 아님); ④번 선지: 소포체 lumen(내강)에 위치하다가 활성화되면 막을 감싸서 막의 분리를 촉진시킨다 (틀림, Dynamin은 세포질(cytoplasmic) 면에서 작동); ⑤번 선지: G domain의 dimer를 이루는 가수분해목 부분이 형성되어 막이 수축하는 변화가 발생하고 동시에 막의 목부분이 된다 (맞음, G domain dimerization → GTPase 활성화 → constriction → fission, 정답). ↩ ↩2 ↩3 ↩4 ↩5 ↩6 ↩7 ↩8 ↩9 ↩10