Intact Tissues Are Usually Fixed and Sectioned Before Microscopy Ch9, 페이지 10
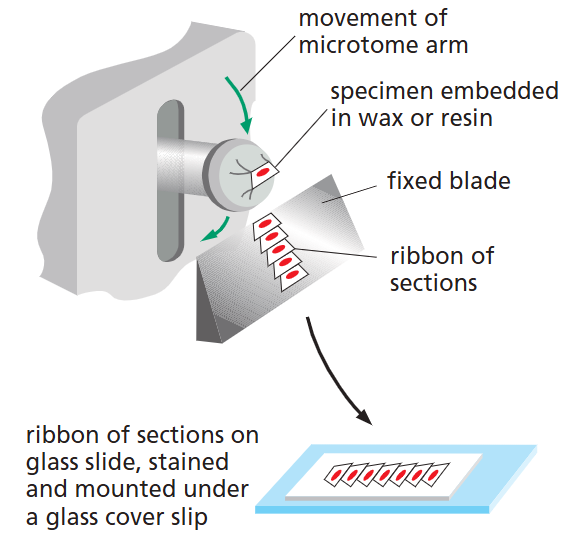 조직이 광학현미경 관찰 준비과정에서 microtome으로 잘려짐.
급속냉각된 샘플이 세포 구조를 더 잘 보존함
조직이 광학현미경 관찰 준비과정에서 microtome으로 잘려짐.
급속냉각된 샘플이 세포 구조를 더 잘 보존함
온전한 조직의 고정과 절편 제작
왜 절편이 필요한가?
배양된 개별 살아있는 세포를 관찰하는 것은 비교적 쉽지만, 대부분의 세포는 복잡한 조직과 기관에 존재. 대부분의 조직 샘플은 너무 두꺼워서 개별 세포를 고해상도로 직접 검사할 수 없기 때문에, 매우 얇고 투명한 조각인 절편(sections)으로 잘라야 함.
고정(Fixation)
목적: 조직 내 세포를 보존
고정액:
- 글루타르알데하이드(Glutaraldehyde): 가장 흔한 고정액
- 단백질의 자유 아미노기와 공유결합을 형성
- 단백질들을 교차결합(cross-linking)시켜 안정화하고 위치를 고정
포매(Embedding)
이유: 조직은 고정 후에도 일반적으로 부드럽고 연약하여 절편을 만들기 전에 냉동하거나 지지 매질에 포매해야 합니다.
포매 매질:
- 파라핀 또는 수지(resins)
- 액체 상태에서 고정된 조직에 침투하고 둘러쌈
- 냉각 또는 중합으로 경화되어 단단한 파라핀 블록 형성
절편 제작(Sectioning)
기구: 마이크로톰(Microtome)
- 강철 또는 유리로 만든 날카로운 날을 가진 기계
- 고기 슬라이서처럼 작동 (그림 9-8)
절편 두께: 일반적으로 0.5–10 μm1 마무리: 절편을 유리 현미경 슬라이드 표면에 평평하게 놓음
세 가지 주요 가시화 접근법
1. 염색(Staining)
- 유기 염료를 사용하여 특정 세포 하 구성 요소에 대한 특이적 친화성 이용
- **예시: H&E
- 음전하를 띤 분자에 친화성
- DNA, RNA, 산성 단백질의 일반적인 분포를 보여줌 (그림 9-9)
2.[Immunofluorescence Staining#^bbd9c5|형광 프로브]와 마커(antibody) 사용
- 관심 단백질을 국재화(localizing)하는 데 매우 민감한 접근법
- 일반적이고 광범위하게 적용 가능
- Antibody가 이용됨
Footnotes
-
2022 중간 2번 — 조직 절편 제작(fixation→embedding→sectioning by microtome, 절편 두께 0.5–10 μm) 및 가시화 방법에 관한 내용이 출제됨. 복기 불완전. (선지 미복기) ↩