Proteoglycan Assembly
Proteoglycan이란
Proteoglycan은 core 단백질에 하나 이상의 glycosaminoglycan chain이 공유적으로 부착된 분자이다. Glycosaminoglycan은 반복되는 disaccharide unit으로 구성된 길고 가지가 없는 중합체이다.
Golgi apparatus에서의 조립
Proteoglycan은 Golgi apparatus를 통과하면서 조립된다. 이 과정은 단백질이 받을 수 있는 가장 무거운 O-linked glycosylation 중 하나이다.
조립 과정
-
Core 단백질 준비: ER에서 합성되어 Golgi apparatus로 전달된 core 단백질
-
Glycosaminoglycan chain 중합화: Core 단백질의 serine 잔기에 glycosaminoglycan chain 중합
- 긴 unbranched 중합체
- 반복되는 disaccharide unit으로 구성
-
황산화: Glycosaminoglycan이 Golgi apparatus에서 즉시 중합된 직후 심하게 황산화됨
- 특징적인 큰 음전하의 상당 부분을 추가
Sulfation
PAPS를 사용한 황산화
Glycosaminoglycan의 당 황산화는:
- Sulfate donor: 3’-phosphoadenosine-5’-phosphosulfate (PAPS)
- PAPS는 세포질에서 trans Golgi network의 내강으로 운반됨
단백질의 일부 tyrosine도 Golgi apparatus를 떠나기 직전에 황산화된다. 이 경우도 PAPS에 의존한다.
Proteoglycan의 운명
조립된 proteoglycan은 여러 목적지로 전달될 수 있다:
1. 분비 Proteoglycan
많은 proteoglycan이 분비되어 세포외기질의 구성 요소가 된다. 예를 들어:
- Cartilage의 aggrecan
- Basement membrane의 perlecan
2. 막 고정 Proteoglycan
일부는 plasma membrane의 세포외 면에 고정된 채로 남는다. 예를 들어:
- Syndecan
- Glypican (GPI-anchored)
3. 점액성 물질의 주요 구성요소
일부 proteoglycan은 slimy material의 주요 구성 요소를 형성한다:
- 많은 상피 표면을 보호하기 위해 분비되는 점액의 mucus
O-linked Glycosylation과의 관계
Proteoglycan 조립은 O-linked glycosylation의 특수한 형태로 볼 수 있다.
일반적인 O-linked glycosylation:
- Selected serine 또는 threonine의 hydroxyl group에 당 추가
- 일부 경우 hydroxylated proline과 lysine (예: collagen)
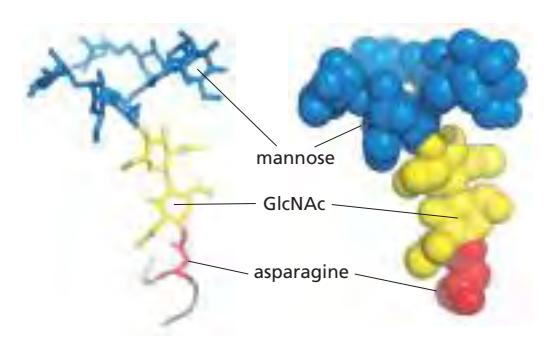
- N-acetylgalactosamine이 먼저 추가됨
- 몇 개에서 10개 이상의 추가 당이 이어짐
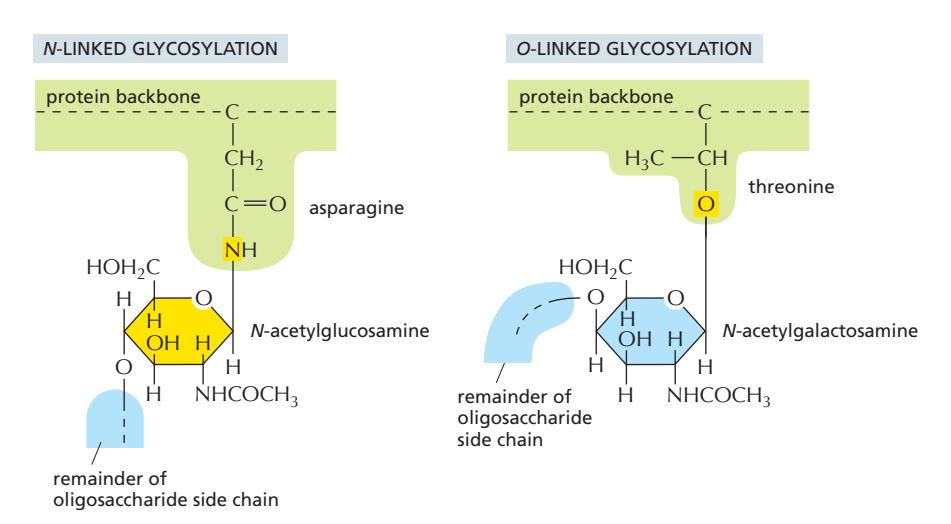
Mucin과의 비교
Mucin은 O-linked glycosylation이 가장 무거운 glycoprotein 중 하나이다:
- Mucus 분비물의 glycoprotein
- Proteoglycan core 단백질과 유사하게 무겁게 glycosylation됨
생물학적 의의
Proteoglycan의 조립과 분비는 다음에 중요하다:
- 세포외기질 구조: Proteoglycan은 조직의 구조적 완전성과 hydration에 기여
- 세포-세포 상호작용: 막 proteoglycan은 세포 표면 수용체로 작용 가능
- Growth factor 조절: 일부 proteoglycan은 growth factor를 결합하여 그 활성을 조절