Complex IV — Cytochrome c Oxidase
개요
Cytochrome c oxidase (Complex IV)는 ETC의 마지막 complex로, cytochrome c로부터 전자를 받아 O₂를 물(H₂O)로 환원시키는 반응을 촉매한다.1234 동시에 세 번째 proton pump로 기능한다.
- 위치: 미토콘드리아 crista membrane
- Proton pumping: 1 H⁺/electron (allosteric conformational change)
- 세포 전체 산소 소모의 약 90% 담당
구조
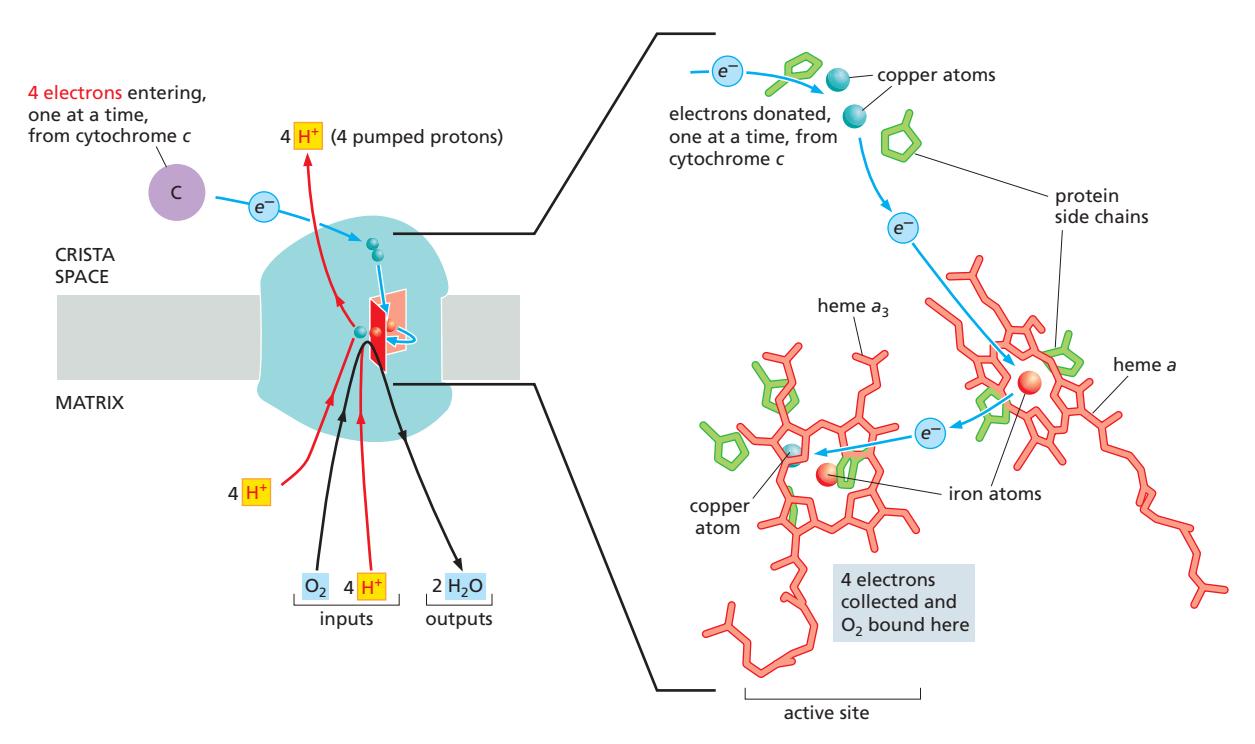 Figure 14-24: Cytochrome c oxidase 구조. ~13개 소단위, 총 ~204,000 dalton. 기능적 core (Subunit I, II, III)가 색으로 표시됨.
Figure 14-24: Cytochrome c oxidase 구조. ~13개 소단위, 총 ~204,000 dalton. 기능적 core (Subunit I, II, III)가 색으로 표시됨.
- ~13개의 단백질 소단위 (세포 종류에 따라 다름), 총 ~204,000 dalton
- 기능적 core를 이루는 3개의 핵심 소단위는 미토콘드리아 genome에 의해 encoding됨:
| 소단위 | 역할 |
|---|---|
| Subunit I (green) | Heme a 및 heme a₃ 포함. bimetallic center 구성 |
| Subunit II (purple) | Copper ions (Cu_A) 포함. Cytochrome c로부터 전자 수용 |
| Subunit III (blue) | 구조적 역할 |
전자 운반 cofactor: 2개의 copper ion (Cu_A, Cu_B) + 2개의 heme (a, a₃)
반응 메커니즘
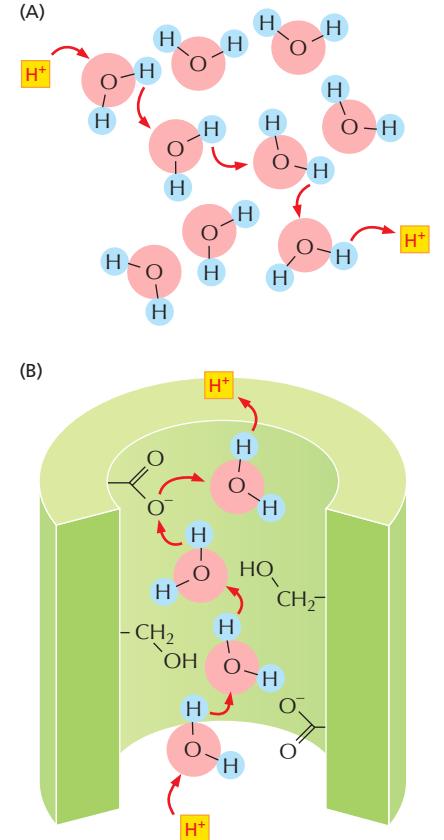 Figure 14-25: Cytochrome c oxidase에서 O₂와 전자의 반응. 전자 경로와 bimetallic center가 표시됨.
Figure 14-25: Cytochrome c oxidase에서 O₂와 전자의 반응. 전자 경로와 bimetallic center가 표시됨.
전자 흐름
Cytochrome c (crista space)
↓ (1개씩)
Cu_A (copper ions, Subunit II)
↓
Heme a (Subunit I) → 전자를 queue처럼 일시 저장
↓
Bimetallic center: Heme a₃ + Cu_B (Subunit I)
↓
O₂ → 2 H₂O
O₂ 환원 (bimetallic center)
- O₂가 heme a₃과 Cu_B 사이에 clamped되어 완전히 4개의 전자를 받을 때까지 유지
- 4 cytochrome c → 4 electrons + 4 H⁺ (matrix) → 1 O₂ → 2 H₂O
- 위험한 superoxide radical (O₂•⁻) 형성 없이 안전하게 환원
Proton pumping
- 동시에 4개의 proton을 추가로 matrix에서 crista space로 펌핑
- Allosteric conformational change에 의해 구동 (→ Proton pumping 참조)
전체 반응 요약
Cyanide 독성
Cyanide (CN⁻) 는 cytochrome c oxidase의 heme iron에 O₂보다 훨씬 강하게 결합하여 효소를 억제 → 미토콘드리아 ATP 생산 급감 → 치명적
진화적 중요성
- O₂를 최종 전자 수용체로 이용하는 것은 혐기성 대사보다 훨씬 많은 에너지 획득 가능
- 세포가 O₂를 직접 안전하게 다룰 수 있는 복잡한 화학이 필요했으며, Complex IV가 그 역할을 함
- 다세포 생물의 등장에 필수적인 에너지원을 제공
Footnotes
-
2022 기말 19번 — Cyanide의 Complex IV 억제 → ETC 정지 → ATP 합성 불가 → 사망 원리 서술형 문항. ↩
-
2023 기말 8번 — Cytochrome c는 Complex III에서 전자를 받아 Complex IV로 전달하므로, 선지 ④(“Complex I·II로부터 전자를 받아 Complex III에 전달”)가 옳지 않음이 정답 근거로 활용됨. ↩
-
2023 기말 11번 — Complex IV의 H⁺ 펌핑 원리(O₂ 환원 시 matrix H⁺ 소비 + 추가 H⁺ 능동 펌핑 2H⁺/2e⁻)가 서술형 답안의 핵심 내용. ↩
-
2023 기말 12번 — Antimycin A에 의한 Complex III 억제로 cytochrome c에 전자 공급이 없어지면 Complex IV도 정지하여 O₂ 소비가 감소한다는 서술형 풀이의 핵심 내용. ↩