FRET (Förster Resonance Energy Transfer)
개요
Fluorescent proteins는 이제 단순히 세포 내 특정 단백질의 위치를 확인하는 것을 넘어, kinetic properties(동역학적 특성)를 밝히고 다른 분자들과의 상호작용 여부를 파악하는 데 활용된다. FRET는 이러한 목적으로 사용되는 강력한 기술이다.
FRET의 정의
Förster Resonance Energy Transfer 또는 Fluorescence Resonance Energy Transfer
- 두 명칭 모두 FRET로 약칭됨
- 단백질 간 상호작용을 모니터링하는 기술
작동 원리
기본 구성
두 분자 표지: -관심 있는 두 분자를 각각 다른 fluorochrome으로 표지
- Fluorochrome 선택 기준:
- **Donor(공여체)**의 emission spectrum(방출 스펙트럼)
- **Acceptor(수용체)**의 absorption spectrum(흡수 스펙트럼)
- 두 스펙트럼이 overlap(겹침)해야 함1
Energy Transfer 메커니즘
조건:
- 두 단백질이 상호작용하여 fluorochromes가 매우 가까운 근접 거리(약 5 nm 이내)로 접근1
과정:
- 첫 번째 fluorochrome(donor)이 여기(excited)됨
- 흡수된 빛으로부터 에너지를 직접 다른 fluorochrome으로 전달
- 비방사적(nonradiatively) 전달 - resonance(공명)에 의해
- 결과: 첫 번째 fluorochrome의 excitation wavelength(여기 파장)로 조명하면
- 두 번째 fluorochrome의 emission wavelength(방출 파장)에서 형광 생성
Figure 9-19: Fluorescence Resonance Energy Transfer (FRET)

실험 설계
목적: 세포 내에서 두 단백질이 상호작용하는지(그리고 언제 상호작용하는지) 결정
준비:
- GFP의 서로 다른 색상 변이형에 부착된 fusion proteins로 먼저 생성
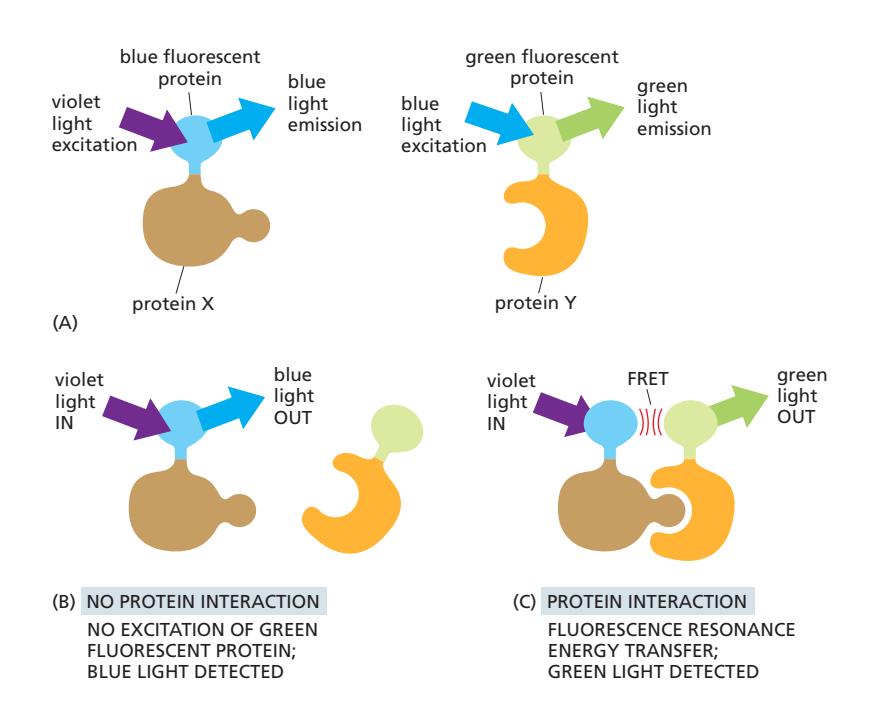
(A) FRET 시스템 구성
Protein X:
- Blue fluorescent protein에 연결
- Violet light(자색광)로 여기
- Blue light(청색광) 방출
Protein Y:
- Green fluorescent protein에 연결
- Blue light로 여기
- Green light(녹색광) 방출
(B) 상호작용 없을 때
실험 조건:
- Protein X와 Y가 상호작용하지 않음
- Violet light로 샘플 조명
결과:
- Blue fluorescent protein에서만 형광 발생
- Green fluorescent protein 형광 없음
(C) 상호작용 시 FRET 발생
실험 조건:
- Protein X와 protein Y가 상호작용
- Violet light로 샘플 조명
결과:
- Blue fluorescent protein이 여기됨
- Resonance transfer of energy(공명 에너지 전달) 발생
- 에너지가 green fluorescent protein으로 전달
- Green light 방출
중요 조건:
- Fluorochromes가 매우 가까워야 함
- 약 1-5 nm 이내
- 모든 protein X와 Y 분자가 항상 결합되어 있는 것은 아니므로 일부 blue light는 여전히 검출 가능
동적 변화 관찰:
- 두 단백질이 상호작용하기 시작하면:
- Donor blue fluorescent protein의 방출 감소
- Acceptor GFP의 방출 증가
GFP 변이형 사용
장점:
- GFP의 서로 다른 spectral variants를 fluorochromes로 사용
- 다양한 조합 가능
- 살아있는 세포에서 직접 관찰 가능
핵심 특징
1. 비침습적 관찰
- 살아있는 세포에서 실시간 모니터링2
- 세포 손상 최소화
2. 높은 공간 해상도
- 1-5 nm 범위의 분자 간 거리 측정1
- FRET 효율은 거리(r)의 6제곱에 반비례(1/r⁶)하므로, donor와 acceptor가 멀어질수록 FRET 효율은 감소한다.1
- 일반 광학 현미경(회절 한계 약 200 nm)보다 훨씬 높은 해상도
3. 동적 정보
- 단백질 상호작용의 시작과 종료 추적1
- 단백질 간 상호작용, 분자간 거리 측정, 세포 신호전달 등 다양한 목적에 사용되며 3차 구조 직접 관찰에만 한정되지 않는다.1
- 상호작용의 강도 변화 측정
4. 정량적 분석
- FRET 효율 측정을 통한 정량적 데이터 획득
- FRET은 비방사적(nonradiative) 공명 에너지 전달을 이용하며, 광표백(photobleaching)을 이용하는 FRAP과는 근본적으로 다른 원리이다.1
- 결합 친화도 및 해리 상수 계산 가능
참고 문헌
- Chapter 9: Visualizing Cells and Their Molecules
- Section: “Protein Dynamics Can Be Followed in Living Cells”
- Related Figure: 9-19, 15-49
- Related concepts: GFP, FRAP, Photoactivation
Footnotes
-
2025 중간 31번 — FRET는 두 분자가 ~5nm 이내일 때 발생한다는 선지 ②가 정답. 선지 ①(동일 파장 방출 시 발생) 오답 근거: donor emission과 acceptor absorption이 overlap해야 함. 선지 ③(거리 증가 시 효율 증가) 오답 근거: FRET 효율은 거리에 반비례(1-5nm 범위 측정). 선지 ④⑤ 오답 근거: FRET는 단백질 상호작용/분자간 거리 측정에 광범위하게 사용되며, photobleaching(FRAP)과 무관. ↩ ↩2 ↩3 ↩4 ↩5 ↩6 ↩7
-
2022 중간 7번 — Co-IP는 세포 용해 후 단백질 복합체를 검출(lysis artifact 가능)하는 반면, FRET는 살아있는 세포에서 실시간으로 단백질 상호작용을 관찰할 수 있어 in vivo 적합성이 더 높다는 차이가 정답 근거로 활용됨. ↩