개요
강한 background fluorescence(배경 형광)는 out-of-focus 분자들이 방출하거나 산란시킨 빛 때문에 발생하며, 이는 관심 있는 특정 분자의 형광을 가려버리는 경향이 있다. 이 문제는 total internal reflection fluorescence (TIRF) microscopy라는 특수한 광학 기술을 사용하여 해결할 수 있다.
TIRF의 원리
Total Internal Reflection
기본 메커니즘: TIRF microscope에서 laser light는 total internal reflection이 발생하는 정확한 임계각으로 cover-slip 표면에 비춘다.
Total internal reflection 때문에:
- 빛이 sample로 들어가지 않음
- 대부분의 형광 분자들은 조명되지 않음
Evanescent Field
전자기 에너지 확장:
- Total internal reflection에도 불구하고 전자기 에너지는 evanescent field로 확장됨
- Cover slip 표면 너머 매우 짧은 거리까지만 표본으로 연장
- Cover slip에 부착되었거나 표면에 매우 가까운 분자들만 여기됨
결과: 이 분자들이 형광을 발할 때, 방출된 빛은 더 이상 overlying molecules의 out-of-focus light와 경쟁하지 않으므로 검출 가능
Figure 9-38: TIRF Microscopy
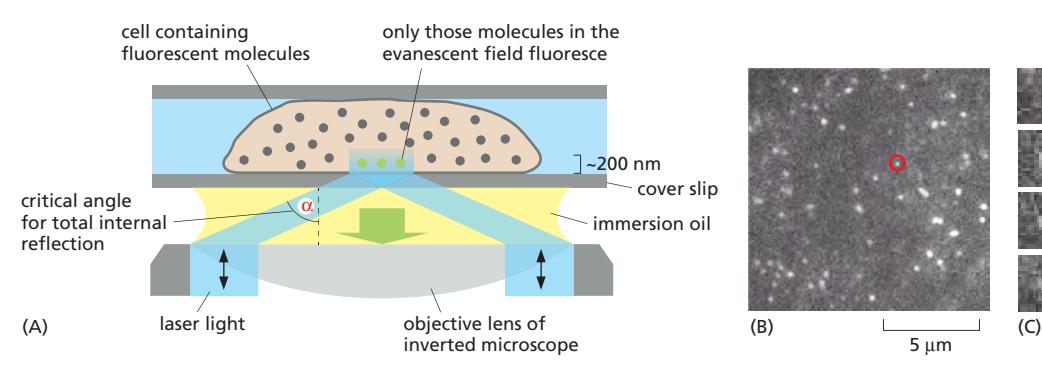
(A) TIRF의 광학적 원리
Excitatory laser light:
- Cover-slip 표면을 critical angle로 조명
- Glass-water interface에서 모든 빛이 반사됨 Evanescent wave:
- 일부 전자기 에너지가 interface를 가로질러 짧은 거리로 확장
- Cover slip에 부착되었거나 표면에 매우 가까운 분자들만 여기
- 약 200 nm 깊이까지만 효과적
(B) Clathrin-coated Pit 형성 추적
실험 시스템:
- Arabidopsis root cell의 plasma membrane 표면 이미지
- Clathrin adaptor protein이 GFP로 tagged 관찰:
- 개별 clathrin-coated pits를 시간에 따라 추적 가능
- Pit의 형성과 subsequent endocytosis 관찰
(C) 개별 Pit의 시간 경과
B에서 링으로 표시된 pit의 1초 간격 이미지:
- Pit의 출현
- Plasma membrane에서의 endocytosis에 의한 제거
- 전체 과정이 약 10초 소요
TIRF의 특징
제한된 깊이
현재 기술:
- 세포 표면 아래 약 200 nm 층으로 제한
- 매우 얇은 영역만 관찰 가능 이유:
- Evanescent wave의 침투 깊이가 매우 짧음
- Exponentially decay함
응용 가능 영역
세포 표면 근처 구조:
- Plasma membrane proteins
- Membrane-associated processes
- Cell adhesion molecules
- Receptor dynamics
TIRF의 주요 응용
1. Single Motor Proteins
극적인 실험 예시:
- 단일 motor proteins의 imaging
- Microtubules를 따라 이동하는 motor proteins
- Actin filaments를 따라 이동하는 motor proteins 장점:
- 개별 분자 수준의 관찰
- 이동 속도와 방향 정밀 측정
- Step size 측정 가능
2. Membrane Dynamics
Receptor trafficking:
- 세포막에서의 receptor 이동
- Clustering 형성
- Lateral diffusion Endocytosis/Exocytosis:
- Clathrin-coated pit 형성 (Figure 9-38B, C)
- Vesicle fusion
- Membrane recycling
3. Cell-Substrate Interactions
Focal adhesions:
- Adhesion complex 형성
- Cell migration 중 adhesion dynamics
- Force transmission
4. Single-Molecule Studies
DNA-protein interactions:
- DNA replication
- Transcription
- DNA repair Enzyme kinetics:
- 단일 효소 분자의 활성
- Substrate binding/release
- Catalytic cycles
변형 기술: Highly Inclined Laminated Optical Sheet
HILO Microscopy
원리:
- TIRF는 아니지만 유사한 접근
- 입사광의 각도를 줄임
- Cover slip에 거의 평행하게 조명 장점:
- 세포 내부 더 깊이 검사 가능
- 200 nm 이상의 깊이
- 균일하지는 않지만 더 넓은 영역 관찰 유용성:
- 식물 세포와 같이 outer wall이 있는 세포
- 곰팡이 세포
- 두꺼운 표본
TIRF의 장점
1. 극도로 낮은 Background
최소화된 배경 형광:
- Out-of-focus light 거의 완전 제거
- 매우 높은 signal-to-noise ratio
- Single-molecule detection 가능
2. 높은 시간 해상도
빠른 Imaging:
- 낮은 background로 인해 짧은 exposure time
- 빠른 동적 과정 추적
- Video rate imaging 가능
3. 광표백 최소화
제한된 조명:
- 표면 근처 분자들만 조명
- 세포 내부 형광 단백질 보존
- 장시간 관찰 가능
4. 광독성 감소
세포 손상 최소화:
- 제한된 영역만 조명
- 세포 전체에 대한 빛 노출 감소
- 살아있는 세포 장기 관찰
제한사항
1. 깊이 제한
얕은 침투:
- 약 200 nm로 제한
- 세포 내부 깊은 곳 관찰 불가
- 표면 현상에만 국한
2. 특수 장비 필요
기술적 요구사항:
- 정밀한 각도 제어
- 고품질 optics
- 특수 objective lens
- Laser illumination system
3. 샘플 준비
Cover slip 의존성:
- 세포가 cover slip에 부착되어야 함
- Floating cells는 관찰 어려움
- 조직 절편은 적용 불가
TIRF vs 다른 현미경 기술
vs Confocal Microscope
Confocal:
- 3D imaging 가능
- 더 깊은 침투 (수십 μm)
- Out-of-focus light를 pinhole로 제거 TIRF:
- 표면만 (200 nm)
- 더 낮은 background
- Single-molecule sensitivity
vs Wide-field Fluorescence
Wide-field:
- 전체 시편 조명
- 높은 background
- 깊이 전체 관찰 TIRF:
- 표면만 조명
- 극도로 낮은 background
- 표면 현상에 특화
vs FRAP
공통점:
- 살아있는 세포 dynamics 연구
- 형광 단백질 사용 차이점:
- TIRF: 공간 선택성 (표면)
- FRAP: 시간 선택성 (photobleaching)
실험적 고려사항
임계각 최적화
각도 조절:
- Total internal reflection을 위한 정확한 각도
- 너무 얕으면: 빛이 투과
- 너무 가파르면: 조명 영역 감소
Objective Lens
고 numerical aperture 필요:
- 일반적으로 NA > 1.4
- Oil-immersion objective
- TIRF-specific objectives
Illumination System
Laser 요구사항:
- 안정적인 laser source
- 적절한 파장
- 균일한 조명
기술적 발전
Improved Illumination
다양한 조명 방식:
- Through-the-objective TIRF
- Prism-based TIRF
- Variable angle TIRF
Multi-color TIRF
동시 다중 색상:
- 여러 형광 단백질 동시 관찰
- Protein-protein interactions
- Complex dynamics
Super-resolution TIRF
TIRF와 superresolution 결합:
- PALM/STORM과 조합
- 표면에서 nanometer resolution
- Single-molecule localization
생물학적 응용 예시
Membrane Protein Trafficking
Receptor dynamics:
- EGFR internalization
- GPCR signaling
- Ion channel gating
Cytoskeletal Dynamics
Actin polymerization:
- 세포 가장자리에서의 actin dynamics
- Lamellipodium formation
- Cell migration
Vesicle Fusion
Exocytosis:
- Synaptic vesicle fusion
- Hormone secretion
- Neurotransmitter release
Cell Adhesion
Focal adhesion dynamics:
- Integrin clustering
- Adhesion assembly/disassembly
- Force generation
데이터 분석
Single-Molecule Tracking
분석 방법:
- Particle tracking algorithms
- Trajectory analysis
- Diffusion coefficient 계산
Quantification
측정 가능한 parameters:
- Molecule count
- Dwell time
- Binding kinetics
- Diffusion rates
요약
핵심 원리: Total internal reflection으로 evanescent wave 생성, cover slip 표면 근처(~200 nm)만 조명, 극도로 낮은 background
주요 특징: Single-molecule sensitivity, 높은 시간 해상도, 최소 광표백, 표면 현상에 특화
주요 응용: Motor proteins imaging, Membrane dynamics, Endocytosis/exocytosis, Cell-substrate interactions, Single-molecule studies
제한사항: 깊이 제한(200 nm), 특수 장비 필요, Cover slip 의존성
생물학적 의의: Membrane trafficking, Cytoskeletal dynamics, Vesicle fusion, Cell adhesion, Molecular motors
참고 문헌
- Chapter 9: Visualizing Cells and Their Molecules, Section: “Single Molecules Can Be Visualized by Total Internal Reflection Fluorescence Microscopy”
- Related Figures: 9-38
- Related techniques: Confocal Microscope, FRAP, Fluorescent Protein Tagging in Living Cells