Stimulated Emission Depletion (STED) Microscopy
개요
STED microscopy는 point spread function의 크기를 줄여 회절 한계를 극복하는 superresolution 기술이다. 약 20 nm의 resolution을 달성할 수 있어, conventional light microscopy보다 약 10배 향상된 성능을 보인다.
Point Spread Function의 이해
기본 개념
Point spread function은 lens에 의해 점 광원이 초점을 맞출 때 형성되는 three-dimensional blurred image 내 빛 강도의 분포다. Diffraction effects 때문에 점 광원과 동일하게 imaging되는 대신, 이미지는 Gaussian distribution에 의해 대략적으로 설명되는 강도 분포를 가지며, 이것이 lens system의 resolution을 결정한다.
STED의 원리
Resolution 향상 방법: Excitation spot의 blurred periphery에 있는 모든 형광 분자들을 ground state나 정상적으로 형광을 내지 않는 state로 다시 전환하고, 매우 center에 있는 분자들만 기록되도록 남겨두는 것이다. ==depletion beam은 ‘유도방출’이라는 원리(photobleacing, photoactivation 아님)로 전자를 내린다. 형광분자가 빛을 방출하기 전에 다시 바닥상태로 돌아가게 하여 ‘형광을 끈다’==
Figure 9-30: Point Spread Function 크기 감소를 통한 Superresolution
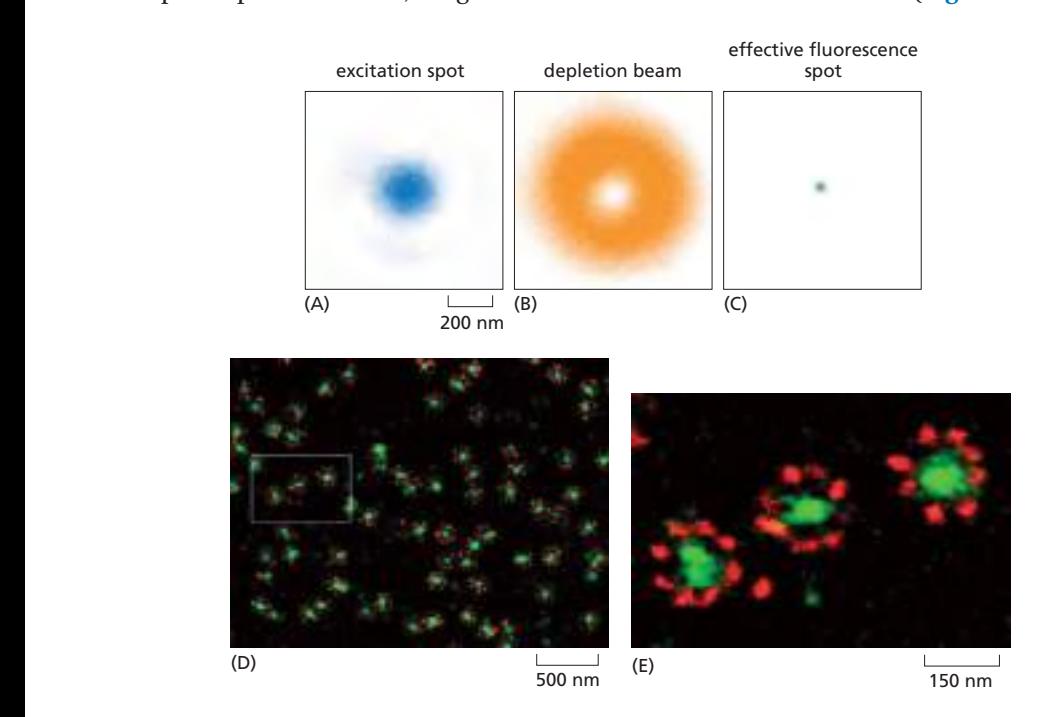
(A) Normal Focused Beam: 정상적인 focused beam of excitatory light의 크기 (B) Doughnut-shaped Depletion Beam: 극도로 강한 superimposed laser beam이 다른 파장이며 torus(도넛) 모양으로, specimen의 모든 곳에서 emitted fluorescence를 depletion시킴. 단, beam의 정중앙은 제외.1 (C) Reduced Point Spread Function: Beam center에서 effective point spread function의 width 감소 작동 원리: Specimen을 scanning하면서 이 작은 point spread function이 STED(stimulated emission depletion) microscopy라 불리는 과정으로 선명한 이미지를 만듦. (D) Nuclear Pore STED Microscopy: STED microscopy를 사용하여 nuclear pore 구조 검사. 고정된 nuclear envelope 샘플을 indirect immunofluorescence로 염색하여 다양한 nuclear pore components에 대한 antibodies 사용. Membrane ring proteins(Figure 12-55 참조)는 red로 염색되고, pore center에 fibrils를 형성하는 FG repeat proteins는 green으로 염색됨. (E) Enlargement: Boxed region의 확대는 membrane ring proteins의 명확한 eightfold symmetry와 약 20 nm resolution의 central fibrillar region을 보여줌.
STED의 작동 메커니즘
Photoswitchable Fluorescent Probes
필수 요구사항: 사용되는 fluorescent probes는 photoswitchable이어야 함. 즉, 서로 다른 파장의 빛으로 emission을 가역적으로 켜고 끌 수 있어야 함.
Scanning Process
Specimen을 이러한 laser 배열로 scan하면서, fluorescent 분자들이 켜지고 꺼지며, 각 위치에서 작은 point spread function이 기록됨.1 Confocal Microscope와 유사한 방식으로 scan하지만, 유사하지만 매우 가까이 있는 분자들이 두 가지 다른 states(형광을 내는 것과 어두운 것) 중 하나에 있도록 보장하기 때문에 회절 한계를 극복함.
Resolution 달성
생물학적 표본에서: 20 nm의 resolutions가 달성되었음 (Figure 9-30 참조)
STED의 특징
주요 장점
- 높은 Resolution: 약 20 nm까지 도달 가능
- 생물학적 표본 적용: Biological specimens에서 실제로 구현 가능
- Confocal과 유사: 기존 confocal microscopy와 유사한 scanning 방식
- 직접적 관찰: Image reconstruction이 비교적 직관적
요구사항
- 고강도 Laser: 매우 밝은 depletion laser 필요
- 복잡한 광학 시스템: Doughnut-shaped beam 생성을 위한 정교한 optics
- Scanning 시간: Point-by-point scanning으로 시간 소요
다른 Superresolution 기술과 비교
vs SIM(Structured Illumination Microscopy): SIM은 모든 형광 dyes 사용 가능, 더 빠름, 하지만 resolution이 100 nm로 제한. STED는 20 nm까지 가능하지만 특수 probes 필요.
vs STORM: 유사한 resolution(~20 nm) 달성하지만 다른 원리 사용. PALM/STORM은 single-molecule localization 기반, STED는 point spread function 축소 기반.
vs Confocal Microscope: Confocal은 회절 한계 내(~200 nm), STED는 이를 10배 초과하여 극복.
참고 문헌
Chapter 9: Visualizing Cells and Their Molecules, Section: “Superresolution Fluorescence Techniques Can Overcome Diffraction-limited Resolution”, Related Figures: 9-29, 9-30, 12-55, Related concepts: deconvolution, SIM(Structured Illumination Microscopy), Confocal Microscope
Footnotes
-
2023 중간 14번 — STED는 여기 레이저(excitation beam)와 도넛 모양의 depletion 레이저를 동시에 사용하여 point spread function의 크기를 줄여 회절 한계를 극복한다는 원리가 정답 근거(선지 ⑤)로 활용됨. 선지 ③(STED는 이미지 재산출 과정 없이 관찰 가능) 오답 근거: STED는 confocal과 유사하게 point-by-point scanning 후 이미지 구성이 필요. 선지 ①②④는 SMLM/SIM 노트에서 오답 근거 확인. ↩ ↩2