Glucose Trimming
Glucose trimming은 N-linked oligosaccharide에서 glucose를 제거하고 재부착하여 단백질의 folding 상태를 표시하는 quality control 메커니즘이다. 이 과정은 Calnexin and Calreticulin과 함께 작동하여 불완전하게 접힌 단백질을 ER에 retention시킨다.
기본 메커니즘
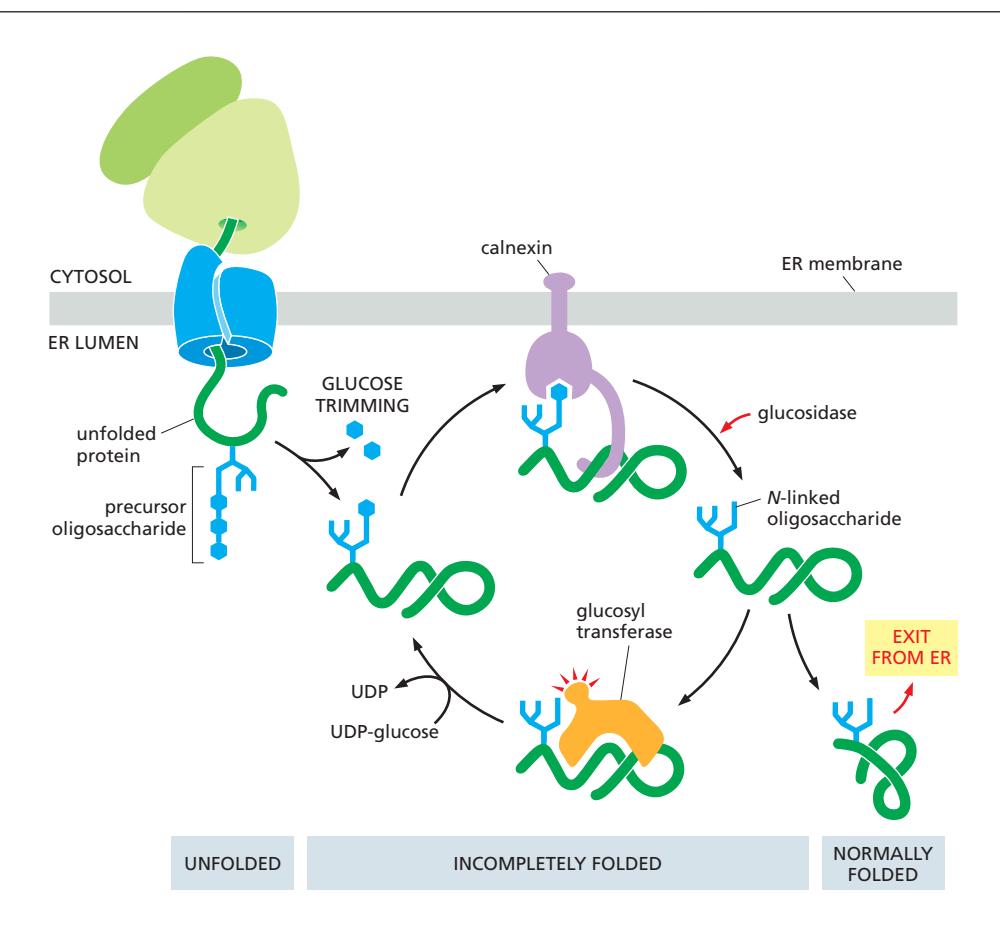
초기 상태
단백질이 ER로 translocation되면서 N-linked oligosaccharide를 부착받는다. 이 precursor oligosaccharide는 14개의 sugar로 구성되어 있으며, 그 중 3개가 glucose이다.
Step 1: Initial Trimming by Glucosidase
ER에 있는 glucosidase가 2개의 glucose를 빠르게 제거한다. 이 반응은 단백질이 ER로 들어온 직후 거의 즉시 일어난다. 결과적으로 1개의 terminal glucose만 남게 되는데, 이것이 singly glucosylated oligosaccharide이다.
Step 2: Calnexin/Calreticulin Binding
Singly glucosylated oligosaccharide는 Calnexin and Calreticulin의 인식 신호이다. 이 lectin chaperone들은 monoglucosylated glycoprotein에 결합하여 단백질이 ER을 빠져나가지 못하도록 retention시킨다. 이 결합 상태에서 단백질은 folding을 시도한다.
Step 3: Final Glucose Removal
Glucosidase가 마지막 남은 glucose도 제거한다. 이제 oligosaccharide에는 glucose가 하나도 없게 되고, calnexin/calreticulin이 단백질로부터 해리된다.
Step 4: Folding State Assessment
단백질이 calnexin/calreticulin로부터 해리된 후, glucosyl transferase가 단백질의 folding 상태를 평가한다. misfolded protein을 인식해 glucose를 재부착한다.
Glucosyl Transferase의 역할
Glucosyl transferase는 quality control의 핵심 효소이다. 이 효소는 불완전하게 접힌 단백질을 선택적으로 인식하여 terminal glucose를 재부착한다.
인식 메커니즘
Glucosyl transferase는 다음과 같은 특징을 가진 단백질을 misfolded로 판단한다:
- 노출된 hydrophobic region
- 비정상적인 structure
- 불완전한 folding intermediate
Glucose 재부착
불완전하게 접힌 단백질로 판단되면, glucosyl transferase가 UDP-glucose로부터 glucose 하나를 oligosaccharide에 transfer한다. 이렇게 다시 monoglucosylated 상태가 된 단백질은 calnexin/calreticulin에 다시 결합한다.
Quality Control Cycle
이 과정은 cycle을 형성한다:
- Monoglucosylated state: Calnexin/calreticulin 결합, ER retention
- Glucose 제거: Glucosidase 작용, chaperone 해리
- Folding 평가: Glucosyl transferase가 검사
- 두 가지 결과:
Cycle의 반복
이 cycle은 단백질이 완전히 접힐 때까지 반복된다. 각 cycle마다 단백질은 folding을 시도할 기회를 얻는다. Calnexin/calreticulin이 단백질의 aggregation을 방지1하면서 이러한 반복적인 folding 시도를 가능하게 한다.
올바른 Folding의 판정 원리
Properly Folded Protein
단백질이 올바르게 접히면:
- Hydrophobic region이 내부로 매립됨
- Native conformation 달성
- Glucosyl transferase가 더 이상 인식하지 않음
- Glucose가 재부착되지 않음
- De-glucosylated 상태로 ER 빠져나감
Incompletely Folded Protein
단백질이 불완전하게 접혔으면:
- Hydrophobic region이 노출됨
- Non-native conformation 유지
- Glucosyl transferase가 인식
- Glucose 재부착
- Calnexin/calreticulin과 재결합
시간 제한과의 연결
Glucose trimming cycle이 반복되는 동안 Mannosidase Timer도 동시에 작동한다. 단백질이 오랜 시간 동안 glucose trimming cycle을 반복하면, mannosidase가 terminal mannose를 제거하기 시작한다.
Mannose가 제거된 oligosaccharide는 더 이상 glucosyl transferase나 calnexin/calreticulin의 좋은 기질이 아니다. 대신 이것은 ER-associated degradation으로 향하는 signal이 된다. 이렇게 glucose trimming system과 mannosidase timer가 협력하여, 빠르게 접히는 단백질은 보호하고 오래 걸리는 단백질은 제거한다.
생리적 중요성
모든 Glycoprotein의 감시
거의 모든 N-linked glycoprotein이 이 system을 거친다. 이는 ER에서 합성되는 단백질의 약 절반에 해당한다. 따라서 glucose trimming은 ER quality control의 주요 축을 담당한다.
Folding 기회 제공
Cycle을 반복하면서 단백질은 여러 번 folding을 시도할 수 있다. Chaperone의 도움으로 aggregation을 피하면서 올바른 구조를 찾아갈 수 있다.
선택적 Retention
Glucose의 존재/부재가 명확한 on/off switch 역할을 한다. 이는 단백질의 ER retention과 export를 정밀하게 조절한다.
ERp57과의 협력
ERp57은 PDI family member로서 calreticulin과 함께 작동한다. ERp57은 free sulfhydryl group을 인식하여 불완전한 Disulfide bond formation을 감지한다.
단백질이 calnexin/calreticulin에 결합되어 있을 때, ERp57도 함께 recruit된다. 이렇게 oligosaccharide 상태(glucose 유무)와 disulfide bond 상태(free SH 유무)를 동시에 모니터링하여 더 정확한 quality control을 수행한다.
Non-Glycosylated Protein
Glucose trimming system은 glycoprotein에만 적용된다. Non-glycosylated protein은 BiP와 같은 다른 chaperone system에 의존한다. 이렇게 두 system이 complementary하게 작동하여 모든 ER protein을 감시한다.
관련 개념
- Calnexin and Calreticulin
- Mannosidase Timer
- Oligosaccharides
- Glycosylation
- Quality control of ER protein folding
- ER-associated degradation
- Protein folding in ER
Footnotes
-
2023 중간 19번 — ⑤ 정답: Glycosylation의 순차적 변형(glucose 잔기 수 3→2→1→0)이 단백질 접힘 진행 정도를 나타내는 타이머 역할. 올바르게 접힌 단백질만 glucose 재부착 없이 ER을 빠져나감. ③ 오답 근거: Calnexin/calreticulin은 aggregation을 방지하여 접힘을 돕는 역할을 함. ↩ ↩2
-
2023 중간 26번 — ② 옳음: ER lumen에서 N-linked glycosylation의 순차적 변형이 단백질 접힘 정도를 나타내며, 올바르게 접힌 단백질만 ER을 떠날 수 있음. ↩