Quality Control of ER Protein Folding
ER protein folding quality control은 ER에서 합성되는 단백질이 올바르게 접히는지를 감시하고, 잘못 접힌 단백질을 선별하여 제거하는 통합적인 시스템이다. 이 시스템은 여러 chaperone, folding enzyme, 그리고 degradation machinery가 협력하여 작동한다.
Quality Control의 필요성
ER는 수천 개의 서로 다른 단백질을 동시에 처리해야 하며, 높은 단백질 농도로 인해 aggregation 위험이 항상 존재한다. Co-translational folding과 post-translational folding이 동시에 일어나고, 복잡한 oligomeric assembly와 disulfide bond 형성이 필요하다. 만약 quality control이 실패하면 misfolded protein이 축적되어 ER stress를 유발하고, 결국 cellular dysfunction과 cell death로 이어질 수 있다.
Quality Control 시스템의 구성
1. 감시 메커니즘
ER은 세 가지 독립적인 감시 시스템을 통해 단백질의 folding 상태를 확인한다:
-
Glycosylation-Based Monitoring: N-linked oligosaccharide의 glucose를 제거하고 재부착하여 folding 상태를 표시한다. Calnexin and Calreticulin이 이 표지를 인식한다.
-
Hydrophobic region 감시: BiP가 노출된 hydrophobic sequence를 인식한다. 올바르게 접힌 단백질은 hydrophobic core가 내부에 매립되어 있지만, 잘못 접힌 단백질은 이러한 영역이 노출되어 있다.
- BiP는 정상상태에서는 단백질의 접힘을 돕고,
- 스트레스 상태에서는 misfolded protein을 붙잡아둔다.
- 이때 너무 오래 ER에 머무른 단백질은 mannose trimming에 의해 ERAD로 타겟팅된다.
-
Free sulfhydryl 감시: ERp57 chaperone이 짝짓기되지 않은 cysteine을 인식하여 불완전한 Disulfide bond formation을 표시한다.
2. 시간 기반 선별
Mannosidase Timer는 단백질이 ER에서 머무는 시간을 측정한다. 단백질이 오래 머물수록 ER-resident mannosidase가 terminal mannose를 제거하여 trimmed oligosaccharide를 생성한다. 이 trimmed oligosaccharide는 degradation signal로 작용하여 해당 단백질을 ER-associated degradation으로 보낸다.
3. UPR 적응 반응
단백질 misfolding이 과도하게 축적되면 Unfolded Protein Response가 활성화된다. UPR은 ER의 protein-processing capacity를 증가시키고, 새로운 단백질 합성을 일시적으로 감소시키며, ERAD 기능을 강화한다.
Quality Control Cycle
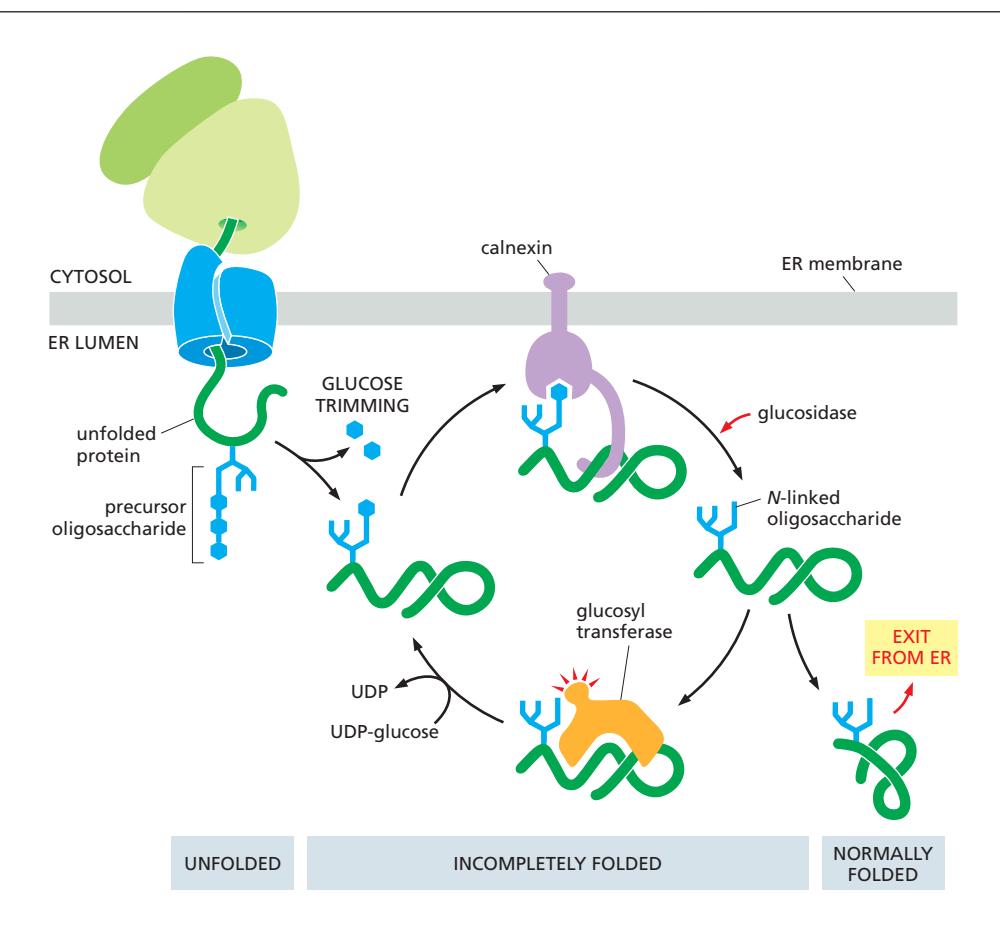
단백질이 ER로 들어온 후 거치는 단계는 다음과 같다:
Checkpoint 1: Initial Glycosylation
모든 glycoprotein은 N-linked oligosaccharide를 부착받는다. 이것이 quality control의 시작점이다.
Checkpoint 2: Glycosylation-Based Monitoring
ER glucosidase가 2개의 glucose를 제거하여 monoglucosylated oligosaccharide를 만든다. 이것이 Calnexin and Calreticulin을 recruit하는 신호가 된다.
Checkpoint 3: Folding Assessment
Glucosyl transferase가 단백질의 folding 상태를 평가한다. 올바르게 접혔으면 glucose를 제거된 상태로 유지하지만, 불완전하게 접혔으면 glucose를 다시 부착한다.
Checkpoint 4: Mannosidase Timer
단백질이 오래 머물면 mannosidase가 mannose를 제거한다. 빠르게 접히는 단백질은 이 단계 전에 ER을 빠져나가지만, 느리게 접히는 단백질은 mannose trimming을 받아 ERAD로 향한다.
결과 경로
성공: ER Export
다음 조건을 만족하는 단백질은 ER을 빠져나간다:
- 올바른 tertiary structure 형성
- 정확한 disulfide bond 배치
- 완전한 oligomeric assembly
- 시간 제한 내 folding 완료
이러한 단백질은 Golgi apparatus로 수송되어 추가 processing을 받고 최종 목적지로 향한다.
실패: ER-associated degradation
다음 조건을 보이는 단백질은 ERAD로 향한다:
- 지속적인 misfolding
- Trimmed oligosaccharides
- Assembly 실패
- 시간 제한 초과
이러한 단백질은 retrotranslocation을 통해 cytosol로 이동하고, proteasome에서 분해된다.
다중 센서의 통합
병렬 감시
여러 시스템이 동시에 작동한다:
- Glycan-based system (calreticulin)
- Hydrophobic-based system (BiP)
- Disulfide-based system (ERp57)
- Time-based system (mannosidase)
중복성과 특이성
이러한 중복성은 glycosylated protein과 non-glycosylated protein 모두를 감시할 수 있게 한다. 각 센서는 서로 다른 folding defect를 인식하므로, 다양한 문제에 맞춤형 대응이 가능하다.
질병과의 연관
α1-Antitrypsin Deficiency
Misfolded α1-antitrypsin이 quality control에 의해 ER에 retention되어 분비가 불충분해진다. 이는 폐와 간 질환을 유발한다.
Cystic Fibrosis (ΔF508-CFTR)
Misfolded CFTR channel이 ERAD에 의해 과도하게 분해되어 functional protein이 부족해진다. 이로 인해 chloride transport defect가 발생한다.
Protein Aggregation Diseases
Quality control이 실패하면 misfolded protein이 ER이나 downstream compartment에서 aggregate를 형성하여 cellular toxicity를 유발한다. Alzheimer’s disease, Parkinson’s disease, prion disease 등이 이에 해당한다.