Oligosaccharide Processing in Golgi
Golgi apparatus는 ER에서 전달받은 N-linked oligosaccharide를 처리하여 이질적인 oligosaccharide 구조를 생성한다.1
Processing의 시작
ER에서 단일 종류의 N-linked oligosaccharide가 많은 단백질에 부착되고, 단백질이 여전히 ER에 있는 동안 trimming된다. 이러한 trimming 반응에 의해 생성된 oligosaccharide intermediate는 단백질 folding을 돕고, misfolded 단백질을 세포질로 운반하여 proteasome에서 분해하는 데 중요한 역할을 한다.
CGN에 도착한 후, 단백질은 Golgi processing 구획의 첫 번째(cis Golgi cisterna)로 들어간다. 그런 다음 다음 구획(medial cisterna)으로 이동하고, 마지막으로 glycosylation이 완료되는 trans cisterna로 이동한다.
Processing 경로
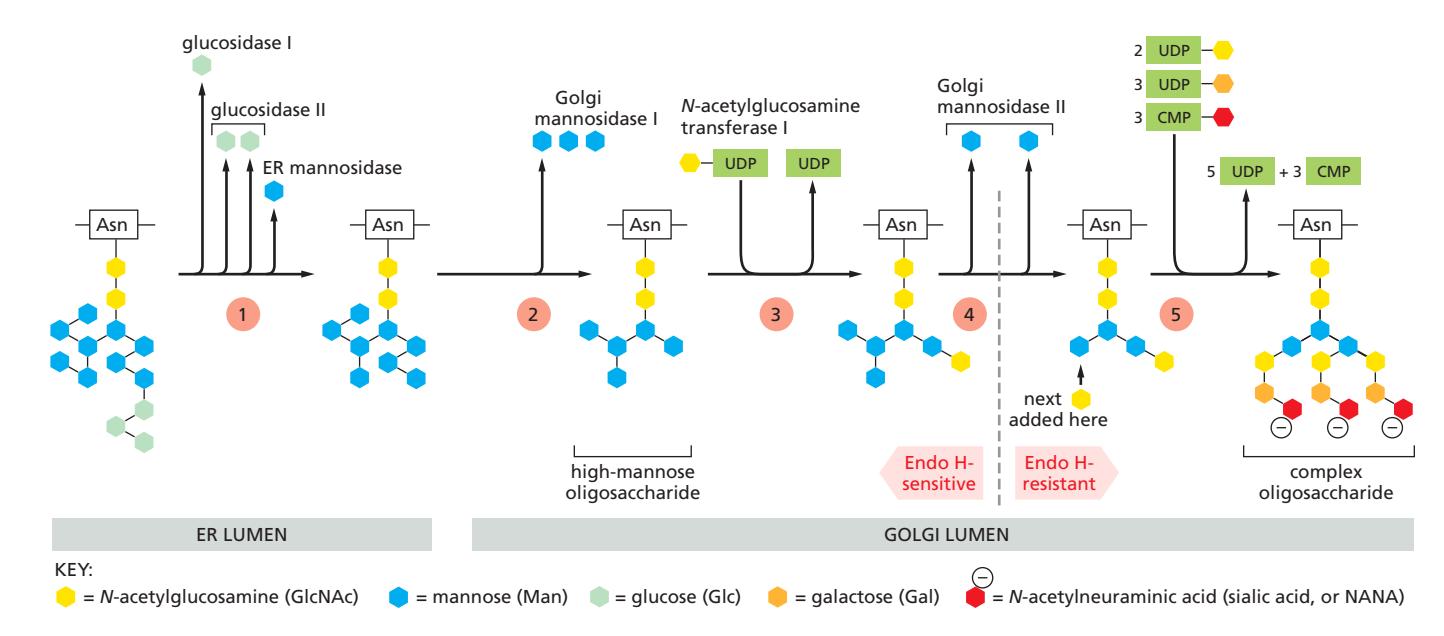
Oligosaccharide processing은 다음과 같이 순차적으로 진행된다:
ER에서 시작 (Step 1)
- N-linked glycosylation된 단백질에 대하여
- Glucose 제거: 단백질에 전달된 oligosaccharide에서 glucose 제거
- ER 막의 mannosidase: 특정 mannose 하나 제거
Golgi Stack에서 (Steps 2-5)
Step 2: Cis Golgi
Golgi mannosidase I: 3개의 mannose를 추가로 제거 mannose 5개 남은 high-mannose oligosaccharide 형성
Step 3: Medial Golgi
N-acetylglucosamine transferase I: N-acetylglucosamine 하나 추가
Step 4: Medial Golgi
Golgi mannosidase II: 2개의 mannose를 추가로 제거
- Complex oligosaccharide에 존재하는 3개의 mannose로 구성된 최종 core 생성
- 이 단계에서 core의 두 N-acetylglucosamine 사이의 결합이 highly specific endoglycosidase (Endo H)의 공격에 저항성이 됨
- Endo H 처리는 complex oligosaccharide와 high-mannose oligosaccharide를 구별하는 데 널리 사용됨
Step 5: Trans Golgi와 TGN
추가 당의 부가:
- N-acetylglucosamine
- Galactose
- Sialic acid
이러한 최종 단계는 순차적으로 작용하는 세 가지 유형의 glycosyl transferase 효소에 의해 수행된다:
- 표시된 nucleotide에 연결되어 활성화된 sugar 기질 사용
- Golgi cisternae의 막은 각 sugar nucleotide가 교환을 통해 들어갈 수 있도록 하는 특정 carrier 단백질 포함
- 당이 내강 면의 단백질에 부착된 후 방출되는 nucleoside phosphate와 교환
두 가지 Oligosaccharide 클래스
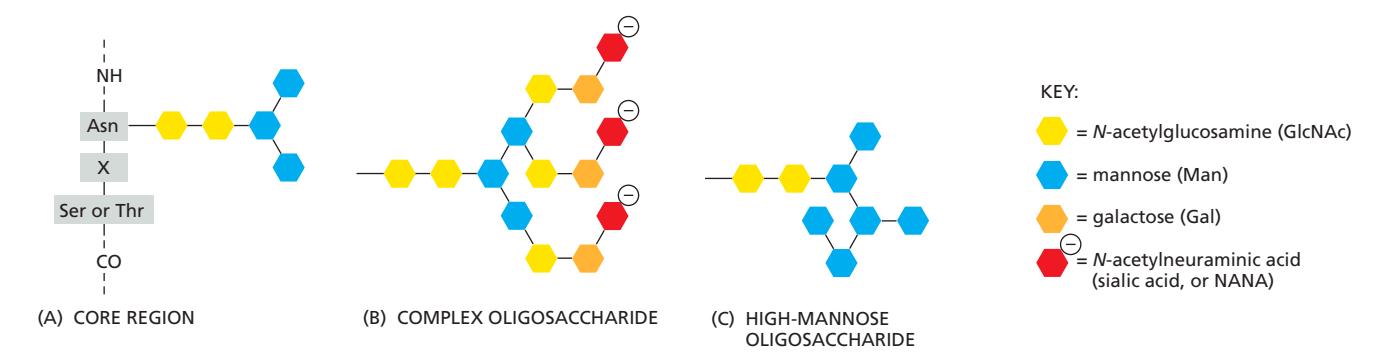
포유류 glycoprotein에 부착되는 N-linked oligosaccharide의 두 가지 broad class:
1. Complex Oligosaccharides
원래 ER에서 추가된 N-linked oligosaccharide가 trimming되고 추가 당이 추가될 때 생성된다.
구조:
- Core region: 일반적으로 2개의 N-acetylglucosamine과 3개의 mannose 이건 공통.
- Terminal region: 특정 trisaccharide unit (N-acetylglucosamine–galactose–sialic acid)의 가변적인 수의 복사본
- 종종 terminal region이 truncated되어 GlcNAc와 galactose만 또는 GlcNAc만 포함
- Fucose가 추가될 수 있음 (일반적으로 asparagine에 부착된 core GlcNAc에)
Complex oligosaccharide는 이질적일 수 있다:
- 3개의 terminal branch를 가진 complex oligosaccharide가 표시되어 있음
- 2개와 4개의 branch도 glycoprotein과 그것을 만드는 세포에 따라 일반적임
2. High-Mannose Oligosaccharides
Trimming되지만 Golgi apparatus에서 새로운 당이 추가되지 않는다.
- Core region까지 완전히 trimming되지 않음
- 추가 mannose 포함
Hybrid oligosaccharide도 존재한다 (하나의 mannose branch와 하나의 GlcNAc 및 Gal branch).
Oligosaccharide 유형 결정 요인(중요)
주어진 oligosaccharide가 high-mannose로 남아 있는지 또는 처리되는지는 주로 단백질에서의 위치에 달려 있다:
- Accessible oligosaccharide: Golgi apparatus의 processing 효소에 접근 가능하면 complex 형태로 전환될 가능성이 높음
- Inaccessible oligosaccharide: 단백질의 접힘 구조나 특정 folding domain 내부에 묻힌 당으로, 효소가 접근할 수 없으면 high-mannose 형태로 남을 가능성이 높음
High mannose form vs Complex form
High mannose form
- Endoplasmic Reticulum + 초기 Golgi 단계까지만 거친 상태
- 특징:
- mannose가 많이 남아 있음
- 추가적인 당(GlcNAc, galactose 등) 거의 없음
Complex form
- Golgi apparatus에서 충분히 가공됨
- 특징:
- mannose 일부 제거됨 (trimming)
- 대신 다양한 당이 붙음
→ GlcNAc, galactose, sialic acid 등 - 가지(branch)가 복잡해짐
차이를 만드는 것
- Asn-X-Ser/Thr 서열 존재
- 구조적 노출 여부
- Golgi 통과 정도 (시간/경로) ← 가장 중요
N-linked vs O-linked
vs O-linked glycosylation 참조
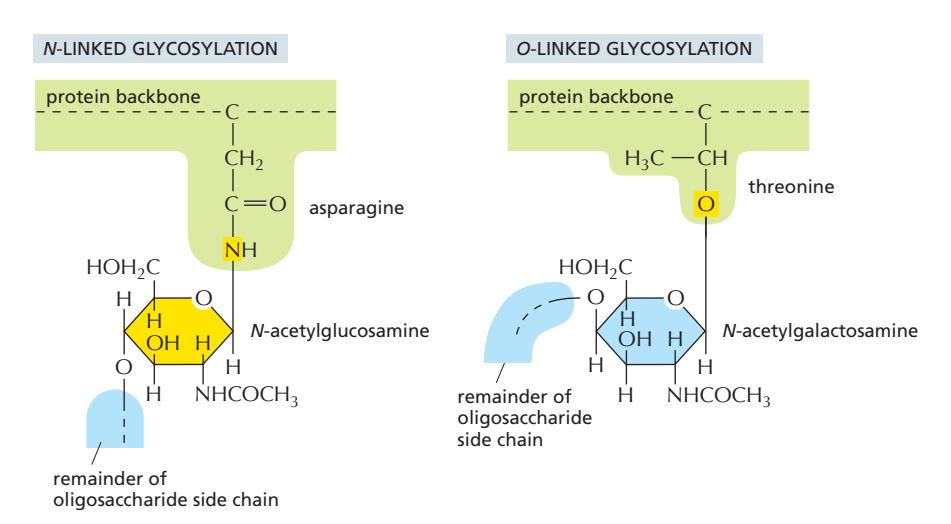 두 가지 방식으로 연결되어 Proteoglycan을 만듦.
N-linked는 Asn(asparagine), O-linked는 Thr(threonine) 혹은 Ser(Serine)
두 가지 방식으로 연결되어 Proteoglycan을 만듦.
N-linked는 Asn(asparagine), O-linked는 Thr(threonine) 혹은 Ser(Serine)
Glycosylation의 목적
protein folding promotion
- Folding이 이루어지고 있는 중간체의 용해도를 늘려 응집을 방지하는 역할
- N-연결된 올리고당의 순차적 변형은 단백질 폴딩의 진행 정도를 나타냄 (glyco-code)
proteolytic enzyme에 의한 digestion 방지
pathogen으로부터 보호, 세포-세포 recognition
세포 신호 전달의 조절 기능
glycosylation에 따라 신호 전달 경로가 달라진다.
관련 주제
- Golgi apparatus의 기능적 구획화
- Golgi apparatus
- N-linked glycosylation
- Quality control of ER protein folding
Footnotes
-
2022 중간 28번 — Golgi에서 N-linked oligosaccharide의 cis→medial→trans 순차적 처리(mannose 제거, sugar 추가)가 정답 근거로 활용됨. ↩