Chapter 12-1: Intracellular Organization and Protein Sorting 정리본
3주차 강의노트 기반 | 출처: 20260320 Intracellular Organization and Protein Sorting.pdf
Chapter 12 구성
- THE COMPARTMENTALIZATION OF CELLS
- THE ENDOPLASMIC RETICULUM
- PEROXISOMES
- THE TRANSPORT OF PROTEINS INTO MITOCHONDRIA AND CHLOROPLASTS
- THE TRANSPORT OF MOLECULES BETWEEN THE NUCLEUS AND THE CYTOSOL
PART 1: THE COMPARTMENTALIZATION OF CELLS
1. 세포(Cell)란 무엇인가 — 역사적 배경
- 세포 = 생명체를 이루는 가장 기본적인 구조적·기능적 단위
초기 인식: protoplasm 개념 (1940~50년대)
- 세포를 **균질한 덩어리(protoplasm)**로 인식: 핵(nucleus)과 나머지(cytoplasm)로만 구분
- 세포 내부 구조물은 살아있는 물질이 응고된 인공산물이라고 여겼다.
전자현미경의 등장 → 세포는 구조화된 공간
- 전자현미경(EM) 등장 → 내부 구조가 보이기 시작
- ribosome, ER, Golgi가 처음 관찰됨
- 결론: “세포는 그냥 액체가 아니라, 구조화된 공간이다”
2. 세포 안에 ‘구획’이 있다는 발견
Discovery of Cell and Organelle 참조
알베르 클로드(Albert Claude)와 세포 분획법
- 알베르 클로드: 세포 분획법(원심분리)을 개발하고 전자현미경으로 세포소기관을 최초로 관찰
- 세포 분획법 (Cell Fractionation)
- 세포를 부드럽게 파쇄 (homogenization)
- **원심분리(differential centrifugation)**를 이용해 속도를 달리하며 순차적으로 분리
- Low speed → 핵, cytoskeleton
- Medium speed → 미토콘드리아
- High speed → microsomes (ER fragments), small vesicles
- Very high speed → 리보솜, 거대 분자
- Sucrose gradient centrifugation으로 더 정밀하게 분리
→ 세포를 ‘덩어리’가 아니라 기능적으로 구분된 소기관(organelle)들의 집합으로 이해하게 됨
Electron Micrograph of Liver Cell (Hepatocyte)
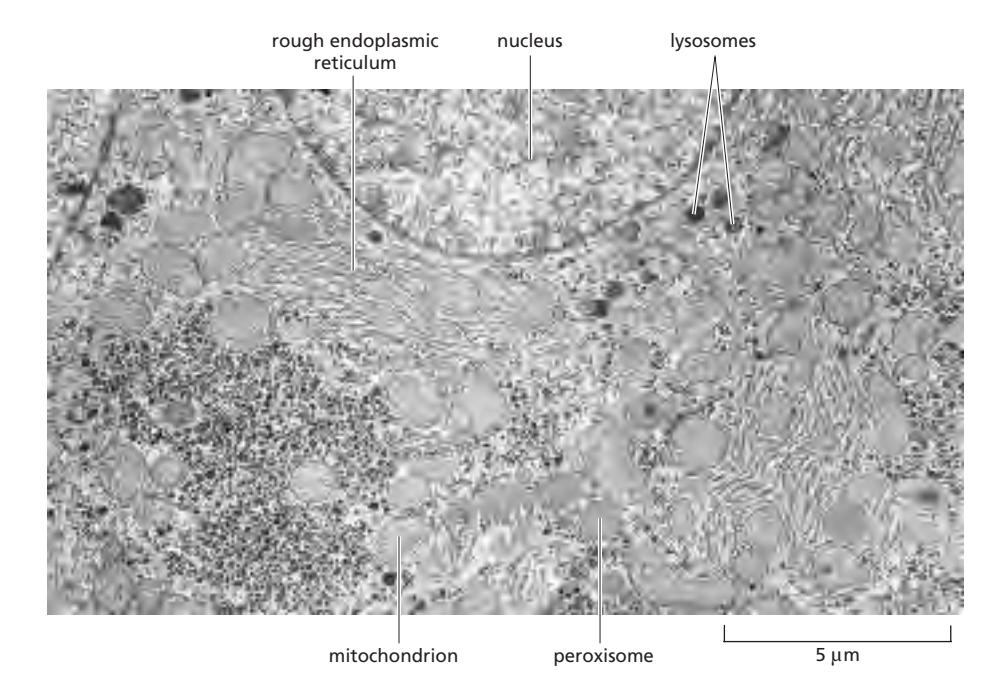 Figure 12-2: An electron micrograph of part of a liver cell seen in cross section
Figure 12-2: An electron micrograph of part of a liver cell seen in cross section
The membrane-enclosed organelles are packed tightly in the cytoplasm, and, in terms of area and mass, the plasma membrane is only a minor membrane in most eukaryotic cells.
- 간세포(hepatocyte) 단면 EM에서 rough ER, nucleus, lysosomes, mitochondrion, peroxisome 등 모두 관찰
- 세포막(plasma membrane)은 실제로 전체 막의 아주 작은 부분만 차지 (hepatocyte 기준 2%)
3. Prokaryote vs Eukaryote
| 원핵생물 (Prokaryotes) | 진핵생물 (Eukaryotes) | |
|---|---|---|
| 어원 | pro (이전) + karyon (핵, 알맹이) → 핵 이전 (before nuclei) | eu (좋은, 참된) + karyon (핵) → 참된 핵 (true nuclei) |
| 핵 | 없음 (nucleoid) | 있음 (nuclear envelope) |
| 세포 소기관 | 막으로 둘러싸인 소기관 없음 | 막으로 둘러싸인 소기관 보유 |
| 세포구조 | 단순 | 복잡 |
| DNA 위치 | 세포질 | 핵 안 |
| 해당 생물 | 박테리아, 고세균 | 동물, 식물, 곰팡이, 원생생물 |
| 진화 | — | 약 27억 년 전 원핵생물로부터 진화 → 세포 내 공생설 |
4. 막(Membrane)의 생화학적 역할
Biochemical Roles of Membranes 참조
4가지 핵심 역할
1. Membranes as platforms for reactions (반응의 플랫폼)
- Membrane-bound enzymes이 막에 부착되어 반응 수행
- ATP 생성에 필수: H⁺ gradient → ATP synthesis (막이 없으면 불가)
2. 세포 내 구획화 (Compartmentalization)
- 막 면적을 늘려 생화학 반응 공간 증가 → 반응 효율 증가
- 기능적으로 구분된 공간(functionally distinct spaces) 형성 → 최적화된 생화학 환경 유지
3. Molecular concentration & regulation
- 국소 농축(local enrichment): 효소, 반응물, 이온을 특정 공간에 집중
- 반응 효율 향상 + 신호 조절 가능
4. Selective transport & protein import
- Lipid bilayer: 대부분의 hydrophilic molecules에 불투과성 (선택적 장벽)
- Membrane transport proteins을 통한 물질 이동 (metabolite 교환)
- Protein targeting/import systems 필요 → organelle 특이성 유지
5. 진핵세포의 막 구획 (Membrane-Enclosed Organelles)
000_ Basic Set of Membrane‐enclosed Organelles in Eukaryotic Cells_MOC 참조
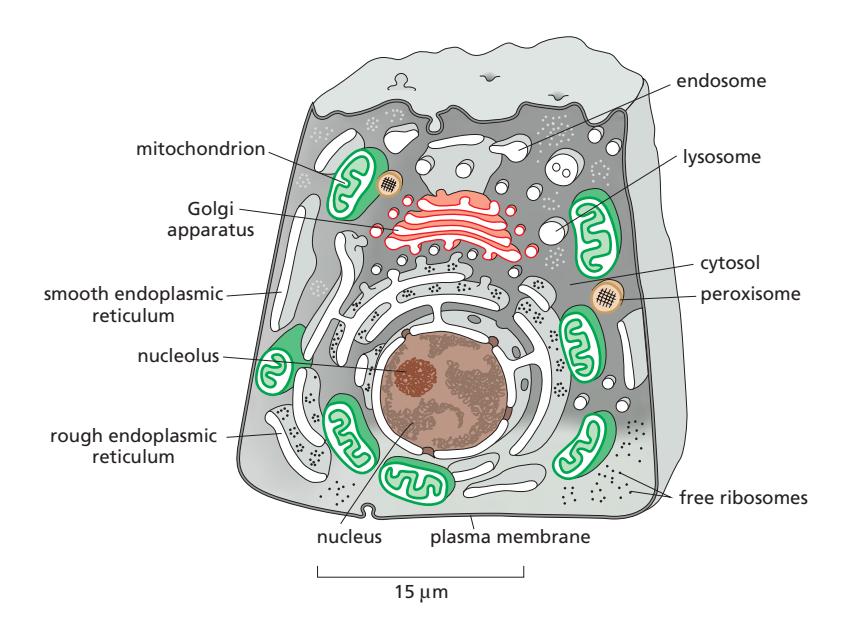 Figure 12-1: The major intracellular compartments of an animal cell
Figure 12-1: The major intracellular compartments of an animal cell
기본 세포 소기관
| 소기관 | 주요 기능 |
|---|---|
| 핵 (Nucleus) | contains genome; site of DNA and RNA synthesis |
| Cytoplasm / Cytosol | Cytosol ~50% of cell volume; protein synthesis and degradation; small molecule degradation; synthesis of building blocks |
| 소포체 (ER) | Rough ER: ribosome-bound; synthesizes membrane & secretory proteins / Smooth ER: lipid synthesis, Ca²⁺ storage |
| Golgi apparatus | Modifies, sorts, and dispatches proteins and lipids from ER |
| 미토콘드리아 & chloroplasts | ATP synthesis; chloroplast also store food/pigments |
| 리소좀 | Digestion of defunct intracellular organelles, macromolecules, and particles |
| 엔도솜 | Sorting compartments for endocytosed material |
| 퍼옥시솜 | oxidative reactions |
The cytosol, rough ER, smooth ER, Golgi apparatus, nucleus, mitochondrion, endosome, lysosome, and peroxisome are distinct compartments isolated by at least one selectively permeable membrane. By contrast, the nucleolus is not enclosed by a membrane → biomolecular condensate.
Table 12-1: Hepatocyte의 세포 구획 부피 비율
| Intracellular compartment | Percentage of total cell volume |
|---|---|
| Cytosol | 54% |
| Mitochondria | 22% |
| Rough ER cisternae | 9% |
| Smooth ER cisternae | 5% |
| Nucleus | 6% |
| Golgi cisternae | 1% |
| Peroxisomes | 1% |
| Lysosomes | 1% |
| Endosomes | 1% |
Table 12-2: 세포 내 막의 비율 (Hepatocyte vs Pancreatic exocrine cell)
| Membrane type | Liver hepatocyte | Pancreatic exocrine cell |
|---|---|---|
| Plasma membrane | 2% | 5% |
| Rough ER membrane | 35% | 60% |
| Smooth ER membrane | 16% | <1% |
| Golgi apparatus membrane | 7% | 10% |
| Mitochondria — Outer membrane | 7% | 4% |
| Mitochondria — Inner membrane | 32% | 17% |
| Nucleus — Inner membrane | 0.2% | 0.7% |
- Plasma membrane은 전체 막의 2%에 불과 → 세포막은 “minor membrane”
- Pancreatic exocrine cell: 단백질 분비 기능 강함 → Rough ER 비율 60%로 높음
6. 세포 내 막의 종류 — 단일막 vs 이중막
단일막 (Lipid bilayer, 單一膜)
- 인지질 이중층 (phospholipid)으로 구성
- 친수성 머리(hydrophilic head) → 바깥 / 소수성 꼬리(hydrophobic tail) → 내부
- 세포막과 세포소기관 막의 선택적 투과 장벽 형성
- 해당 구획: ER, Golgi, lysosome, 세포막(plasma membrane)
이중막 (Double membrane, 二重膜)
- 두 개의 lipid bilayer (bilayer × 2)
- 외막(outer membrane) / 내막(inner membrane) 분리 구조
- 막 사이 공간: intermembrane space
- 각 막은 서로 다른 단백질과 기능 보유
- 대개 **내부 공생설(endosymbiotic origin)**과 관련
- 해당 구획: 핵막(nuclear envelope), 미토콘드리아(mitochondria), 엽록체(chloroplasts)
7. 세포 내부 막의 기원 — Origin of Internal Membranes
Origin of Internal Membranes 참조
Ancestral Cells (prokaryote-like)
- Like bacteria/archaea: only plasma membrane → 내부 막 없음
- 모든 기능이 세포막 하나에서 수행 (ion pumping, ATP synthesis, protein secretion, lipid synthesis)
- 세포 크기 증가 → 부피↑, 표면적 대 부피 비(surface area-to-volume ratio) 감소 → plasma membrane만으로는 막-의존 기능 감당 불가
내부 막의 형성 — 2가지 경로
1. 세포막의 함입 (Invagination of plasma membrane)
- 세포막이 안쪽으로 접힘
- ER, 핵막 형성
- ER/Golgi의 lumen은 세포 외부와 위상적으로 동일(topologically equivalent to cell exterior)
- 기능 공간 분리 + 막 표면적 증가
2. 세포 내 공생 (Endosymbiosis) (~16억 년 전)
- **혐기성 세포(anaerobic archaeon)**이 **호기성 세균(aerobic bacterium)**을 흡수하는 사건 발생
- → 최초의 진핵세포(eukaryotic cell) 탄생
- 흡수된 세균 → 미토콘드리아 형성 → 고효율 ATP 생산 가능
진화 3단계:
- Enclosure: archaeal membrane이 bacterial symbiont를 감쌈 (Invagination)
- Escape: endosymbiont genome이 cytosol로 탈출
- Elaboration: 내부 구획 정교화 → endomembrane system 형성 → 기능 분화
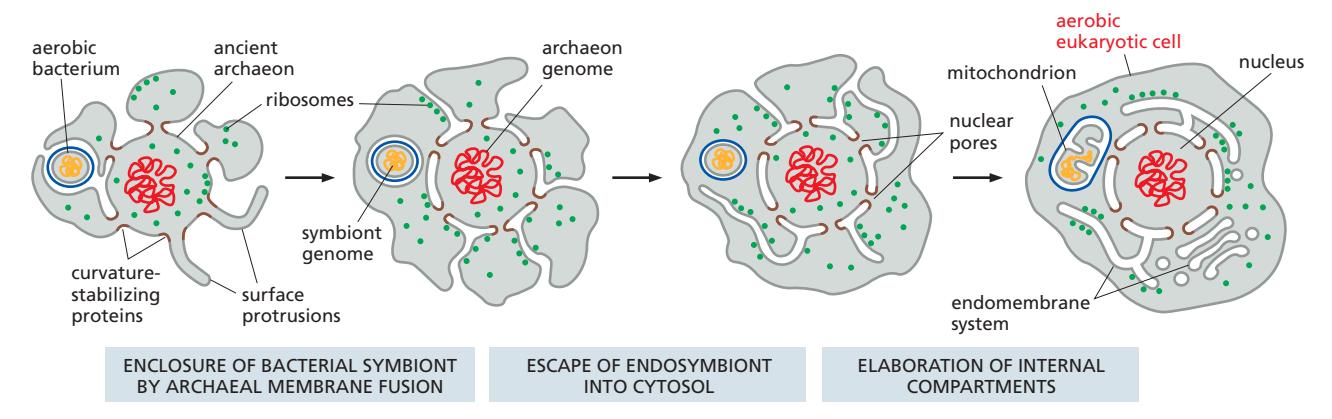 Figure 12-3: Evolutionary origins of the major internal membrane systems of a eukaryotic cell
Figure 12-3: Evolutionary origins of the major internal membrane systems of a eukaryotic cell
8. Topological Equivalence (위상적 동등성)
Topological Relationships of Organelles 참조
정의: 두 구획이 막을 가로지르지 않고 분자를 이동시킬 수 있다면 위상학적으로 동일하다.
“막을 통과하지 않고 이동할 수 있는 공간은 같은 위상(topology)에 있다”
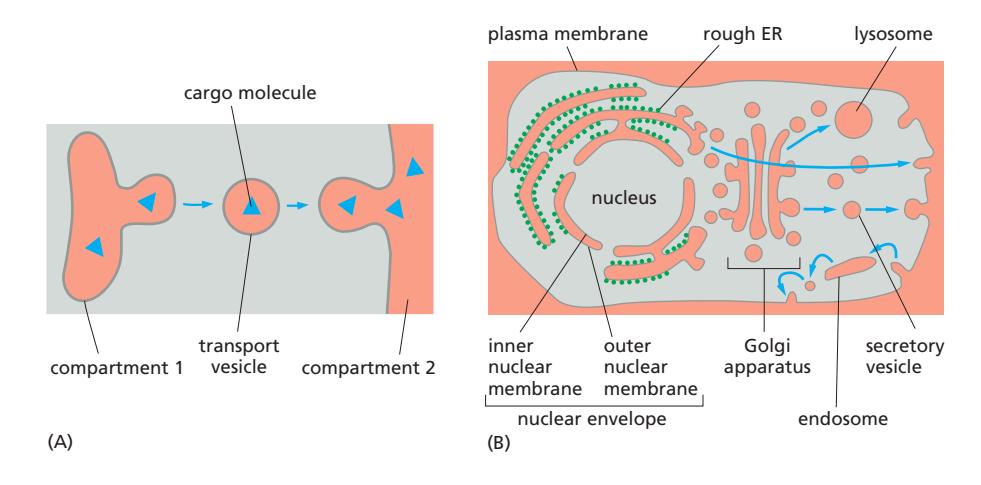 Figure 12-4: Topologically equivalent compartments in the secretory and endocytic pathways
Figure 12-4: Topologically equivalent compartments in the secretory and endocytic pathways
Secretory & Endocytic Pathways
Secretory pathway (분비 경로)
- ER → Golgi → plasma membrane or lysosome
- 막을 통과하지 않음 → Vesicular transport (budding & fusion)
Endocytic pathway (내이입 경로)
- Plasma membrane → endosomes → lysosomes or back to Golgi/ER
예외: Mitochondria & plastids
- Vesicular traffic에 참여하지 않음 → 위상학적으로 독립
Vesicle Budding and Fusion
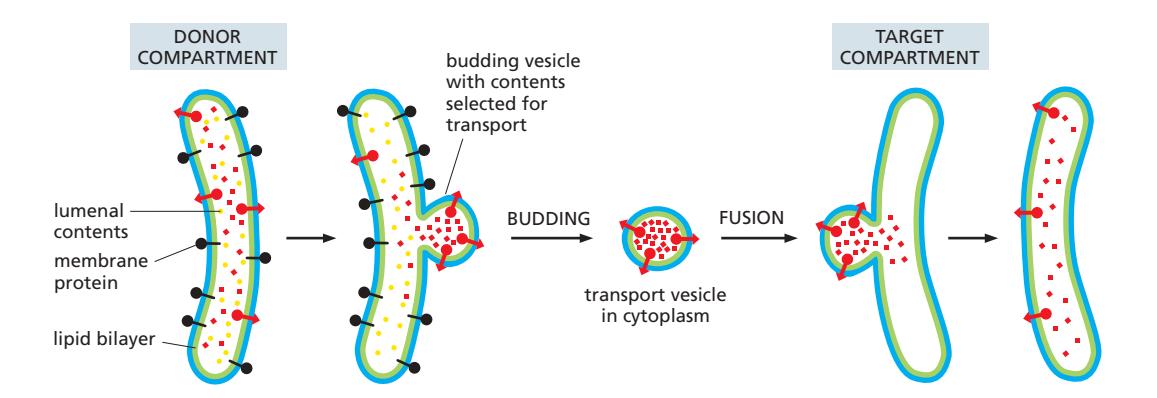 Figure 12-11: Vesicle budding and fusion during vesicular transport
Figure 12-11: Vesicle budding and fusion during vesicular transport
- Transport vesicle이 donor compartment에서 출아(bud)하여 target compartment에 융합
- 핵심: 막 단백질의 방향(orientation)이 항상 보존됨
- Cytosol-facing domain → 항상 cytosol
- Lumen-facing domain → 항상 lumen
- Vesicle transport = 내용물 이동 + 방향성 유지
Engulfment (삼킴)
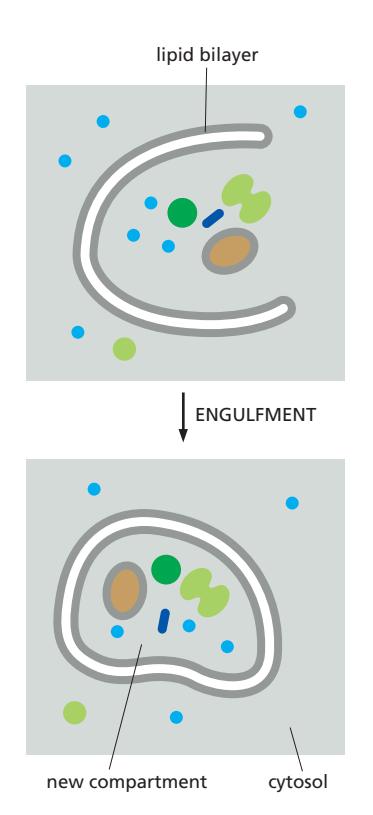 Figure 12-12: Formation of a new compartment by engulfment
Figure 12-12: Formation of a new compartment by engulfment
- 이중막이 세포질 내용물을 감쌈 → 새로운 compartment 형성
- 예: autophagy(세포 자가소화), nuclear envelope 재형성
9. 단백질 수송 메커니즘 4가지
000_Protein Traffic_MOC 참조
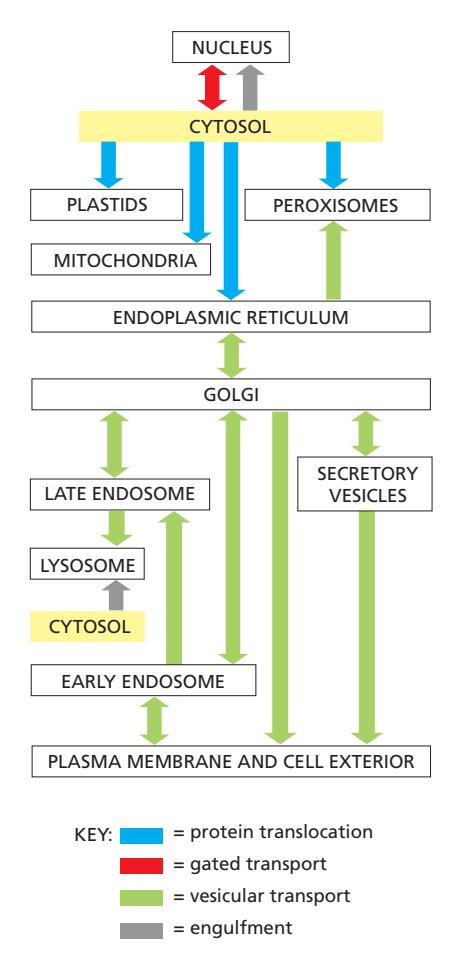 Figure 12-10: A simplified “road map” of protein traffic within a eukaryotic cell
Figure 12-10: A simplified “road map” of protein traffic within a eukaryotic cell
단백질은 cytosolic ribosome에서 합성을 시작하여 최종 목적지로 이동
| 메커니즘 | 색상 | 설명 |
|---|---|---|
| Protein Translocation | 파란색 | Transmembrane protein translocators가 cytosol에서 위상적으로 구분된 공간으로 직접 수송 |
| Gated Transport | 빨간색 | Protein과 RNA가 핵공 복합체(nuclear pore complex)를 통해 cytosol ↔ nucleus 이동 |
| Vesicular Transport | 초록색 | 막으로 둘러싸인 수송 중간체(vesicle)가 위상적으로 동일한 compartment 사이에서 단백질 이동 |
| Engulfment | 회색 | 이중막이 세포질 일부(소기관 포함)를 감쌈 |
10. Sorting Signals — 단백질 주소 “addresses”
Signal sequences = 세포 내 주소 “addresses”: 단백질이 어디로 갈지 결정, sorting receptor가 인식
- 각 단백질의 아미노산 서열(amino acid sequence) 안에 인코딩
- Signal sequence의 기능은 아미노산 조성, 전하 분포, 소수성에 의해 결정
- 단백질 목적지별 signal sequence 예:
| 목적지 | Signal sequence 특징 |
|---|---|
| Import into nucleus | 양전하(Lys, Arg) 풍부 |
| Export from nucleus | Met-Glu-Glu-Leu…등 소수성 포함 |
| Import into mitochondria | N-말단 양전하 + 소수성 반복 패턴 |
| Import into ER | N-말단 소수성 서열 (Leu, Val, Ile, Phe 등) |
| Import into peroxisome | C-말단 Ser-Lys-Leu (-SKL) |
| Return to ER | C-말단 Lys-Asp-Glu-Leu (-KDEL) |
11. Biomolecular Condensates (생체분자응집체)
개념: 막 없이 형성되는 기능적 구획
- Biomolecular condensates: 막 없이 형성되는 기능적 구획
- 특정 분자들이 모여 농축된 영역 형성
- Phase separation(상분리) 기반: 네트워크가 형성되어 액체처럼 분리
Multivalent Interaction (다가 상호작용)
- 하나의 분자가 여러 결합 부위 보유
- 동시에 여러 분자와 결합 → 네트워크 형성 → 액체처럼 분리 (phase separation)
- Multi (여러 개) + valent (결합가) = 하나의 분자가 여러 개의 결합부위를 가지고 동시에 여러 분자와 결합하는 상호작용
Scaffold & Client 구조
- Scaffold macromolecules (단백질, RNA): condensate의 뼈대 형성
- Client molecules: scaffold에 선택적으로 모집됨 → 특정 분자만 선택적으로 모임
- 막 없이도 compartmentalization 가능 / 반응속도 조절 가능
- 동적으로 형성·해체 가능
Compartment = 반드시 membrane이 필요한 것은 아님
Table 12-3: Eukaryotic Biomolecular Condensates 예시
| Biomolecular condensate | Location | Function |
|---|---|---|
| Nucleolus | Nucleus | rRNA transcription and ribosome assembly |
| Stress granules | Cytosol | Temporary storage of translation-related components |
| P-granules | Cytosol | RNA metabolism and inheritance |
| Cajal body | Nucleus | mRNA processing |
| Paraspeckles | Nucleus | Regulation of gene expression |
| PML body | Nucleus | Storage of nuclear factors; regulation of gene expression |
| Postsynaptic density | Dendrite | Organization of macromolecules for neuronal transmission |
Nucleolus — Multilayered Condensate 예시
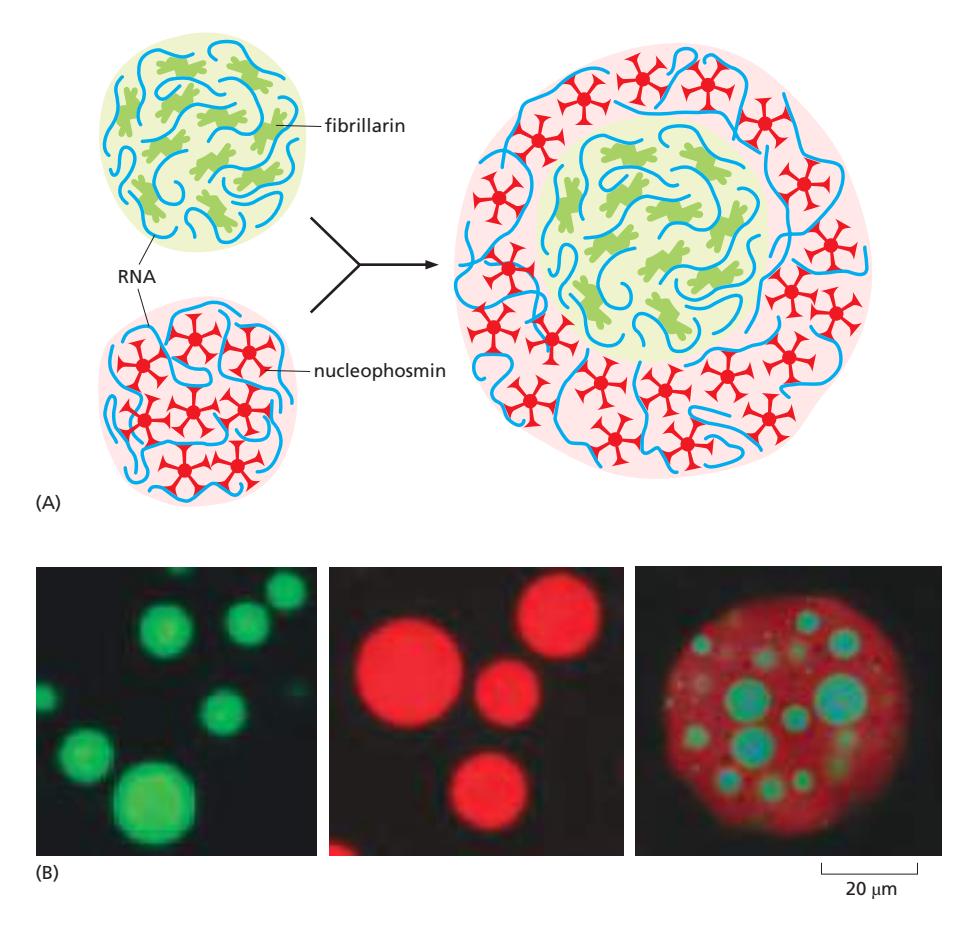
- Nucleolus = 핵 안의 막 없는 biomolecular condensate
- 구성:
- Fibrillarin (fibrillar component) + RNA
- Nucleophosmin (granular component) + RNA
- → Multilayered condensate: 하나의 구조 안에 서로 다른 condensate 공존
- Core (fibrillarin-rich) + outer layer (nucleophosmin-rich)
- 기능: rRNA transcription and ribosome assembly
- 반응을 공간적으로 분리 가능, 서로 다른 기능을 동시에 수행
- 막 없이도 compartmentalization 가능
Condensate의 동적 조절 — Phosphorylation
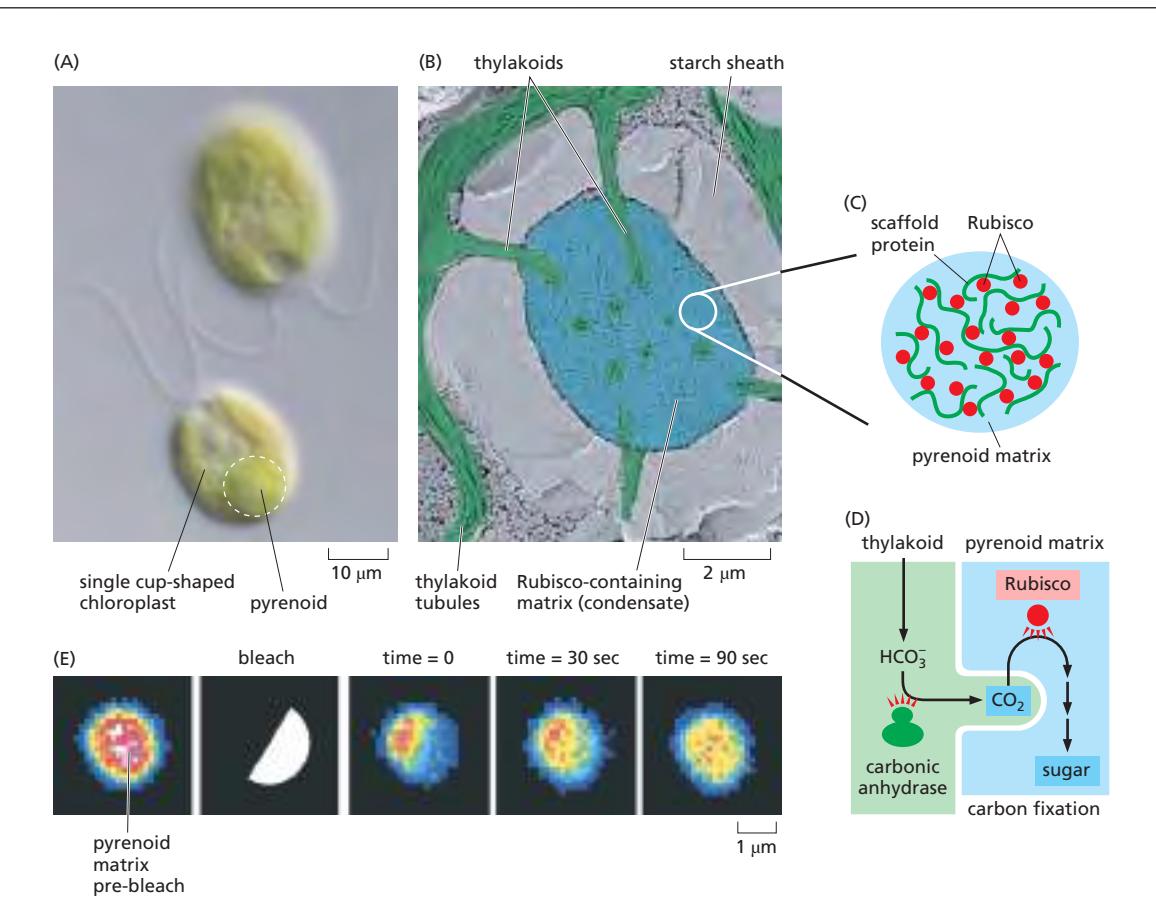 Figure 12-9: Phosphorylation regulates the formation and dissolution of condensates during signaling
Figure 12-9: Phosphorylation regulates the formation and dissolution of condensates during signaling
신호 있을 때 (condensate 형성)
- 신호시작 (Trigger): Ligand가 receptor에 결합 → Receptor 활성화
- Phosphorylation: Receptor의 cytosolic tail에 결합 → Docking site 생성
- Condensate formation: Multivalent protein들이 동시에 결합 → 네트워크(Signal Hub) 형성
- Signal amplification: 효소와 기질이 한곳에 집중 → 반응속도 증가 → 신호 증폭
신호 없을 때 (condensate 해체) 5. Disassembly: Dephosphorylation 발생 → 결합 부위 사라짐 → condensate 붕괴 → 신호 종료
12. Summary — PART 1
- Cell Organelles: 진핵세포는 다양한 막 소기관을 가짐 / 각 소기관은 특정 단백질 조합 → 고유 기능 수행
- Biomolecular condensates: 막 없이도 compartment 형성 가능 / Phase separation 기반 / 필요에 따라 동적으로 형성·해체
- Protein Targeting to Organelles: 단백질은 signal sequence를 가짐 / Sorting receptor가 인식 / 아미노산 조성 + 전하 + 소수성 → 목적지 결정
- Organelle Distribution During Cell Division: 세포 분열 시 소기관은 분배 또는 재구성 / Biomolecular condensate는 self-assemble 방식으로 재형성
PART 2: THE ENDOPLASMIC RETICULUM
13. ER 구조 — 광범위한 네트워크
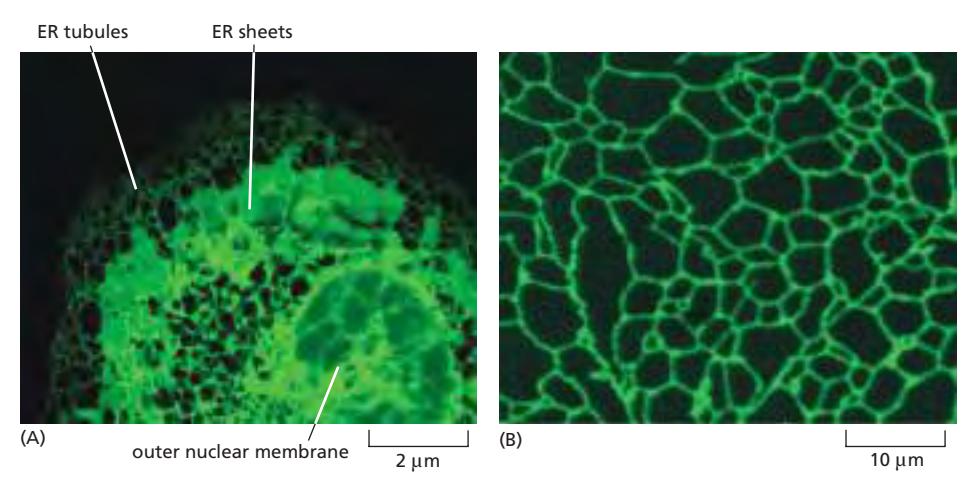 Figure 12-14: Fluorescence micrographs of the endoplasmic reticulum (animal & plant cell)
Figure 12-14: Fluorescence micrographs of the endoplasmic reticulum (animal & plant cell)
- ER = tubule(관) + sheet(판) 구조
- 세포 전체에 퍼진 연속적인 네트워크 → ER lumen은 모두 연결되어 있음
- Outer nuclear membrane = ER의 일부 (outer nuclear membrane이 rough ER과 연속)
- ER lumen = nuclear envelope 내부 공간 → 같은 위상적 공간(topological space)
14. ER의 구조적·기능적 다양성 — Rough vs Smooth ER
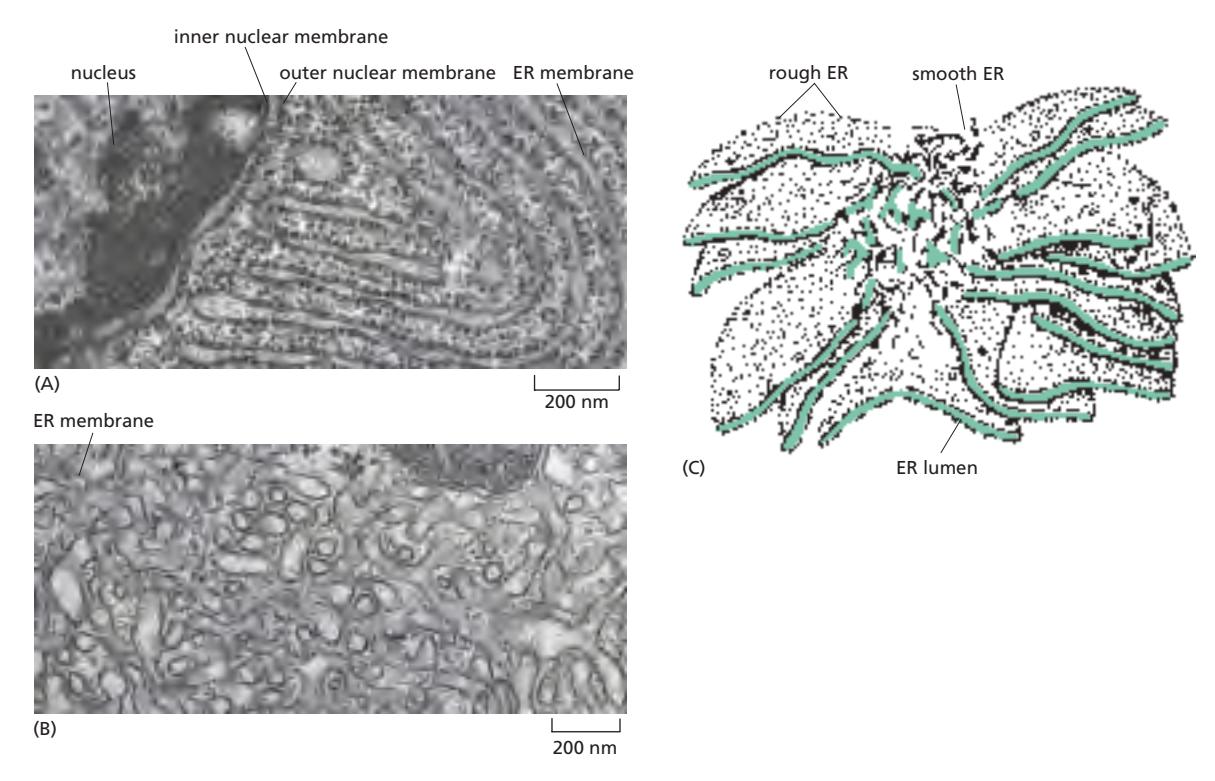 Figure 12-15: The rough and smooth ER (Pancreatic exocrine cell vs Leydig cell)
Figure 12-15: The rough and smooth ER (Pancreatic exocrine cell vs Leydig cell)
| Rough ER | Smooth ER | |
|---|---|---|
| 구조 | Sheet (flat membrane) | Tubule (curved membrane) |
| 리보솜 | 있음 | 없음 |
| 기능 | 단백질 합성 (membrane & secretory proteins) | 지질 합성, Ca²⁺ 저장 |
| 위치 | Nucleus 근처 | 세포 전체 |
| 특징 | Flat membrane → ribosome 결합에 유리 → protein synthesis | Curved tubule → surface 확장 → lipid metabolism |
| 대표 세포 | Pancreatic exocrine cell (단백질 분비 세포, Rough ER 60%) | Steroid-secreting Leydig cell (testosterone 분비) |
15. ER Contact Sites (막 접촉 부위)
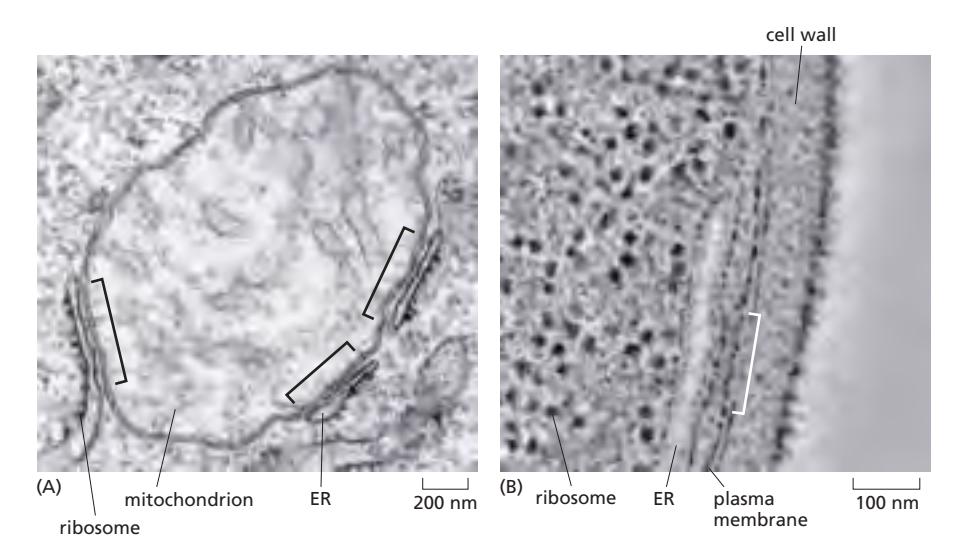 Figure 12-16: The ER makes close contacts with the mitochondria and plasma membrane
Figure 12-16: The ER makes close contacts with the mitochondria and plasma membrane
- ER이 mitochondria 및 plasma membrane과 밀접하게 접촉 (~10–30 nm 거리 유지)
- Membrane contact site (MCS): 막은 붙어 있지만 membrane fusion은 일어나지 않고 단백질에 의해 연결됨
MAM (Mitochondria-Associated Membrane)
- ER–Mitochondria 접촉 부위
- 지질 합성/이동 + apoptosis 조절
ER–Plasma membrane 접촉 부위
- Ca²⁺ influx 조절 + signaling platform 역할
16. Microsome 분리 실험 — Rough vs Smooth 구분
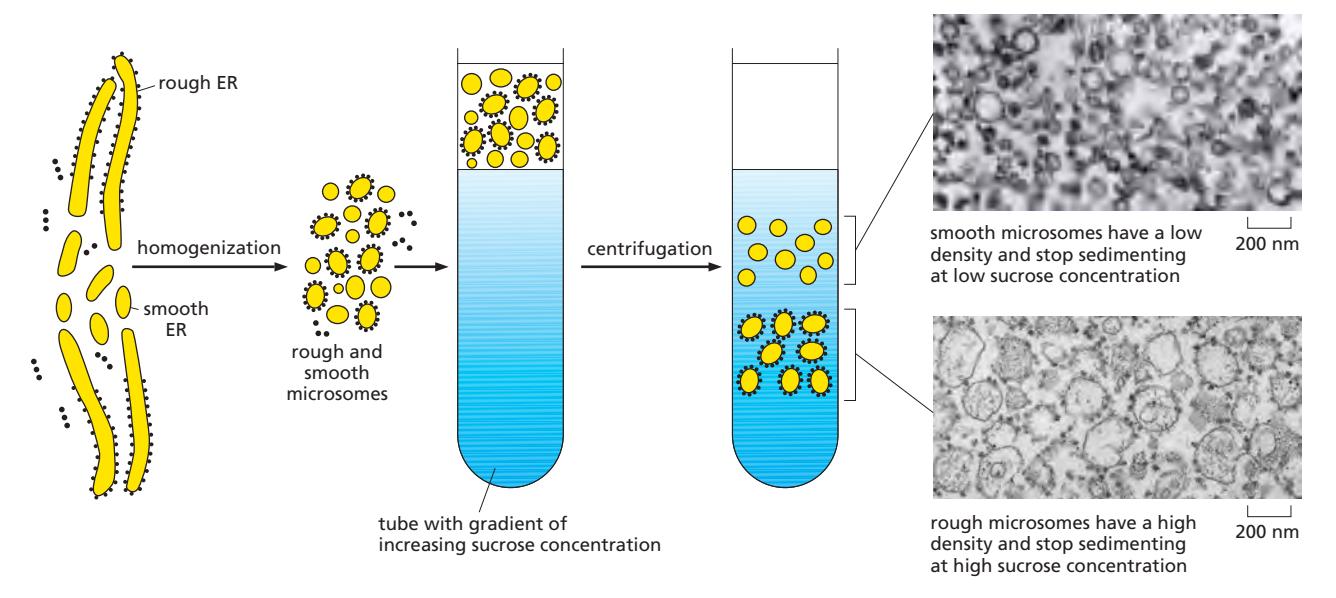 Figure 12-17: The isolation of purified rough and smooth microsomes from the ER
Figure 12-17: The isolation of purified rough and smooth microsomes from the ER
- Homogenization으로 ER membrane이 잘려서 vesicle 형태로 재조립 → Microsome 형성
- Sucrose gradient centrifugation: 밀도에 따라 분리
| Rough microsomes | Smooth microsomes | |
|---|---|---|
| 밀도 | 높음 (ribosomes 때문) | 낮음 (ribosomes 없음) |
| 원심분리 위치 | High sucrose concentration에서 정지 | Low sucrose concentration에서 정지 |
| EM 관찰 | 리보솜으로 뒤덮인 vesicle (rough ER 유래) | 리보솜 없는 vesicle (smooth ER, Golgi cisternae 등 유래) |
17. Signal Hypothesis — ER로의 단백질 타겟팅 발견
Experimental basis for the signal hypothesis 참조
Protein targeting = sequence에 의해 결정된다
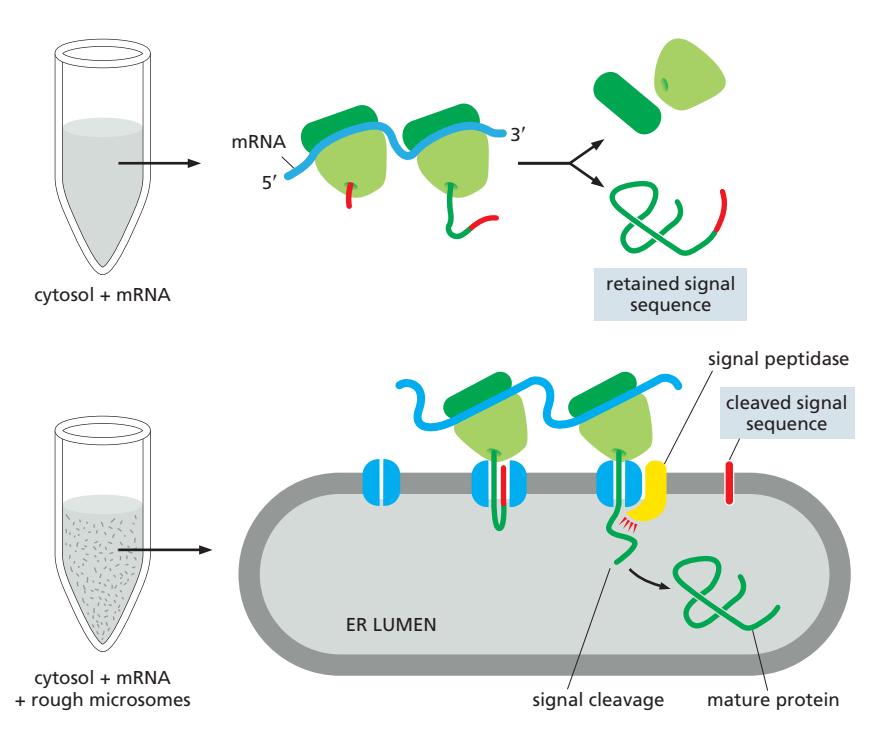 Figure 12-18: Experimental basis for the signal hypothesis
Figure 12-18: Experimental basis for the signal hypothesis
실험 근거 (Cell-free translation 실험)
Without rough ER microsomes
- Cytosol의 ribosome이 mRNA를 정상 분비 단백질보다 약간 더 큰 단백질로 번역함
- (signal sequence가 붙어 있어서 더 큼)
With rough ER microsomes
- 정확한 크기의 단백질이 생산되었고
- Microsome 내부에 위치함
- N-terminus의 짧은 signal sequence가 signal peptidase에 의해 절단됨
결론: Signal sequences direct proteins to the ER
18. SRP (Signal-Recognition Particle)
SRP 참조
SRP 구조
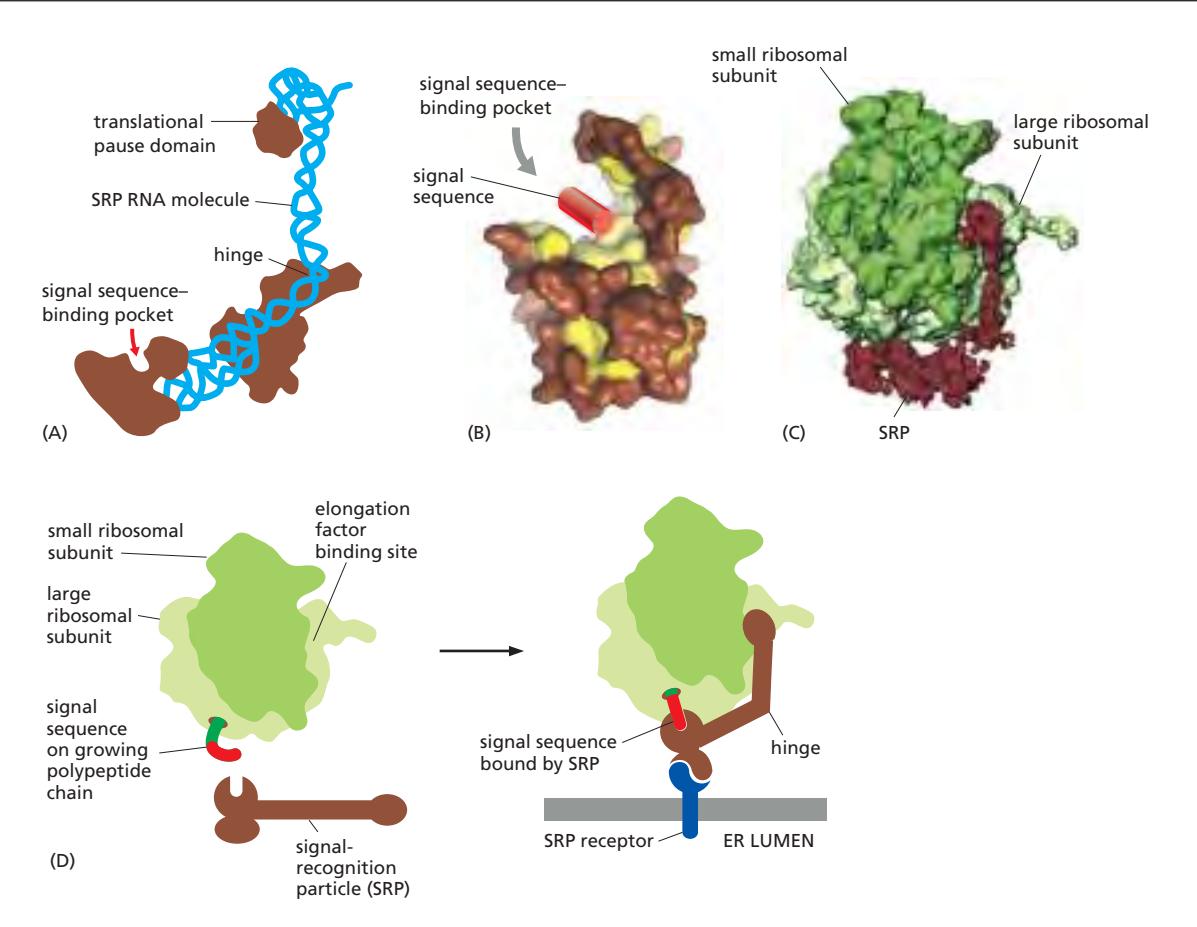 Figure 12-19: The signal-recognition particle (SRP)
Figure 12-19: The signal-recognition particle (SRP)
- Rodlike ribonucleoprotein complex
- 6 protein subunits (갈색) + 1 RNA molecule (파란색)
- SRP RNA가 backbone 형성: signal sequence-binding pocket ↔ translational pause domain 연결
- Signal sequence-binding pocket: 소수성 groove에 signal sequence (hydrophobic region)가 결합
SRP의 역할
- Signal sequence가 리보솜에서 나오면 SRP가 인식·결합
- Conformational change → SRP receptor에 대한 결합 부위 노출
- Translation을 느리게(slow) 함 → ER로 이동할 시간 확보
19. Co-translational Translocation — SRP 매개 ER 타겟팅 과정
Co-translational translocation 참조
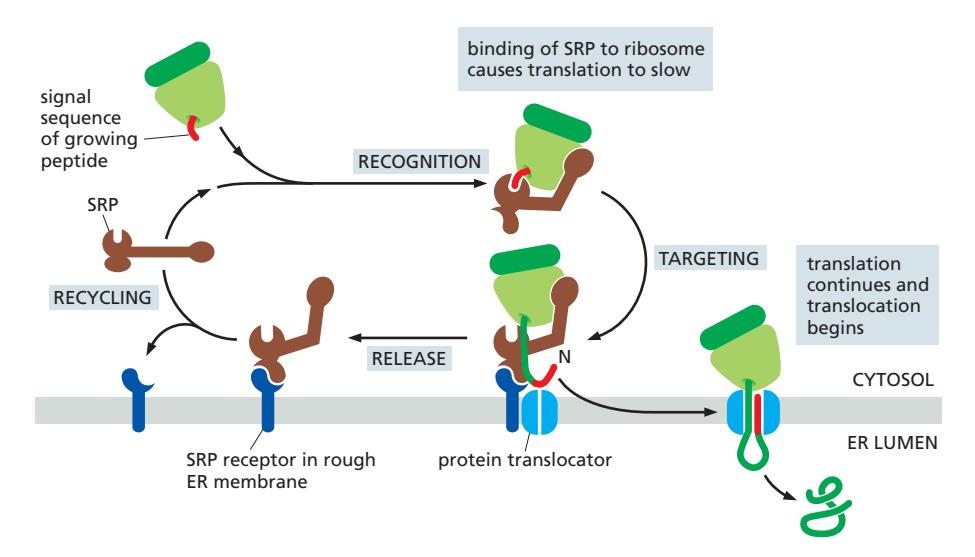 Figure 12-20: How ER signal sequences and SRP direct ribosomes to the ER membrane
Figure 12-20: How ER signal sequences and SRP direct ribosomes to the ER membrane
전체 과정 4단계:
1단계: SRP detects the signal
- 단백질 합성 중 signal sequence (N-terminus) 등장
- SRP는 노출된 ER signal sequence와 ribosome 모두에 결합
- Ribosome + nascent chain + SRP → 복합체 형성
- Translation을 느리게(slow) 함 → ER로 이동할 시간 확보
2단계: SRP finds the docking site
- SRP가 complex를 ER membrane의 SRP receptor로 이동
3단계: Handoff to the translocator
- SRP(SRP receptor와 complex를 이룬)가 ribosome의 결합 부위에서 멀어지고, 이 위치는 ER membrane의 **translocator(Sec61)**가 차지
- SRP는 signal sequence를 방출하고, 이것이 translocator에 삽입되어 polypeptide chain 전달 시작
- Translation 재개 → 새로 합성되는 폴리펩타이드가 ER lumen으로 translocation 시작
4단계: Recycling
- SRP와 SRP receptor는 분리되어 다음 타겟팅 사이클에 재사용
- 두 단백질 모두 GTP-binding domain 보유
- GTP 결합 및 가수분해가 정확한 ER 도킹 이후에 SRP가 signal sequence를 방출
- GTP hydrolysis가 이 과정의 에너지와 방향성(directionality)을 제공
20. Free vs Membrane-bound Ribosome
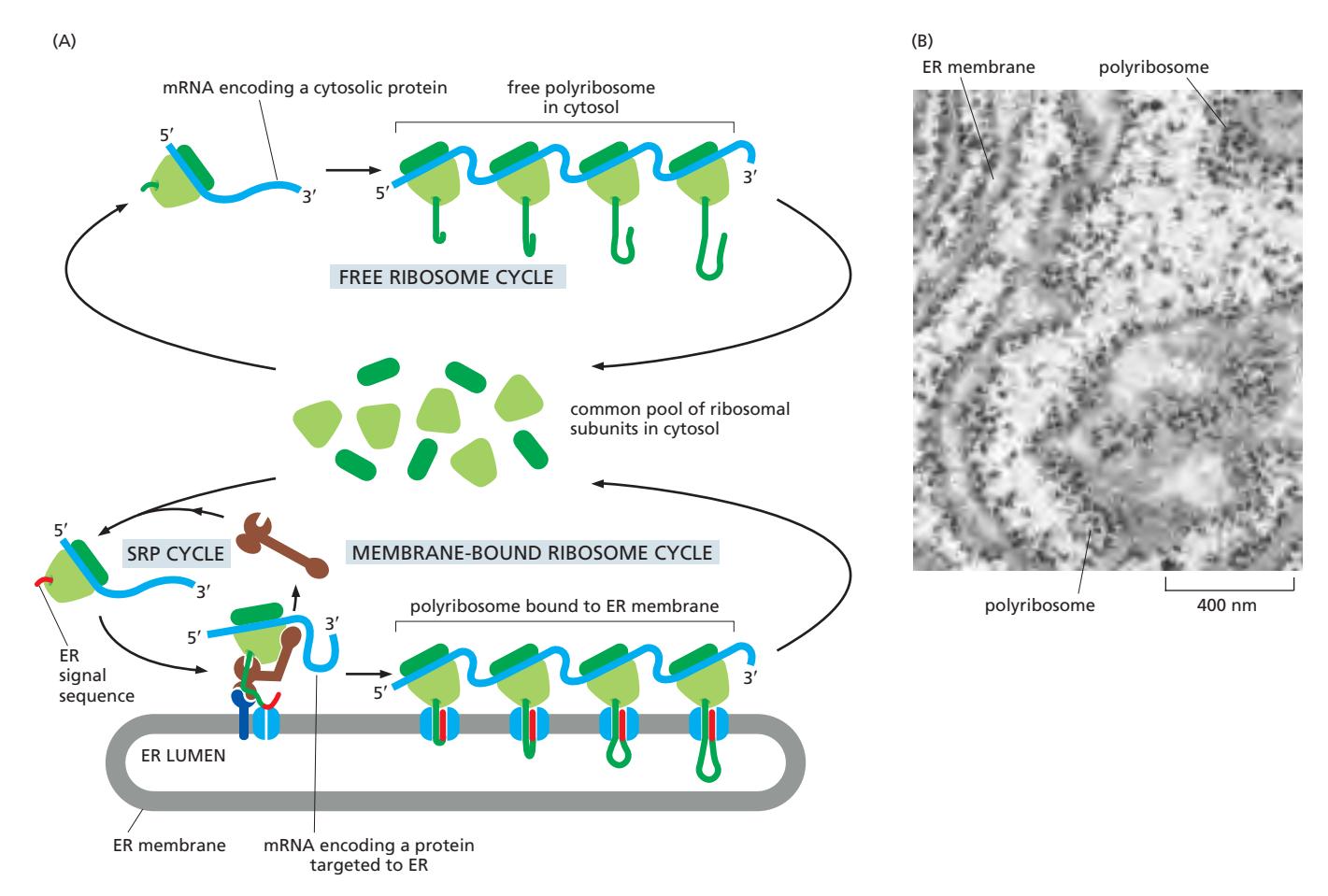 Figure 12-21: Free and membrane-bound polyribosomes
Figure 12-21: Free and membrane-bound polyribosomes
All ribosomes are identical in structure; they can synthesize proteins for either the cytosol or the ER, depending on the signal sequence of the nascent polypeptide.
Free ribosome cycle
- Cytosol에서 번역 시작
- Signal sequence가 없음 → 단백질은 cytosol에 남음
Membrane-bound ribosome cycle
- 번역 중 ER signal sequence가 노출되면 SRP가 인식·결합하여 ER로 이동
- Ribosome이 ER membrane에 부착 → 단백질이 ER lumen으로 들어감
Polyribosome (폴리리보솜)
- 하나의 mRNA에 여러 ribosome이 연달아 연결된 상태로 translocator에 붙은 상태로 번역을 진행
- protein synthesis가 끝나고 ribosome subunits는 분해되어 다시 cytosol의 common pool로 돌아감
21. Sec61/SecY Translocator (전이복합체)
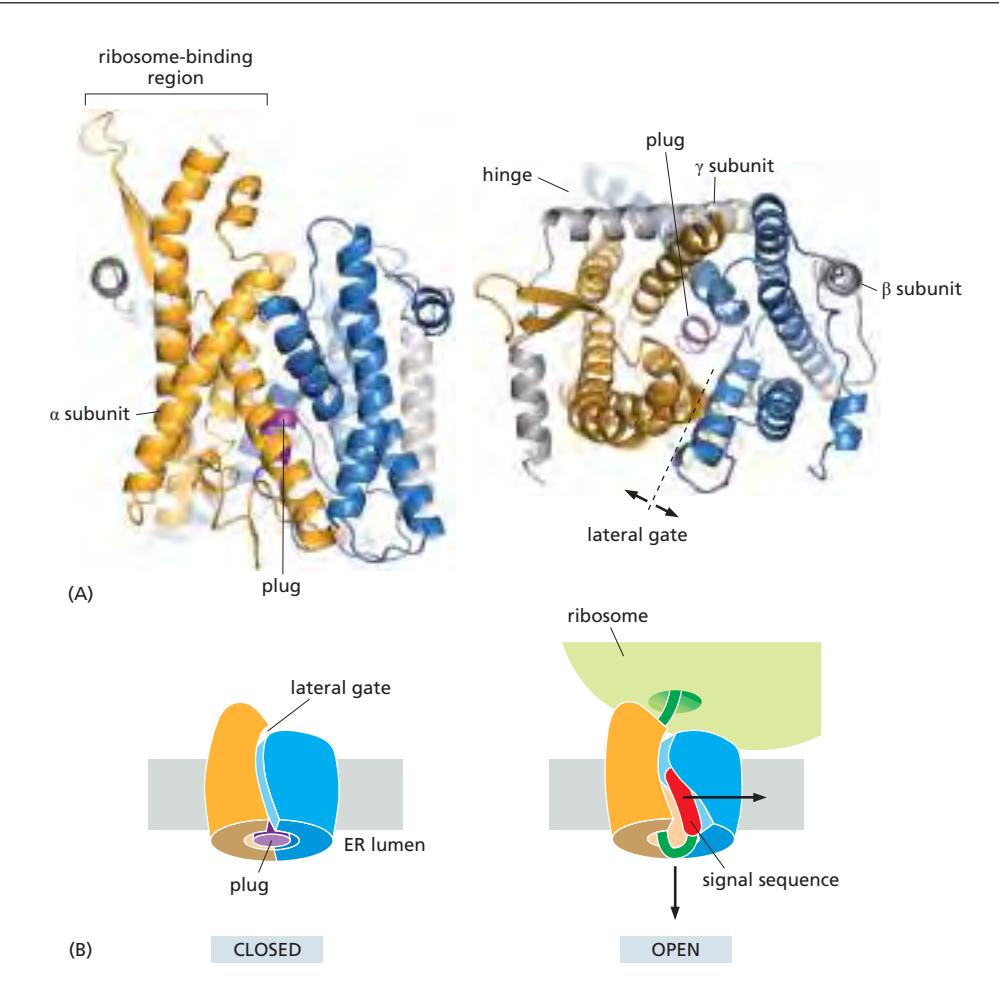 Figure 12-22: Structure of the Sec61 translocator (side view & top view)
Figure 12-22: Structure of the Sec61 translocator (side view & top view)
구조
- Sec61 (진핵생물) / SecY (세균, 고세균): ER membrane에 있는 단백질 통로(channel)
- Plug: 평소에 채널 입구를 막고 있음
- Lateral gate: 채널 옆면에 위치, 막으로의 단백질 삽입에 사용
- Hinge: 채널이 열리고 닫히는 데 관여
작동 원리
Closed state (평상시)
- Plug가 입구를 막고 있어 채널이 닫혀 있음
Active (open) state
- Signal sequence가 들어오면 plug가 이동하고 channel이 열림
- Translocation 중에 ribosomal large subunit 내부의 polypeptide tunnel이 Sec61 channel과 정렬됨
- ribosome의 peptidyl-transferase center에서 15 nm 떨어진 ER lumen까지 폴리펩타이드의 연속적인 경로 형성
- Polypeptide chain이 ER lumen으로 이동
2가지 결과:
- Translocation: 단백질 전체가 ER lumen으로 완전히 통과 (secreted protein / lumen protein)
- Lateral gate 통과: channel이 옆으로 열리면서 소수성 TM segment가 막으로 삽입 (membrane protein 형성)
central channel을 통한 translocation과 lateral gate를 통한 integration(embedding proteins into the membrane)을 선택적으로 처리할 수 있다.
중요: 전체 ER import 과정 (SRP 인식 → Sec61 translocation)은 polypeptide가 fold할 기회를 갖기 전에 co-translationally 발생한다.
22. Co-translational vs Post-translational Translocation
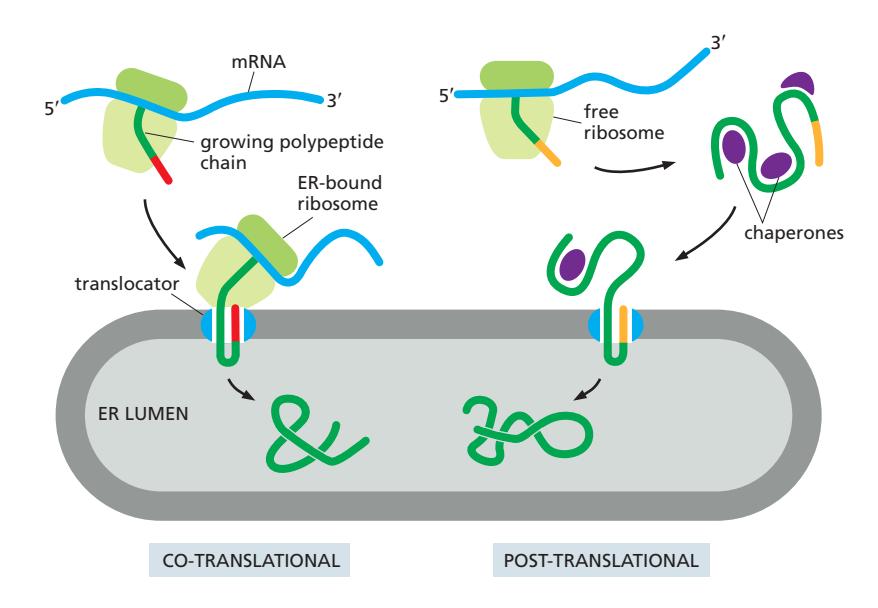
Figure 12-24: Co-translational and post-translational protein translocation
| Co-translational | Post-translational | |
|---|---|---|
| 타이밍 | 번역과 동시에 translocation | 번역 완료 후 translocation |
| SRP | 필요 | 불필요 |
| Chaperone | 불필요 | 필요 (단백질이 접히지 않도록) |
| 에너지원 | Translation 자체가 driving force (ATP 불필요) | ATP 필요 |
| 진핵생물 post-translational | — | Sec62/63 complex + BiP (Hsp70) + ATP |
두 경우 모두 단백질은 special ER signal sequence에 의해 ER로 안내됨
23. 3가지 Protein Translocation 방식 비교
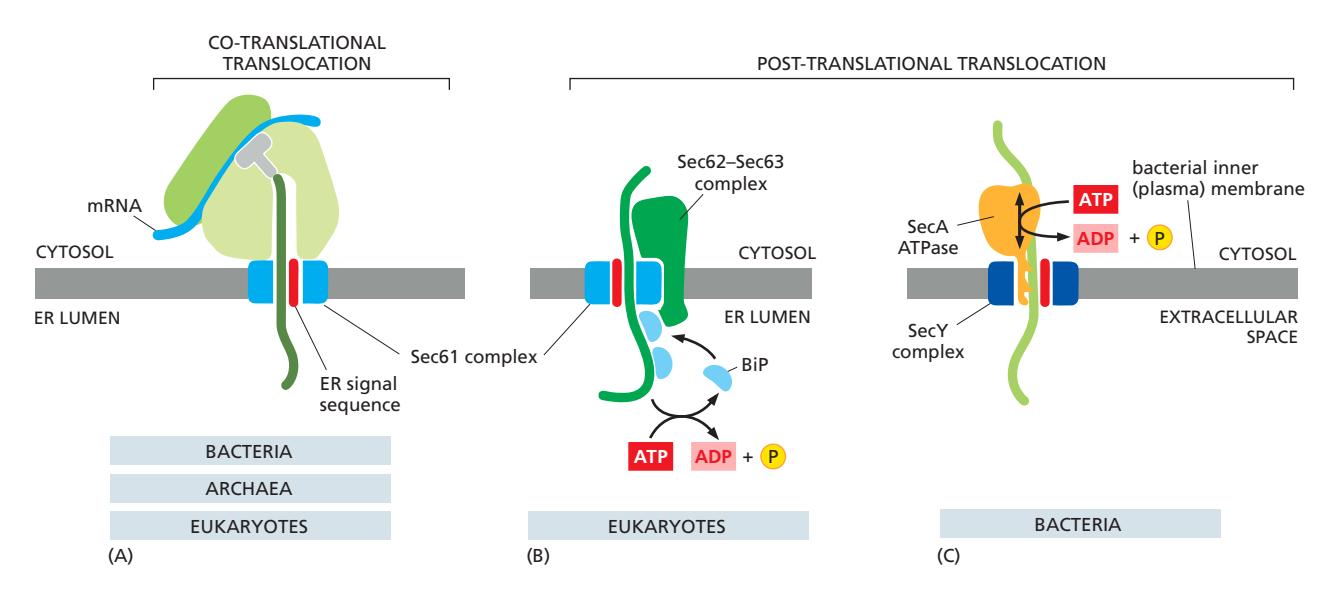 Figure 12-25: Three ways protein translocation can be driven through structurally similar translocators
Figure 12-25: Three ways protein translocation can be driven through structurally similar translocators
| (A) Co-translational | (B) Post-translational (Eukaryote) | (C) Bacterial | |
|---|---|---|---|
| 존재 | Bacteria, Archaea, Eukaryotes (공통) | Eukaryotes 전용 | Bacteria 전용 |
| 복합체 | Sec61 complex | Sec62/63 complex | SecY complex |
| 보조 인자 | SRP + SRP receptor | BiP (Hsp70) in ER lumen | SecA ATPase |
| 에너지 | Translation 자체 (ATP 불필요) | ATP | ATP |
| 원리 | Ribosome이 계속 번역하면서 polypeptide를 밀어 넣음 | BiP가 ER lumen 쪽에서 결합 → ATP 가수분해 구동 결합/방출 주기 → 한방향으로 이동 | SecA가 단계적으로 밀어 넣음 (piston 운동) |
Sec61, SRP, and the SRP receptor are found in all organisms, but SecA is unique to bacteria, and the Sec62–Sec63 complex is unique to eukaryotes.
24. Transmembrane Protein 삽입 — Single-pass
Transmembrane Protein Insertion 참조
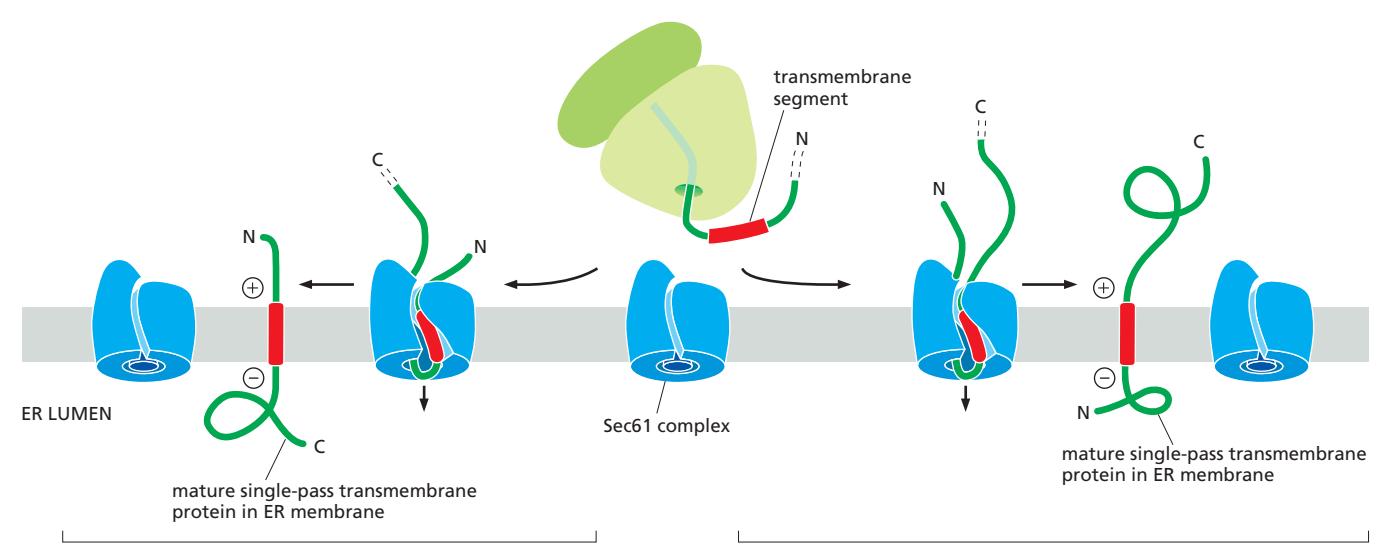 Figure 12-26: A transmembrane segment directs membrane protein insertion into the ER membrane
Figure 12-26: A transmembrane segment directs membrane protein insertion into the ER membrane
핵심 원리
- 단일 통과 막단백질은 **막관통 구간(transmembrane segment, TMS)**을 이용해 ER 막에 삽입
- TMS는 SRP에 의해 signal sequence처럼 인식되어 Sec61 translocator로 전달
- TMS는 lateral gate를 통해 지질이중층으로 삽입
starting-transfer sequence의 N/C terminal 방향 결정
TMS가 Sec61에서 lateral gate에 삽입될 때 두 가지 방향 중 하나:
N-말단이 세포질 쪽에 남는 경우:
- N-terminal 쪽이 길 때
- N-terminal 쪽에 양전하를 많이 띌 때
- N-terminal 쪽이 접혀져 있을 때
C-말단이 세포질 쪽에 남는 경우:
- C-terminal 쪽에 양전하를 많이 띌 때
25. Sequential use of cleaved ER signal sequence & TM segment
sequential use of cleaved ER signal and TM segment during membrane protein insertion 참조
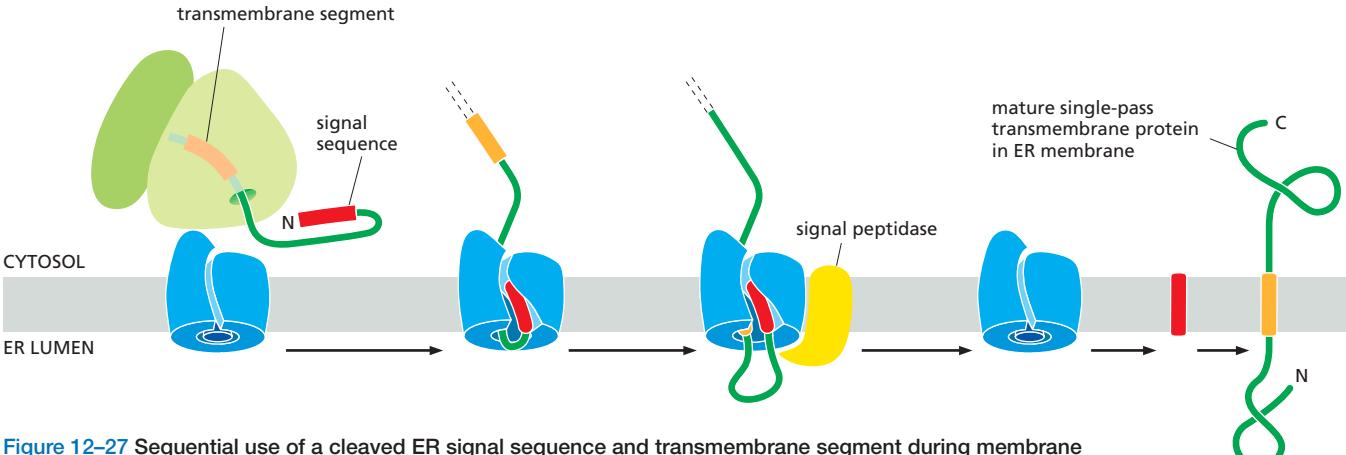 Figure 12-27: Sequential use of a cleaved ER signal sequence and transmembrane segment
Figure 12-27: Sequential use of a cleaved ER signal sequence and transmembrane segment
Lumen 쪽에 큰 N-말단 도메인을 가진 막단백질의 삽입 과정:
- N-말단 cleaved ER signal sequence로 ER 타겟팅 (분비 단백질과 동일)
- Signal sequence가 Sec61로 들어가고 signal peptidase가 절단
- 단백질의 나머지 부분이 ER lumen으로 translocation 시작
- TM segment가 Sec61에 도달 → 전이 정지(stop-transfer) 일어남 → translocation 중단
- TM segment가 lateral gate로 나가 지질이중층에 자리 잡음
- 나머지 단백질은 세포질 쪽에서 합성되다가 번역이 종료
- 결과: N-말단 도메인은 ER lumen (→ 최종적으로 세포 외부), C-말단은 cytosol
26. Multipass Transmembrane Protein 삽입
Multipass Transmembrane Protein Processing 참조
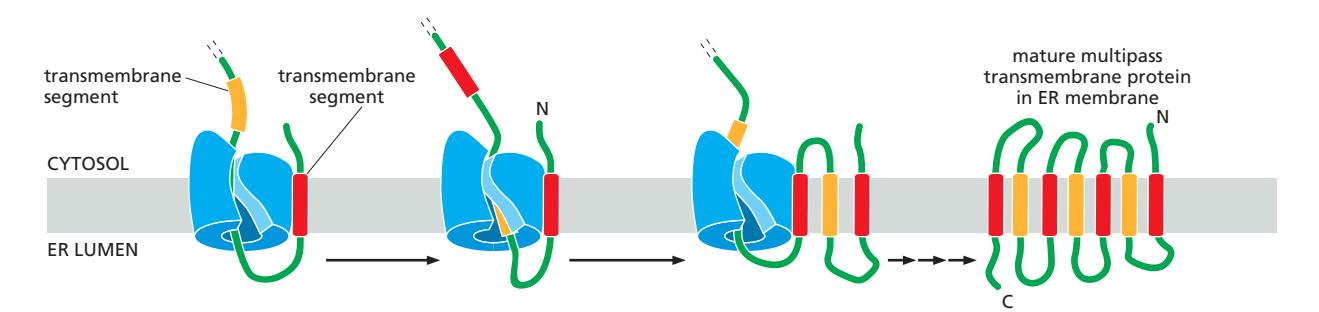
Figure 12-28: The insertion of a multipass transmembrane protein into the ER membrane
- 첫 번째 TM segment: single-pass membrane protein과 동일한 방식으로 삽입
- 이후 TM segments: 바로 앞의 구간과 반대 방향으로 lateral gate에 삽입
- 반복 → 모든 TM segment가 막에 자리 잡음
- 결과: 지그재그 구조로 막을 여러 번 통과하는 단백질 완성
Start-transfer signal vs Stop-transfer signal
각 TMS는 start-transfer sequence 또는 stop-transfer sequence로 번갈아 작용하며, 각각이 polarity(전하 분포)의 차이로 방향성을 독립적으로 결정한다.
-
Start-transfer sequence (시작 신호)
- SRP가 인식하여 Sec61 translocator로 유도
- Lateral gate를 통해 막에 삽입 → 그 다음 도메인이 ER lumen으로 translocation 시작
- TMS 방향 결정: 주변 아미노산의 **polarity (양전하 분포)**에 의해 결정
-
Stop-transfer sequence (정지 신호)
- Sec61로 들어오면 translocation을 멈춤 (stop-transfer)
- Lateral gate로 빠져나가 지질이중층에 삽입
- 이후 나머지 도메인은 cytosol 쪽에서 합성됨
-
핵심: 각 TMS가 개별적으로 polarity를 기반으로 방향을 결정하므로, 첫 번째 TMS가 전체 topology를 일방적으로 결정하는 것이 아니라 각 TMS가 삽입될 때 방향 결정에 기여함
-
이 과정이 모든 TM segment가 삽입될 때까지 계속됨
27. Tail-Anchored Proteins — Post-translational 막 삽입
Tailed-Anchored proteins insertion 참조
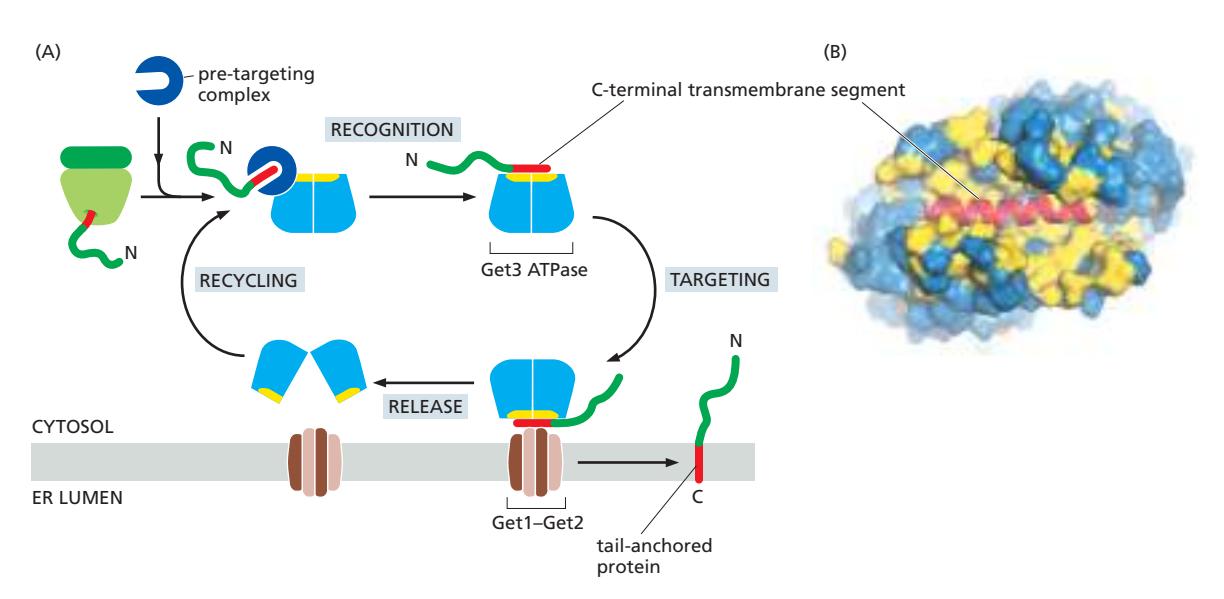
Figure 12-29: The insertion mechanism for tail-anchored proteins (Get3 pathway)
Tail-anchored proteins: C-말단에 single TM segment를 가진 막단백질로, 번역이 완전히 끝난 후 ER 막에 삽입됨 (SRP 사용 불가)
왜 SRP를 사용할 수 없는가?
- Ribosome이 termination codon에 도달하는 시점에 TMS가 될 polypeptide sequence가 여전히 ribosome exit tunnel 내부에 존재
- SRP가 이를 인식할 수 없음 → 단백질이 ribosome에서 cytosol로 먼저 방출됨
Get3 Pathway (진핵생물) 6단계
1단계: 번역 완료 & C-말단 노출
- 번역이 끝나면서 TMS가 세포질 쪽으로 노출
2단계: Pre-targeting complex 인식
- 세포질의 pre-targeting complex가 새로 노출된 소수성 C-말단 TMS를 즉시 인식·결합
- 단백질이 aggregation되거나 misfolding되는 것을 방지
3단계: Get3 결합
- Pre-targeting complex가 Get3 ATPase에 TMS를 전달
- Get3 내부의 **hydrophobic pocket(소수성 홈)**에 TMS가 자리 잡음
- 많은 methionine side chain으로 구성 → 유연한 구조
- 다양한 크기와 형태의 TMS를 인식·수용 가능
4단계: ER 막 타겟팅
- Get3-TMS 복합체가 ER 막의 Get1–Get2 receptor complex와 결합
- Get1–Get2는 막 단백질 삽입 기계 역할
5단계: 막 삽입
- ATP 가수분해 (ATP → ADP)로 Get3이 TMS를 방출
- TMS가 ER 막의 이중층에 삽입, 단백질의 N-말단은 세포질 쪽에 위치
6단계: Get3 재활용
- ADP가 해리되고 ATP가 결합 → Get3이 세포질로 돌아가 다음 라운드 준비
28. GPI Anchor (당인지질 앵커)
GPI anchor 참조
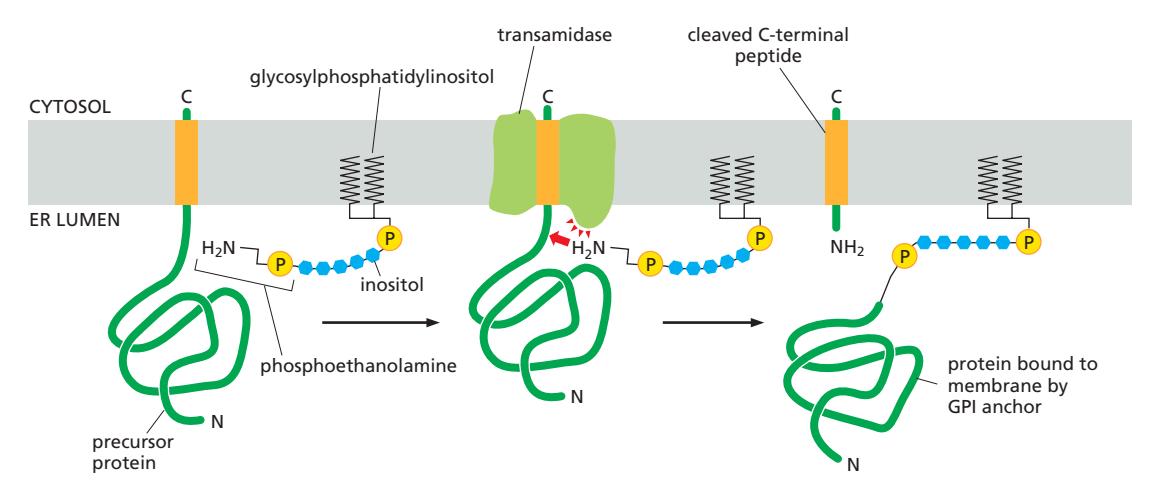 Figure 12-31: The attachment of a GPI anchor to a protein in the ER
Figure 12-31: The attachment of a GPI anchor to a protein in the ER
특징 & 기능적 의미
- 위치: 세포막의 외부(extracellular face)에만 위치
- 이동성: GPI anchor는 막을 자유롭게 lateral diffusion 가능 → 단백질 이동성이 높음
- 기능: 효소, 수용체, 세포 접착 단백질 등 다양
- 예시: Prion protein, alkaline phosphatase, Thy-1 glycoprotein
GPI 구조
GPI=glycophosphatidylinositol
- Inositol → 지질에 연결 (GPI 이름의 유래: Glycosylphosphatidylinositol)
- Inositol - GlcN(글루코사민) - 3개의 mannose -phosphoethanolamine
- 마지막 mannose가 phosphoethanolamine에 연결 → 단백질의 C-말단과 결합
GPI Anchor 부착 과정 (5단계)
1단계: ER로 이동
- N-말단 signal sequence로 ER 막으로 이동
- Signal peptidase가 N-말단 시그널을 절단
2단계: C-말단 막고정
- C-말단의 15~20개의 소수성 아미노산이 막에 박혀 있는 상태
- 나머지 단백질 부분은 ER lumen 쪽에 위치
3단계: Transamidase 작용 — GPI 부착
- ER의 transamidase 효소가 C-말단 막관통 부위를 절단
- 절단과 동시에 새로운 C-말단을 미리 만들어진 **GPI 구조물의 아민기(-NH₂)**에 붙임
- 아마이드 결합 형성 → 단백질과 GPI가 연결
4단계: Signal sequence for GPI modification
- C-말단 소수성 부위와 그 근처 lumen 쪽 몇 개 아미노산이 GPI 부착 신호 역할
- 이 신호를 다른 단백질에 붙이면, 그 단백질도 GPI-anchored protein이 됨
5단계: Membrane localization
- GPI는 지질에 붙어있기 때문에 단백질은 여전히 막에 고정됨
- 모든 아미노산 부분은 ER lumen 쪽(→ 최종적으로 세포막 바깥쪽)에 노출
29. ER 내 단백질 Folding — Chaperone 시스템
ER lumen으로 translocation된 단백질은 unfolded polypeptide chain 상태로 들어와 올바른 3차원 구조로 접혀야 한다.
ER Folding 환경
- Cytosol보다 산화된 환경 → Disulfide bond formation 촉진, PDI 활성에 필수
- 고농도의 chaperone과 folding enzyme
주요 Chaperone 3종
BiP (Binding Protein)
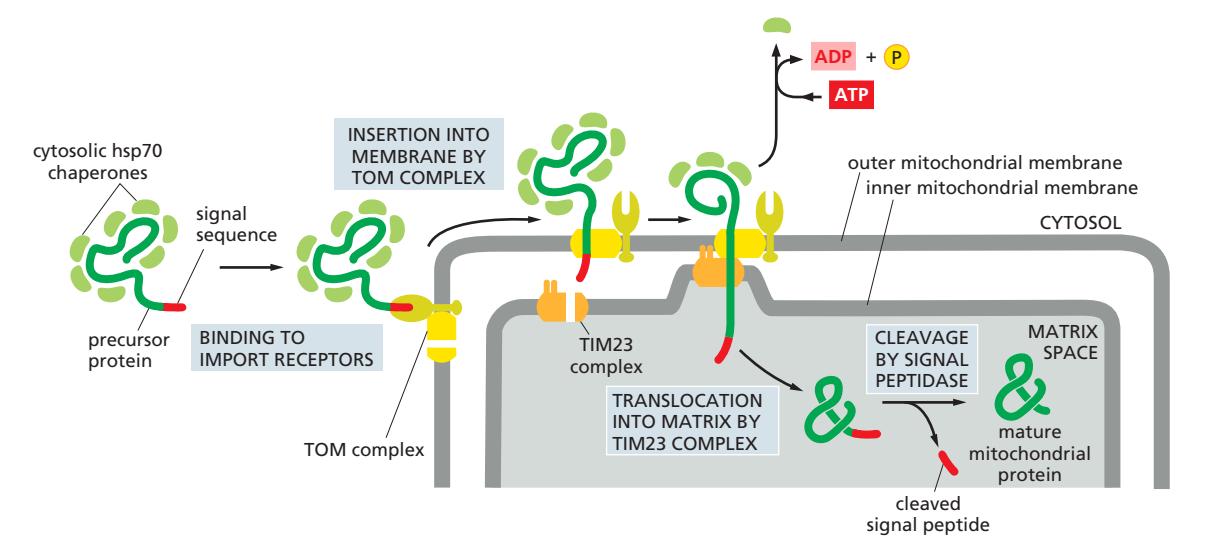 Figure 12-46: BiP의 ATP-dependent chaperone cycle 예시
Figure 12-46: BiP의 ATP-dependent chaperone cycle 예시
- Hsp70 family member, ER resident protein (C-말단 KDEL retention signal)
- Hydrophobic region 인식 → aggregation 방지, ER retention
- ATP-dependent cycle:
- ATP 결합 → Low affinity state (substrate 교환 빠름)
- ATP hydrolysis → High affinity state (tight binding)
- ADP 방출 → substrate 방출, folding 시도 기회
- BiP는 정상상태에서는 단백질의 접힘을 돕고,
- 스트레스 상태에서는 misfolded protein을 붙잡아둔다.
Calnexin / Calreticulin
- Ca²⁺-dependent lectin chaperone (glycoprotein 특화)
- Calnexin: ER membrane-bound / Calreticulin: ER lumen 내 soluble
- Singly glucosylated N-linked oligosaccharide 인식 → retention (ER 탈출 방지)
- ERp57 (PDI family member)와 협력 → free sulfhydryl group 인식 → 불완전한 disulfide bond 감지
PDI (Protein Disulfide Isomerase)
- Disulfide bond 형성 촉매 + 잘못 형성된 disulfide bond 재배열
- Oxidoreductase: 양방향 활성 (형성 & 분해 모두 가능)
- C-말단 KDEL signal → ER resident
- PDI family: 여러 specialized member 존재 (일부는 ERAD에서 unfolding에 특화)
30. Disulfide Bond Formation — PDI 메커니즘
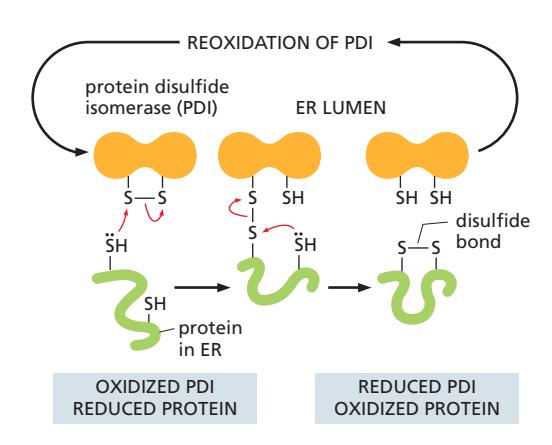 Figure 12-30: The formation of disulfide bonds in the ER lumen
Figure 12-30: The formation of disulfide bonds in the ER lumen
ER lumen = oxidizing environment (cytosol은 reducing) → disulfide bond 형성에 유리
PDI 4단계 메커니즘
- Substrate 인식: PDI가 새로 translocation된 단백질의 free cysteine (–SH) 인식
- PDI의 disulfide bond가 substrate protein의 free sulfhydryl group으로부터 전자를 받음 → 이 과정에서 PDI와 substrate 사이에 intermolecular mixed disulfide bond 형성
- Substrate의 두 번째 free sulfhydryl group이 전자를 mixed disulfide bond에 기부
- 결과: Substrate protein이 산화됨 (disulfide bond 형성)
- PDI는 환원됨 (reduced state)
- 다른 ER enzyme이 reduced PDI를 reoxidize함 → 다음 cycle 준비
Disulfide Bond 재배열 (Rearrangement)
- 여러 cysteine이 있어 처음에는 잘못 pairing될 수 있음
- PDI가 incorrect disulfide bond를 인식 → 절단 → 올바른 쌍으로 재형성
- Trial-and-error 방식의 올바른 folding 가능
Cytosolic domain에는 disulfide bond가 형성되지 않음 (cytosol = reducing environment)
31. N-linked Glycosylation — 당사슬 En Bloc 부착
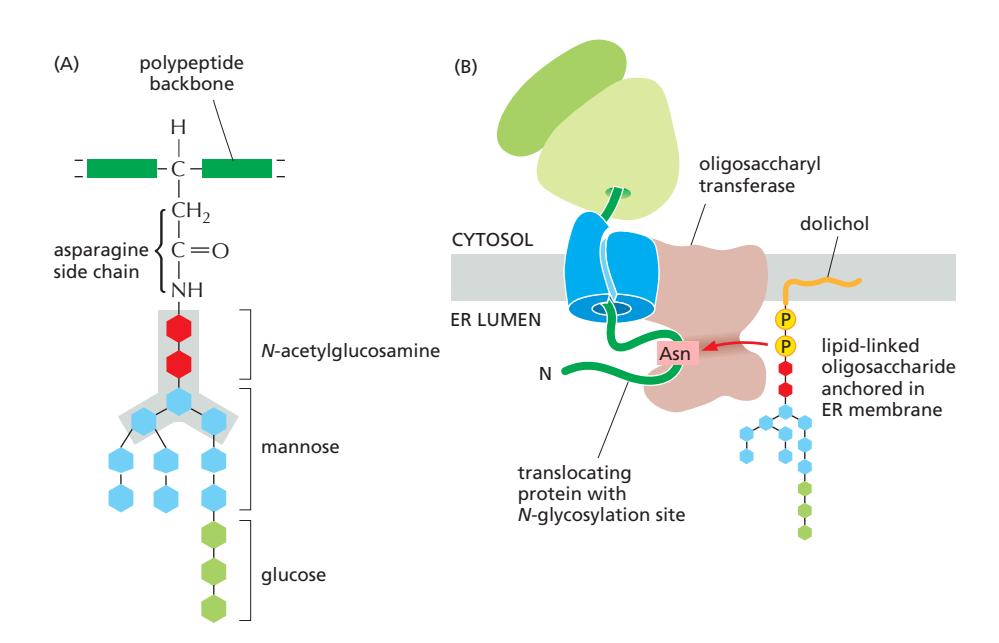 Figure 12-31: N-linked glycosylation — precursor oligosaccharide structure and transfer
Figure 12-31: N-linked glycosylation — precursor oligosaccharide structure and transfer
N-linked glycosylation은 preformed precursor Oligosaccharides가 단백질의 asparagine 잔기에 en bloc (한 덩어리로) 부착되는 과정이다. ER에서 일어나는 가장 흔한 glycosylation 형태이다.
Precursor 구조: Glc₃Man₉GlcNAc₂ (총 14개 sugar)
| Sugar | 개수 |
|---|---|
| N-acetylglucosamine (GlcNAc) | 2개 |
| Mannose (Man) | 9개 |
| Glucose (Glc) | 3개 |
- Core region (5개 sugar: GlcNAc×2 + Man×3) → Golgi에서 extensive trimming 후에도 보존
Oligosaccharyl Transferase (OST)
- Sec61 complex와 결합 : Co-translational하다!
- Active site가 ER lumen에 노출
- Target sequence: Asn-X-Ser/Thr
- Asn: Asparagine (attachment site)
- X: Any amino acid except proline
- Ser/Thr: Serine or Threonine
Co-translational Modification이다 — polypeptide가 ER lumen에 진입하는 즉시, translation 진행 중에 부착
N-linked Glycosylation의 기능
- Quality Control Tag → proper protein folding in ER (glucose 유무로 folding 상태 표시)
- Protein Stability and Solubility 향상: 당의 극성으로 solubility 증가, aggregation 방지, protease로부터 보호
- Cell-Cell Recognition → immune system: lectin binding, receptor recognition, protein sorting
- 특정 위치로 protein targeting
32. Glycosylation-Based Quality Control — Glucose Trimming Cycle
Glycosylation-Based Monitoring 참조
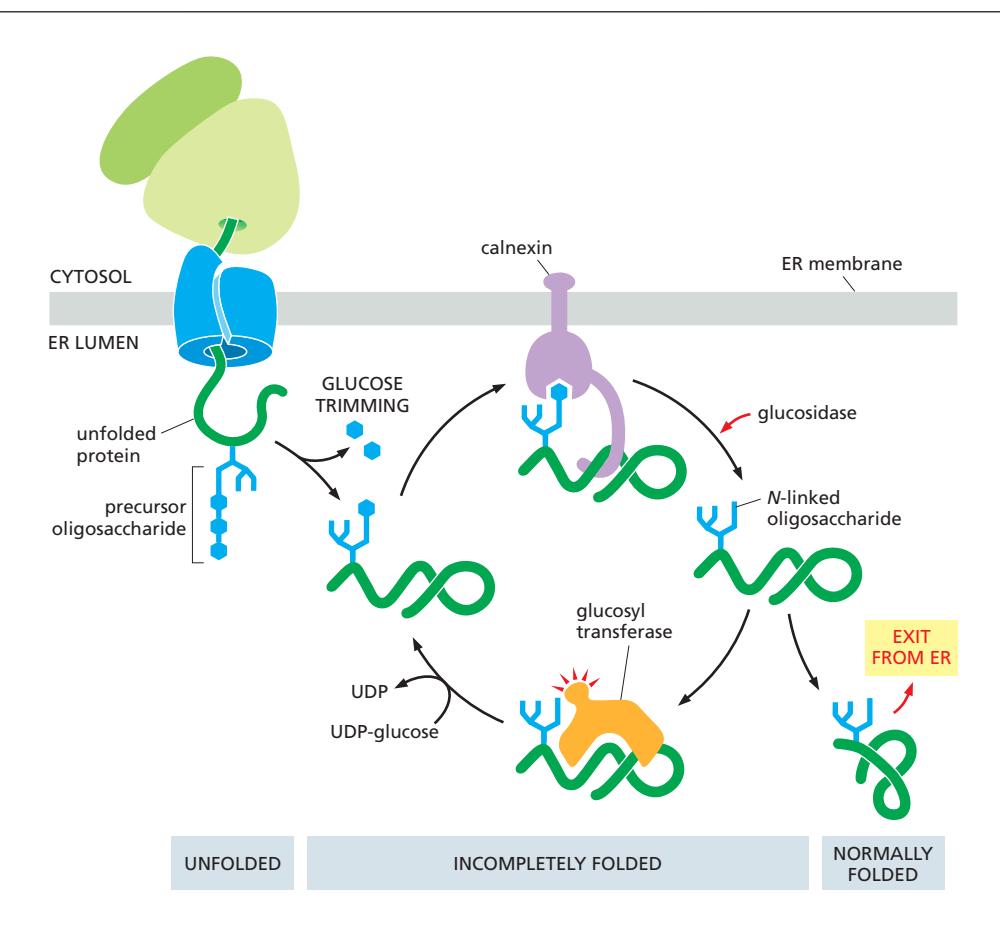 Figure 12-33: The glucose trimming cycle for quality control of glycoprotein folding
Figure 12-33: The glucose trimming cycle for quality control of glycoprotein folding
감시 메커니즘: N-linked oligosaccharide의 glucose를 제거하고 재부착하여 folding 상태를 표시
Quality Control Cycle 4단계
Step 1: Initial Trimming by Glucosidase
- ER glucosidase가 3개 중 2개 glucose를 빠르게 제거
- 결과: Singly glucosylated 상태 (Glc₁Man₉GlcNAc₂)
Step 2: Calnexin/Calreticulin Binding
- Monoglucosylated oligosaccharide → Calnexin/Calreticulin 결합 신호
- 단백질을 ER에 retention (탈출 방지)
- ERp57도 함께 recruit → free SH group (불완전한 disulfide)도 동시 감시
- Folding 시도
Step 3: Final Glucose Removal
- Glucosidase가 마지막 glucose 제거 → Calnexin/Calreticulin 해리
- De-glucosylated glycoprotein 형성
Step 4: Folding State Assessment
- Glucosyl transferase가 단백질의 folding 상태를 평가 (노출된 hydrophobic region 인식)
| 결과 | 처리 |
|---|---|
| 올바르게 접힘 | Glucose 재부착 없음 → ER export |
| 불완전하게 접힘 | Glucose 재부착 → cycle 반복 |
- 각 cycle마다 단백질은 folding을 시도할 기회를 얻는다.
- Calnexin/calreticulin이 단백질의 aggregation을 방지하면서 반복적 folding 시도 지원
33. ERAD (ER-Associated Degradation) — 잘못 접힌 단백질 제거
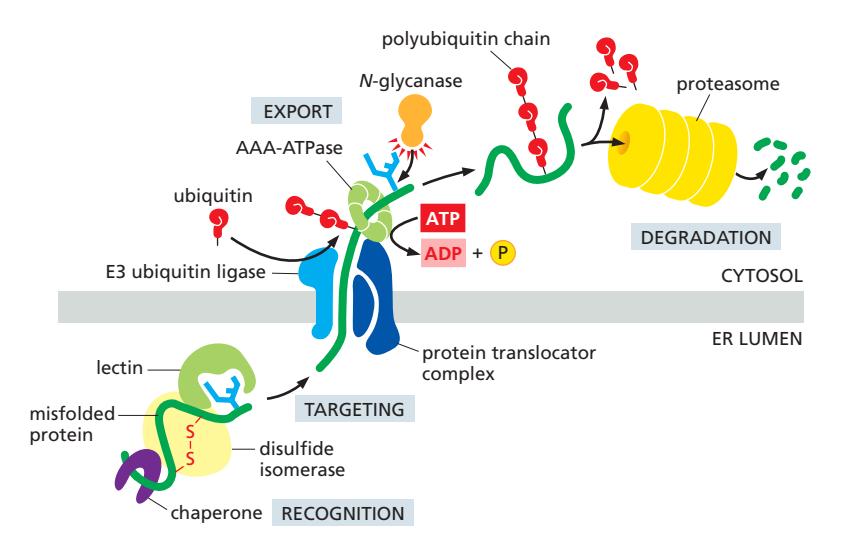 Figure 12-34: ER-associated degradation (ERAD) pathway
Figure 12-34: ER-associated degradation (ERAD) pathway
Chaperone의 도움에도 불구하고 올바르게 접히지 못한 단백질 → ERAD로 분해
Recognition Signals (인식 신호)
| 신호 | 인식 인자 |
|---|---|
| Trimmed N-linked oligosaccharides (mannose 감소) | ER-lumenal lectin이 trimmed oligosaccharide 인식 |
| Exposed hydrophobic regions | BiP |
| Free sulfhydryl groups (미완성 disulfide) | ERp57 (PDI family) |
| Unassembled oligomeric subunits | BiP, calnexin/calreticulin |
ERAD 전체 과정 (6단계)
- Substrate Recognition: Chaperone, lectin, PDI family가 misfolded protein 인식 → retrotranslocation machinery로 guide
- Unfolding: PDI family가 disulfide bond 완전히 환원 → linear polypeptide chain (translocator 통과를 위해 필수)
- Retrotranslocation: Translocator channel을 통해 ER → cytosol로 이동
- Ubiquitylation: E3 ubiquitin ligase (translocator complex 일부)가 cytosol 측에서 polyubiquitin 부착
- Proteasome recognition signal
- Backsliding into ER 방지
- AAA-ATPase의 binding handle
- Extraction: AAA-ATPase가 ubiquitylated substrate 인식 → ATP hydrolysis로 pulling force → cytosol로 완전 추출
- Deglycosylation + Proteasomal Degradation: Cytosolic N-glycanase가 oligosaccharide 제거 → proteasome에서 분해 → amino acid 재활용
34. Quality Control 종합 — BiP와 Mannosidase Timer
Quality control of ER protein folding 참조
Quality Control 시스템 3요소
1. 감시 메커니즘 (Glycosylation-Based)
- N-linked oligosaccharide의 glucose를 제거하고 재부착하여 folding 상태를 표시
- Calnexin/calreticulin → 불완전한 glycoprotein retention
- BiP → hydrophobic region 감시
- ERp57 → free sulfhydryl 감시
2. 시간 기반 선별 (Mannosidase Timer)
- ER-resident mannosidase가 terminal mannose를 천천히 제거
- Fast folding → mannosidase 작용 전 ER 탈출
- Slow folding → mannose trimming → ERAD signal
- Trimmed oligosaccharide → ERAD lectin(OS-9, EDEM 등) 인식 → degradation (비가역적)
3. UPR 적응 반응
- ER stress 과도 시 UPR 활성화 → ER capacity 증가 (§35 참조)
BiP의 이중 역할 요약
| 상태 | BiP의 역할 |
|---|---|
| 정상 | 단백질의 접힘을 돕고 (folding assistant) |
| ER stress | misfolded protein을 붙잡아둔다 (retention factor) |
너무 오래 ER에 머무른 단백질은 mannose trimming에 의해 ERAD로 타겟팅된다.
35. Unfolded Protein Response (UPR) — ER 스트레스 적응 반응
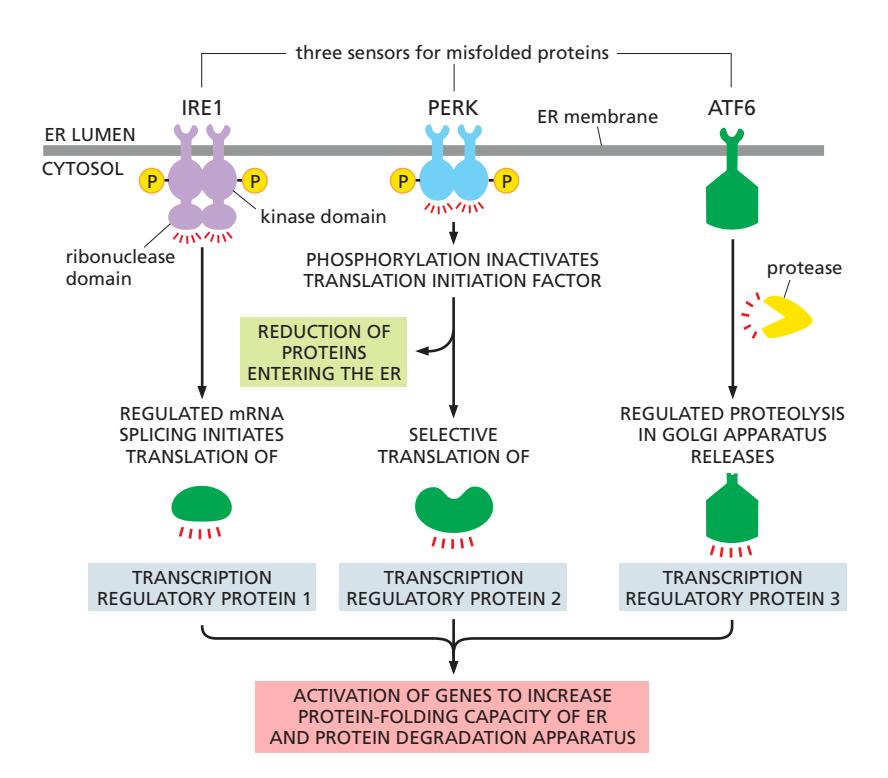 Figure 12-35: The three pathways of the unfolded protein response (UPR)
Figure 12-35: The three pathways of the unfolded protein response (UPR)
UPR은 세 가지 독립적이면서 협력하는 경로로 구성된다.
공통 Trigger
- Misfolded protein 축적 → BiP가 IRE1 / PERK / ATF6에서 해리 → 각 sensor 활성화
1. IRE1 Pathway (가장 보존된 경로)
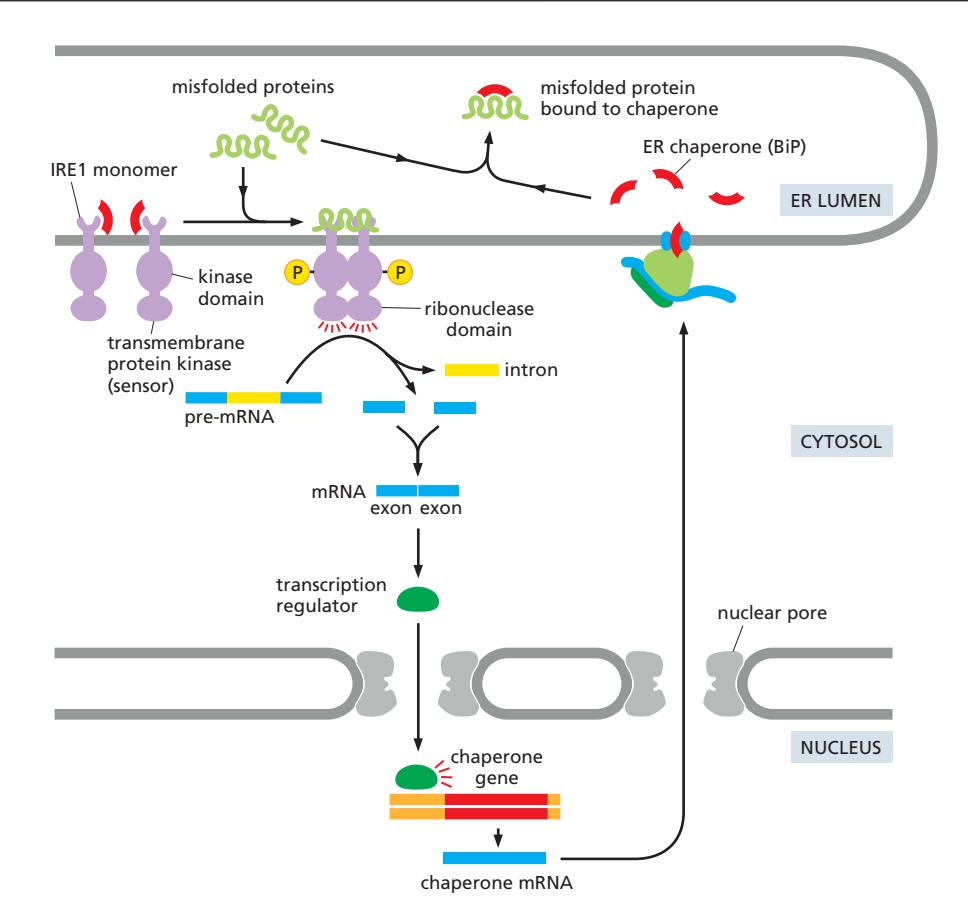 Figure 12-36: The IRE1 pathway — XBP1 mRNA splicing
Figure 12-36: The IRE1 pathway — XBP1 mRNA splicing
정상 상태:
- BiP가 IRE1의 lumenal domain에 결합
- IRE1이 inactive monomer로 유지
ER stress 시:
- BiP가 misfolded protein에 결합하기 위해 IRE1에서 dissociate
- Misfolded protein이 IRE1의 lumenal domain에 직접 결합
- IRE1 monomer들이 oligomerize
- Trans-autophosphorylation 발생
- Cytosolic ribonuclease domain 활성화
- cytosolic mRNA를 splicing (핵 splicing과 독립, spliceosome 불사용)
- Activated IRE1이 XBP1 mRNA의 두 위치를 인식
- Intron이 제거됨
- Spliced mRNA가 transcription factor를 encode
- 이 전사인자가 핵으로 들어감
- UPR target gene의 transcription 증가
- ER chaperone, ERAD component, lipid synthesis enzyme 등 발현
2. PERK Pathway
3. ATF6 Pathway
공통 Target Genes
| 유전자 | 기능 |
|---|---|
| BiP, PDI, Calnexin, Calreticulin | ER chaperone (folding capacity ↑) |
| ERAD machinery | Degradation capacity ↑ |
| Lipid synthesis enzyme | ER membrane 확장 |
36. ER에서의 Phospholipid 합성
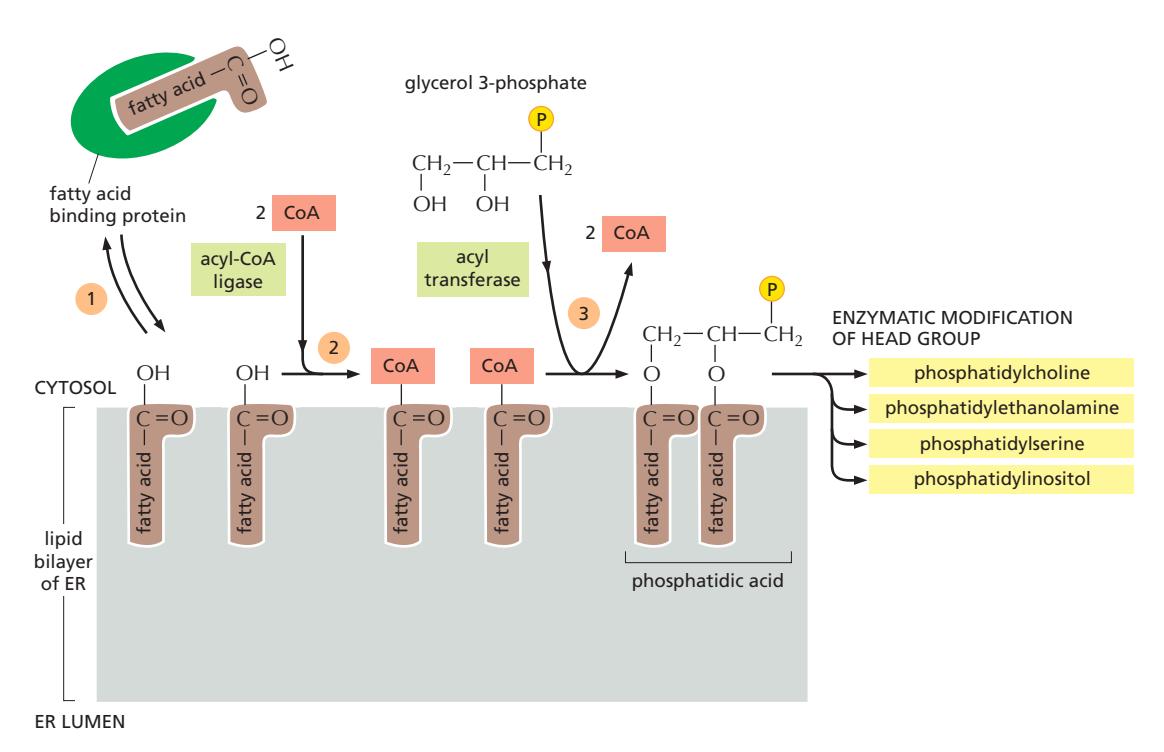 Figure 12-37: Phospholipid synthesis in the ER
Figure 12-37: Phospholipid synthesis in the ER
ER membrane = 세포의 주요 lipid 합성 장소 (phospholipid, cholesterol, ceramide 등)
- 합성에 관여하는 모든 효소는 ER membrane에 위치하며, 이들의 active site는 cytosol을 향하고 있다.
- 모든 phospholipid 합성은 cytosolic leaflet에서만 일어남
Phospholipid 합성 4단계
Step 1: Fatty Acid 전달
- Cytosol에서 합성된 fatty acid는 물에 녹지 않으므로 fatty acid binding protein이 이들을 ER로 운반한다.
Step 2: Fatty Acid 활성화 & 부착
- ER membrane에 도착한 fatty acid는 acyl-CoA ligase에 의해 CoA와 결합하여 활성화된다 (fatty acid-CoA). Acyl transferase가 두 개의 activated fatty acid를 glycerol phosphate에 순차적으로 부착하여 phosphatidic acid를 생성한다.
Step 3: Precursor for phospholipids
- 강의노트엔 그냥 이렇게만 써 있음. phospholipids의 precursor로 기능한다.
Step 4: Head Group 수정
- 이후 단계들은 새로 형성된 lipid molecule의 head group을 결정한다. 이 단계들은 bilayer의 화학적 성질을 결정하지만, net membrane growth를 일으키지는 않는다.
합성되는 주요 Phospholipid
- Phosphatidylcholine (PC) / Phosphatidylethanolamine (PE) / Phosphatidylserine (PS) / Phosphatidylinositol (PI)
37. Phospholipid Translocator — Membrane Asymmetry
Lipid bilayer synthesis / Scramblase / Flippase 참조
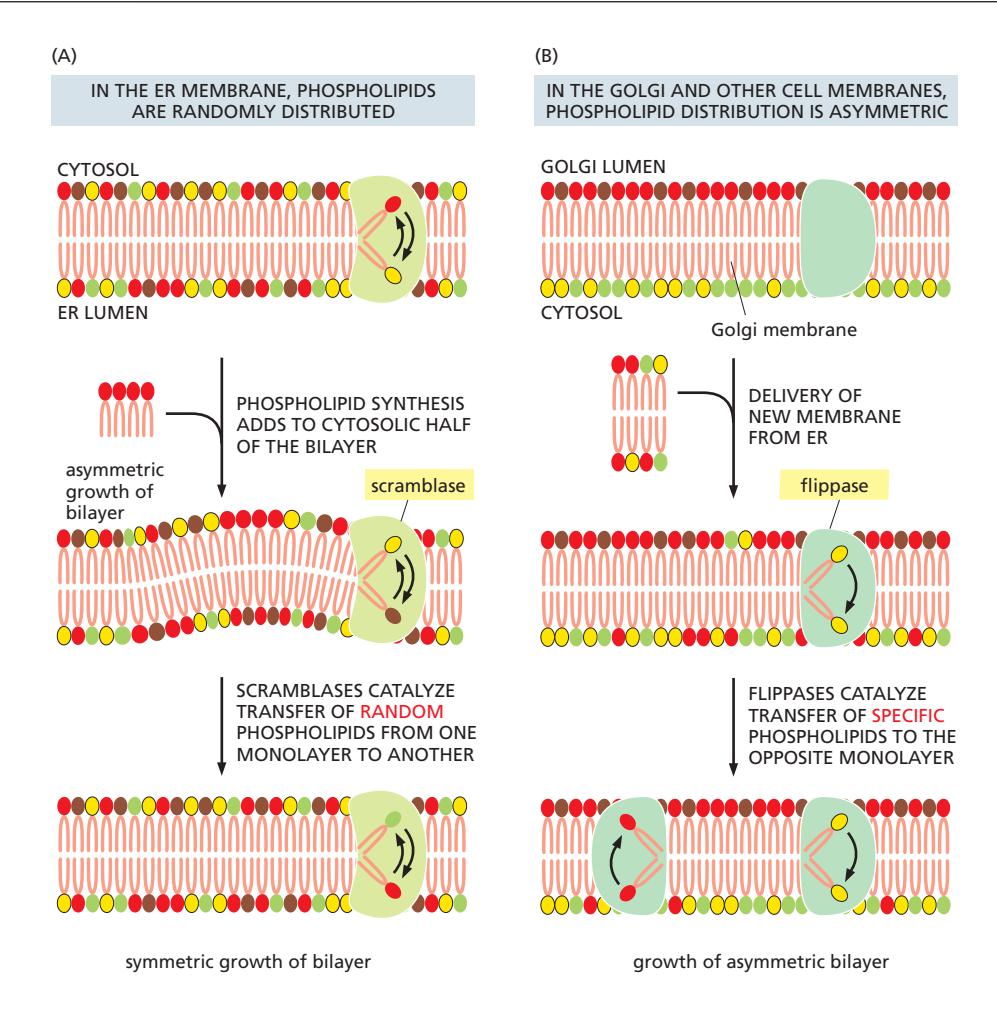 Figure 12-38: Scramblase and flippase establish membrane lipid asymmetry
Figure 12-38: Scramblase and flippase establish membrane lipid asymmetry
Membrane 확장의 비대칭성
- Phospholipid 합성이 cytosolic leaflet에서만 일어남 → 한쪽만 확장될 위험
- ER membrane은 두 leaflet에서 다른 phospholipid들이 거의 동등하게 분포되어 있다.
Scramblase — ER에서의 대칭 분포
- 이 대칭적 분포는 scramblase라는 phospholipid translocator에 의해 달성된다.
- Scramblase는 새로 형성된 phospholipid molecule 일부를 cytosolic leaflet에서 lumenal leaflet로 전달한다.
- 이때 ATP는 필요하지 않다. 즉 passive transport
- 비선택적: 모든 phospholipid 종류 동등하게 이동 / 양방향: 평형을 향해
Flippase — Golgi·Plasma membrane의 비대칭 유지
- ATP가 Flippase의 기능에 필요한 active transport이다.
- Golgi와 plasma membrane은 Flippase에 의해 asymmetry를 유지한다.
- Cytosolic side → PS, PE
- Outer/lumen side → PC, sphingolipid
- 선택적 (aminophospholipid 특이): PS, PE를 안쪽(cytosolic side)으로 이동 / 단방향
Scramblase vs Flippase 비교
| Scramblase | Flippase | |
|---|---|---|
| 위치 | ER membrane | Golgi, Plasma membrane |
| 에너지 | ATP 불필요 (passive) | ATP 필요 (active) |
| 방향성 | 양방향 (평형) | 단방향 |
| 기질 특이성 | 비선택적 | 선택적 (PS, PE 특이) |
| 결과 | Bilayer 대칭 | Bilayer 비대칭 |
Apoptosis 시 특이 변화
Apoptosis 동안 flippase가 비활성화되고 scramblase가 활성화되어 phosphatidylserine(PS)이 extracellular leaflet에 노출된다. 이는 macrophage에게 세포를 제거하라는 신호가 된다.