Unfolded Protein Response
Unfolded protein response (UPR)는 ER lumen에 misfolded protein이 축적될 때 활성화되는 신호전달 경로이다. UPR은 ER의 protein-processing capacity를 증가시키고, 새로운 단백질 합성을 조절하며, 필요시 세포 사멸을 유도하여 ER homeostasis를 회복한다.
UPR의 필요성
ER Stress의 원인
ER stress는 다음과 같은 상황에서 발생한다:
- Misfolded protein의 과도한 축적
- 단백질 합성 속도가 folding capacity 초과
- Chaperone 부족
- 환경적 stress (heat, oxidative stress)
- 영양 결핍
- Viral infection
Stress의 결과
ER stress가 해소되지 않으면:
- Chaperone이 포화됨
- Misfolded protein이 aggregate 형성
- ER function 손상
- Cellular dysfunction
- 최종적으로 cell death
Three Parallel UPR Pathways
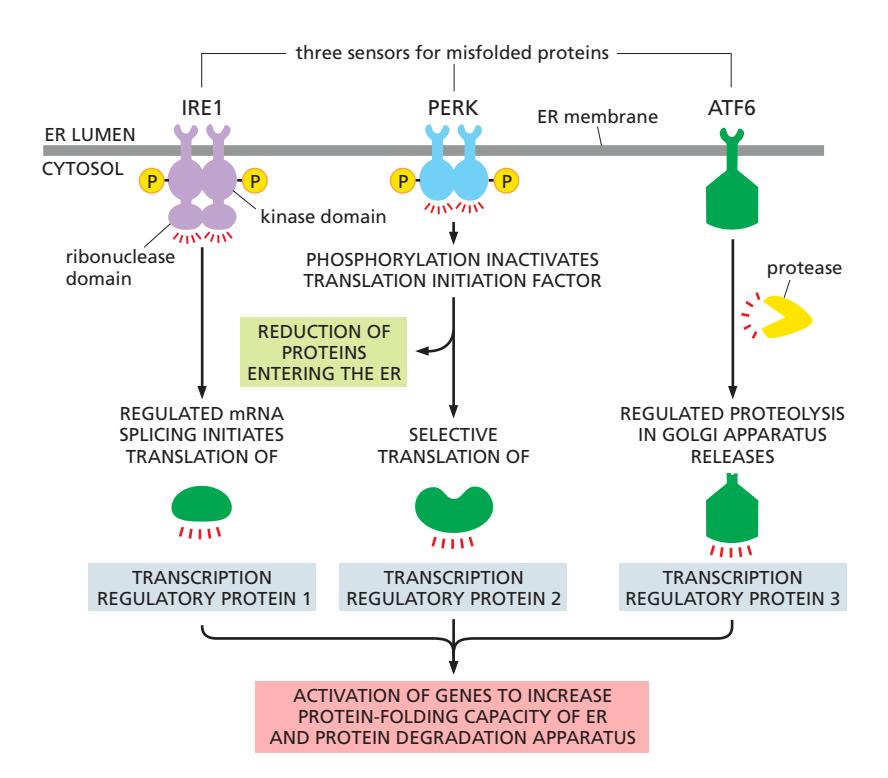
UPR은 세 가지 독립적이면서 협력하는 경로로 구성된다.1 각 경로는 ER membrane에 있는 transmembrane sensor protein에서 시작하여, 최종적으로 핵에서 전사인자를 활성화한다.
1. IRE1 Pathway
Sensor Activation
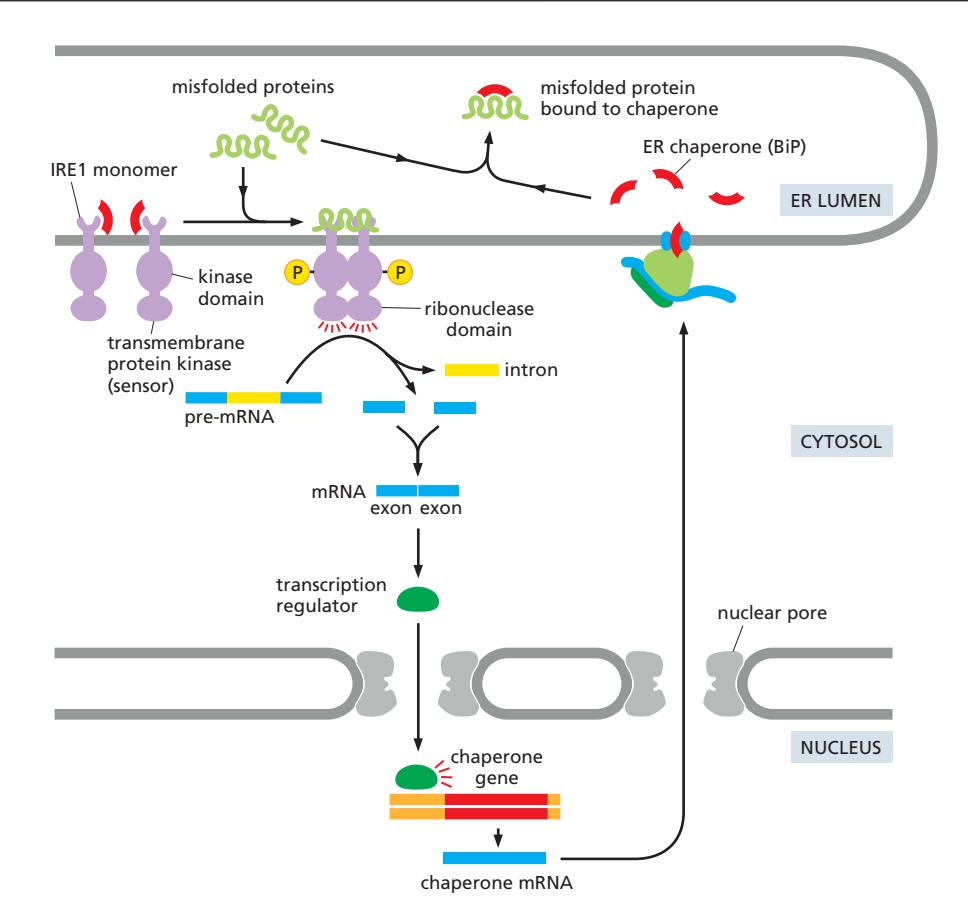
IRE1은 transmembrane protein kinase이자 endoribonuclease이다.
Normal state:
- BiP가 IRE1의 lumenal domain에 결합
- IRE1이 inactive monomer로 유지
Stress condition:
- BiP가 misfolded protein에 결합하기 위해 IRE1에서 dissociate
- Misfolded protein이 IRE1의 lumenal domain에 직접 결합
- IRE1 monomer들이 oligomerize
- Trans-autophosphorylation 발생
- Cytosolic ribonuclease domain 활성화
Unique mRNA Splicing Mechanism
IRE1 pathway의 가장 독특한 특징은 cytosolic mRNA를 splicing한다는 것이다. 이는 nuclear splicing과 완전히 독립적이며 spliceosome을 사용하지 않는다.
Mechanism:
- Activated IRE1이 XBP1 mRNA의 두 위치를 인식
- Endoribonuclease가 두 지점을 절단
- Intron이 제거됨2
- RNA ligase가 남은 exon들을 연결
- Spliced mRNA 생성
결과:
- Spliced XBP1 mRNA가 XBP1s transcription factor를 encode
- 이 전사인자가 핵으로 들어감
- UPR target gene의 transcription 증가
- ER chaperone, ERAD component, lipid synthesis enzyme 등 발현
Evolutionary Conservation
IRE1 pathway는 yeast에서 처음 발견되었으며 모든 eukaryotic cell에 보존되어 있다. 이는 UPR의 가장 오래되고 필수적인 경로임을 시사한다.
2. PERK Pathway
Sensor Activation
PERK도 transmembrane kinase이며 IRE1과 유사한 방식으로 활성화된다:
- BiP dissociation
- Oligomerization
- Trans-autophosphorylation
Translational Control
PERK의 주요 target은 translation initiation factor eIF2α이다.
Step 1: eIF2α Phosphorylation Activated PERK가 eIF2α를 인산화한다. 인산화된 eIF2α는 translation initiation을 억제한다.
Step 2: Global Translation Attenuation 대부분의 mRNA 번역이 감소한다. 이는 ER로 들어오는 새로운 단백질의 양을 줄여서 ER의 부담을 경감한다.
Step 3: Selective Translation 흥미롭게도, 일부 특정 mRNA는 eIF2α가 인산화된 상태에서 오히려 선호적으로 번역된다. 이 중 하나가 ATF4 transcription factor이다.
Step 4: ATF4-Mediated Transcription 번역된 ATF4가 핵으로 들어가서 UPR target gene을 활성화한다. 여기에는 antioxidant enzyme, amino acid metabolism enzyme, ERAD component 등이 포함된다.
Dual Function
PERK pathway는 두 가지 시간 척도로 작동한다:
- 즉각적 효과: Translation 억제로 ER load 감소
- 장기적 효과: Transcription 활성화로 ER capacity 증가
3. ATF6 Pathway
Latent Transcription Factor
ATF6는 ER membrane에 embedded된 전사인자이다. 이 독특한 구조 때문에 특별한 활성화 메커니즘이 필요하다.
Normal state:
- ATF6가 ER membrane에 anchored
- Transcription factor domain이 cytosol에 노출
- 하지만 핵으로 갈 수 없음
Stress condition:
Step 1: ER to Golgi Transport ER stress가 발생하면 ATF6가 Golgi apparatus로 수송된다. 이 수송은 COPII vesicle을 통한 정상적인 ER-to-Golgi trafficking을 이용한다.
Step 2: Proteolytic Cleavage Golgi membrane에 있는 Site-1 protease (S1P)와 Site-2 protease (S2P)가 순차적으로 ATF6를 절단한다.
- S1P가 lumenal domain을 절단
- S2P가 transmembrane domain을 절단
- Cytosolic domain이 membrane에서 release
Step 3: Nuclear Translocation Cleaved cytosolic domain이 핵으로 이동하여 active transcription factor로 작동한다.
Step 4: Gene Activation ATF6가 UPR target gene을 활성화한다. 특히 ER chaperone과 ERAD component의 발현을 증가시킨다.
Similarity to SREBP
이 activation mechanism은 cholesterol biosynthesis를 조절하는 SREBP의 활성화와 매우 유사하다. 둘 다 regulated intramembrane proteolysis (RIP)를 사용한다.
Target Gene의 중복과 특이성
Common Targets
세 pathway가 활성화하는 유전자들이 부분적으로 겹친다:
- ER chaperone (BiP, PDI, calnexin 등)
- ERAD component3
- Protein translocation machinery
- Lipid synthesis enzyme (ER membrane 확장용)
Pathway-Specific Targets
각 pathway는 고유한 target도 가진다:
IRE1:
- ER expansion
- Lipid synthesis
- Phospholipid biosynthesis
PERK:
- Antioxidant response
- Amino acid metabolism
- Apoptosis regulators
ATF6:
- ER quality control
- Protein secretion
- XBP1 (IRE1 pathway component)
Coordinated Response
세 pathway가 동시에 활성화되면 종합적이고 강력한 adaptive response가 일어난다. 이는 단일 pathway보다 훨씬 효과적으로 ER homeostasis를 회복한다.
Physiological UPR
UPR은 병리적 상황뿐만 아니라 정상적인 생리적 과정에서도 사용된다.
Insulin Production in β Cells
식사 후 혈당이 상승하면 pancreatic β cell은 대량의 insulin을 생산해야 한다. 이때 ER의 부담이 급격히 증가한다.
Adaptive response:
- PERK의 부분적 활성화
- eIF2α의 transient phosphorylation
- Insulin synthesis rate 조절
- ER overload 방지
- 적절한 insulin 분비 유지
B Cell Differentiation
B cell이 plasma cell로 분화하면 antibody를 대량 생산하기 시작한다. 이를 위해서는 ER의 극적인 확장이 필요하다.
Preparatory response:
- IRE1 활성화
- XBP1 mRNA splicing
- ER chaperone과 membrane 대량 생산
- ER content의 dramatic increase
- Antibody secretion capacity 확보
이러한 예들은 UPR이 단순히 stress response가 아니라, 세포의 정상적인 adaptation mechanism임을 보여준다.
Chronic UPR과 Apoptosis
Persistent Activation의 결과
만약 ER stress가 해소되지 않으면:
- UPR signaling이 지속됨
- 특히 PERK pathway의 prolonged activation
- Pro-apoptotic gene 활성화
- Cell death pathway 진입
Cell Death Decision
세포는 다음 기준으로 생존과 사멸을 결정한다:
Short-term UPR → Survival:
- Adaptation 성공
- ER homeostasis 회복
- 정상 기능 재개
Prolonged UPR → Death:
- Adaptation 실패
- Irreversible damage
- Apoptosis 유도
Rationale
Multicellular organism의 관점에서 보면, 지속적으로 dysfunction을 보이는 세포를 제거하는 것이 더 안전하다. 이런 세포가 계속 존재하면 주변 세포와 비정상적인 상호작용을 하거나 organism 전체에 해를 끼칠 수 있다.
PERK-Mediated Apoptosis
Mechanism:
- Prolonged eIF2α phosphorylation
- Sustained ATF4 translation
- CHOP (C/EBP homologous protein) induction
- Pro-apoptotic protein upregulation
- Mitochondrial apoptosis pathway activation
- Cell death
Negative Feedback과 Termination
UPR의 자기 제한
UPR이 성공적으로 작동하면:
- Misfolded protein 감소
- ER stress 완화
- Sensor protein의 inactivation
- UPR signaling 감소
Phosphatase Expression
UPR은 자신을 종료시키는 factor도 유도한다:
- GADD34 (Growth arrest and DNA damage-inducible protein 34)
- Protein phosphatase 1 (PP1)과 결합
- eIF2α 탈인산화
- Translation 회복
적절한 Timing
너무 빨리 UPR을 끄면 문제가 해결되기 전에 adaptation이 중단된다. 너무 늦게 끄면 불필요한 에너지 소비와 potential cell death risk가 있다. Negative feedback mechanism이 이러한 timing을 최적화한다.
질병과의 연관
Metabolic Diseases
Diabetes:
- β cell의 chronic ER stress
- UPR dysregulation
- Cell death (특히 PERK pathway dysfunction)
- Insulin deficiency
Neurodegenerative Diseases
Alzheimer’s, Parkinson’s:
- Protein misfolding
- Chronic ER stress
- Prolonged UPR activation
- Neuronal death
Cancer
Solid tumors:
- Hypoxia로 인한 ER stress
- UPR activation이 survival 촉진
- Angiogenesis와 metastasis 지원
- Chemotherapy resistance
- Therapeutic target으로 주목
관련 개념
- Quality control of ER protein folding
- Glycosylation-Based Monitoring
- Mannosidase Timer
- ER-associated degradation
- BiP
- Protein folding in ER
- ER stress
Footnotes
-
2021 중간 22번 — UPR 작용기전: BiP가 IRE1/PERK/ATF6에서 해리되면 각각 XBP1 mRNA splicing, eIF2α 인산화(번역 억제), Golgi에서 S1P/S2P 절단 → ATF6 활성화. ER stress 지속 시 apoptosis. 복기 불완전. (선지 미복기) ↩
-
1. 왜 인트론이 남은 채로 나갔나요?
보통의 mRNA는 핵 내에서 Spliceosome에 의해 인트론이 제거되어야만 핵공 복합체(NPC)를 통과할 수 있는 ‘통행증’을 얻습니다. 하지만 XBP1 mRNA는 구조적으로 매우 특이한 루프(Loop) 형태의 인트론을 가지고 있어, 일반적인 핵 내 Splicing 기작을 회피하도록 설계되어 있습니다.
이 미성숙한 상태의 mRNA는 일단 세포질로 **수출(Export)**됩니다. 하지만 이 상태에서는 번역이 제대로 일어나지 않거나, 비활성 상태의 단백질만을 생산하게 됩니다. ↩
-
2023 중간 26번 — ER 기능에 대한 설명 중 틀린 것. ERAD(misfolded 단백질을 세포질로 역위하여 proteasome 분해)는 실제 맞는 내용. 복기 불완전(복기 오류 가능성 있음). ↩