Protein Folding in ER
ER lumen으로 translocation된 단백질은 unfolded polypeptide chain 상태로 들어와 올바른 3차원 구조로 접혀야 한다. 이 과정은 ER lumen의 여러 chaperone과 folding enzyme의 도움을 받는다.
ER의 Folding Environment
산화 환경
- Cytosol보다 더 산화된 환경
- Disulfide bond formation 촉진
- Protein disulfide isomerase (PDI) 활성에 필수
고농도의 Folding Machinery
- Chaperones: 단백질 aggregation 방지
- Folding catalysts: 특정 반응 촉매
- Quality control factors: Folding 상태 감시
주요 Chaperone Systems
1. BiP (Binding Protein)
특성:
- Hsp70 family member
- Major component of ER folding machinery
- ER resident protein (KDEL retention signal)
메커니즘:
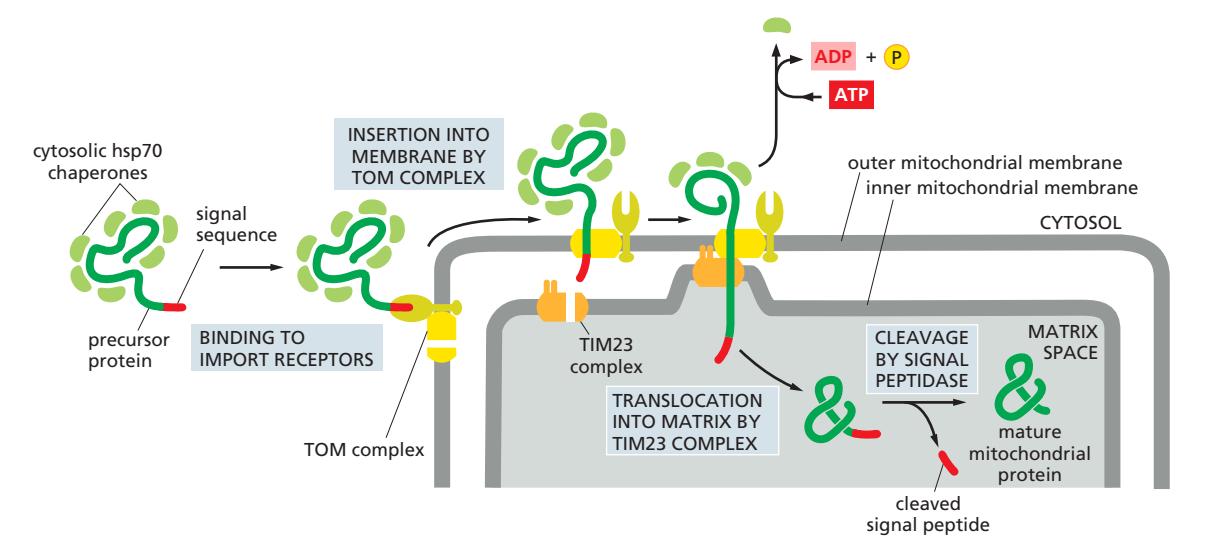
- Recognition: Exposed hydrophobic sequences에 결합
- Prevention of aggregation: 단백질 aggregation 방지
- Retention: 불완전하게 조립된 oligomeric complex를 ER에 유지
- ATP-dependent cycle:
- ATP 결합 → Low affinity state
- ATP 가수분해 → High affinity state
- ADP 방출 → Substrate 방출, 재결합 기회
역할:
- Post-translational translocation에서 pulling motor
- Co-translational translocation의 보조
- Unfolded protein의 일시적 결합
- Protein aggregation 방지
2. Calnexin and Calreticulin
- Ca²⁺-dependent lectin chaperones
- Glycoprotein 특화
- Calnexin and Calreticulin 참조
3. ERp57
- PDI family member
- Calnexin/calreticulin과 협력
- Free sulfhydryl 그룹 인식
- Disulfide bond formation 보조
Folding Catalysts
1. Protein Disulfide Isomerase (PDI)
기능:
- Disulfide bond 형성 촉매
- Incorrect disulfide bond 재배열
- Oxidoreductase 활성 (양방향)
상세 메커니즘:
2. Peptidyl-prolyl Isomerase
- Proline 잔기의 cis-trans isomerization 촉매
- Slow folding step 가속화
- Rate-limiting step 해결
Quality Control System
1. Glycosylation-Based Monitoring
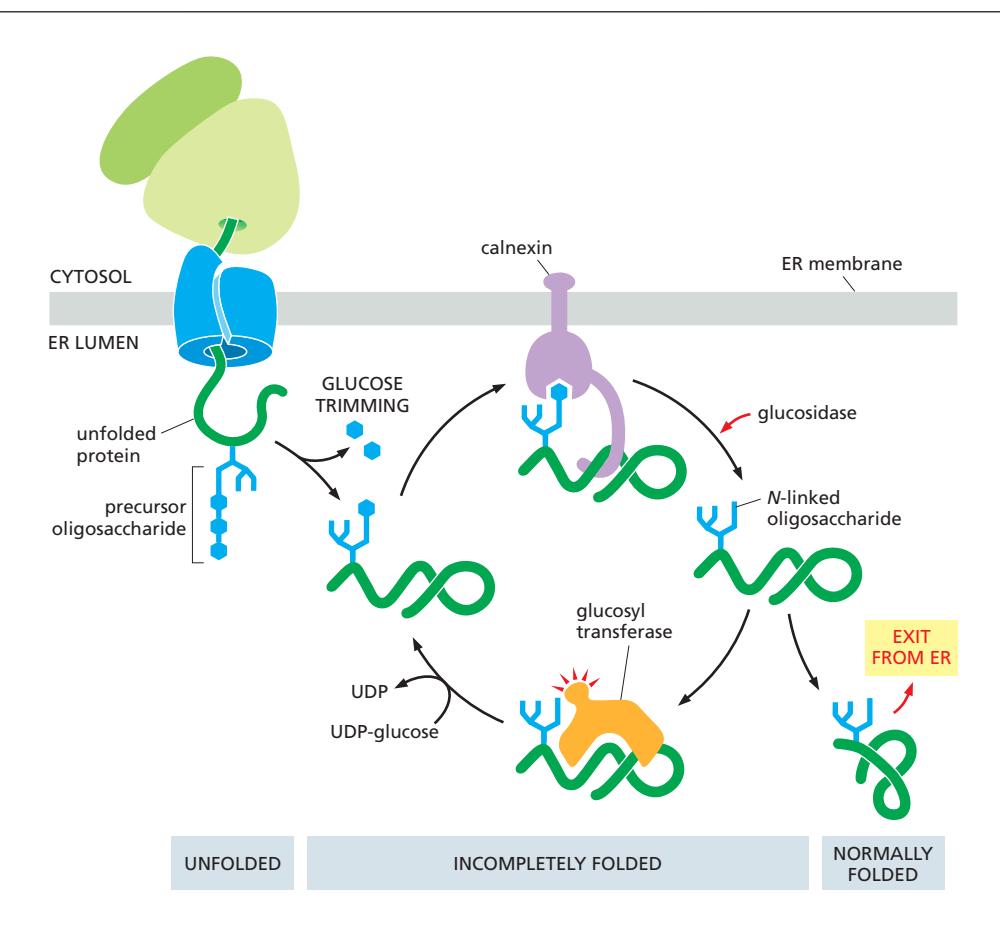
System components:
- Oligosaccharides: Folding 상태 표지
- Glucosidase: Glucose 제거
- Glucosyl transferase: Glucose 재부착
- Calnexin and Calreticulin: 불완전한 단백질 인식
Quality check cycle:
- N-linked oligosaccharide 부착
- 2개의 glucose 제거
- Calnexin/calreticulin 결합→접힐 때 까지 붙잡고 ER 밖으로 못나가게 함.
- Folding 시도
- Glucose 제거 및 방출(잘 접힌 경우)
- Folding 상태 평가:
- Properly folded → Export
- Incompletely folded → glucosyl transferase에 의해 Glucose 재부착, cycle 반복
2. Time-Based Monitoring
Mannosidase system:
- ER에서 머무는 시간 측정
- Terminal mannose 천천히 제거
- Trimmed oligosaccharide = degradation signal
Timer mechanism:
- 빠른 folding → ER 빠져나감
- 느린 folding → Mannose trimming
- 과도한 retention → ER-associated degradation
Folding 실패와 대응
1. ER-Associated Degradation (ERAD)
Trigger:
- Prolonged ER retention
- Trimmed oligosaccharides
- Persistent unfolded regions
Process:
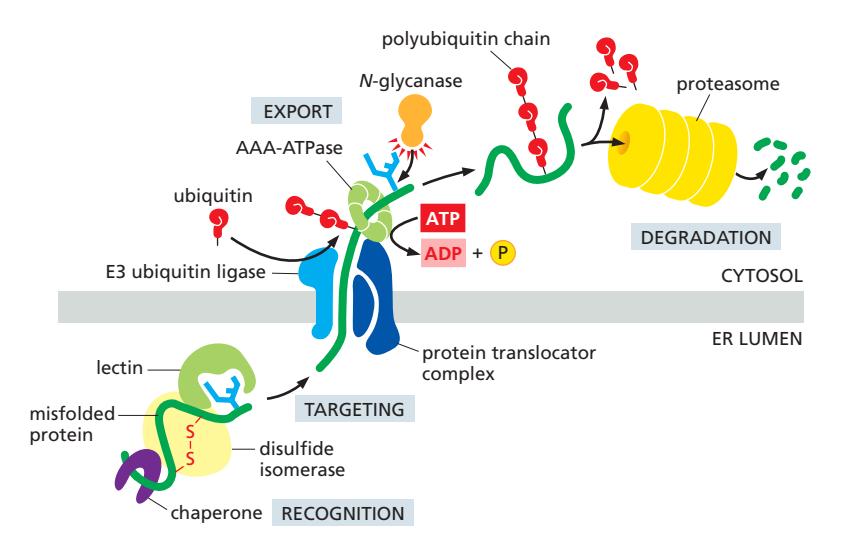
- Misfolded protein 인식
- ER-to-cytosol retrotranslocation
- Deglycosylation
- Ubiquitylation
- Proteasomal degradation
2. Unfolded Protein Response (UPR)
Trigger:
- Misfolded protein 축적
- ER capacity 초과
Response:
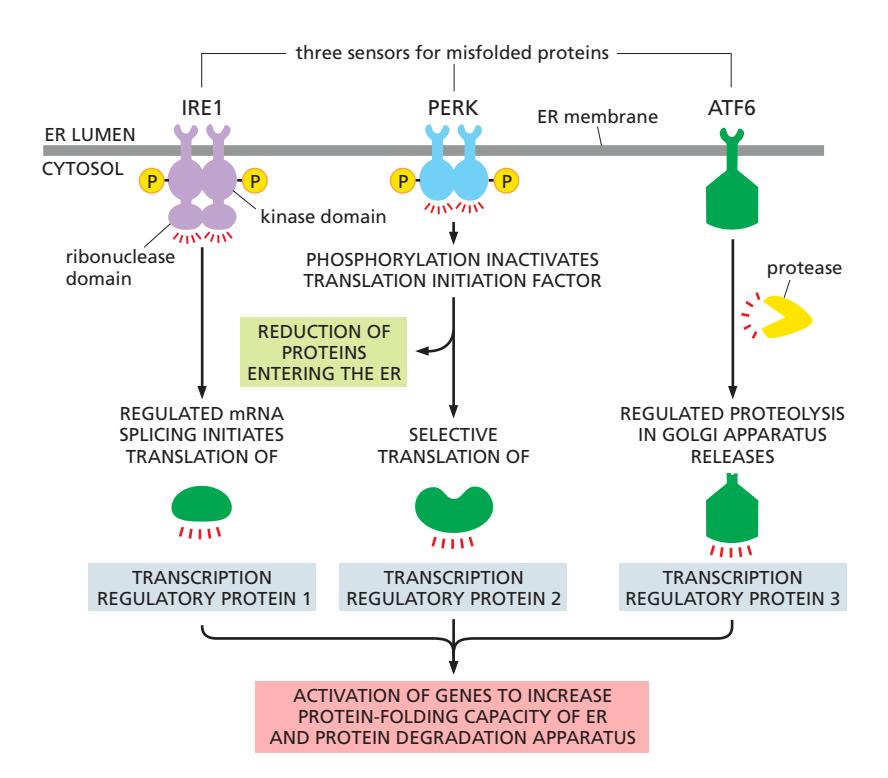
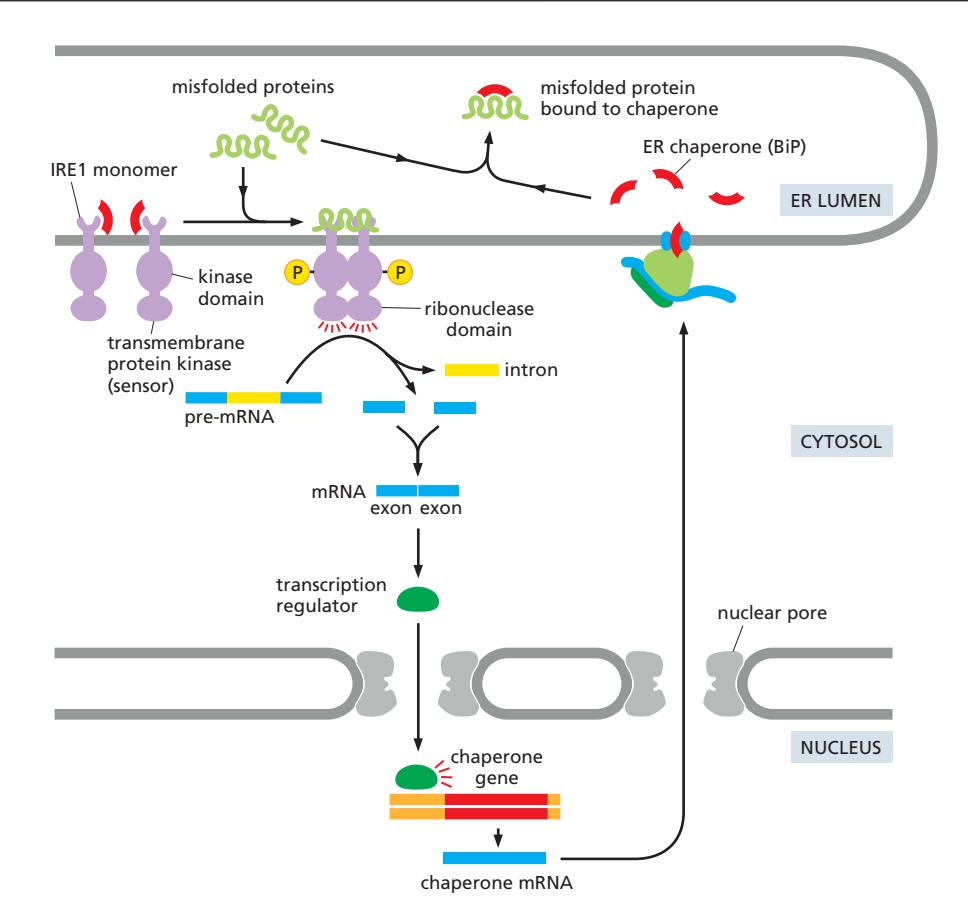
세 가지 pathway:
- IRE1 pathway: mRNA splicing으로 전사인자 활성화
- PERK pathway: Translation 감소, 선택적 전사인자 번역
- ATF6 pathway: Proteolytic cleavage로 전사인자 방출
결과:
- ER chaperone 증가
- ERAD machinery 증가
- ER export factor 증가
- ER expansion
- 지속적 stress → Apoptosis
Folding의 시공간적 조절
Co-translational Folding
- Translocation 중 folding 시작
- Domain-by-domain folding
- Chaperone이 early folding intermediate 포획
Post-translational Folding
- Complete polypeptide chain 후 folding
- Multiple chaperone의 순차적 작용
- Complex protein의 경우 더 긴 시간 필요
Compartment-Specific Folding
- ER lumen의 산화 환경
- High Ca²⁺ concentration
- Abundant chaperones
- Specialized folding catalysts
생리적 중요성
1. Protein Quality
- 올바르게 접힌 단백질만 ER 통과
- Functional protein 생산 보장
- Misfolded protein의 독성 방지
2. Cell Homeostasis
- ER capacity와 demand 균형
- Adaptive response to stress
- Cell survival vs. apoptosis 결정
3. Secretory Pathway Integrity
- Downstream organelle 보호
- Functional complex assembly
- Proper trafficking 보장