Chemiosmotic Coupling
정의
**Chemiosmotic coupling (화학삼투 결합)**은 막을 가로지르는 전자 전달(“chemi”)과 막 수송 과정(“osmotic”)의 연결로 ATP를 합성하는 메커니즘이다.12
“This mechanism is known as chemiosmotic coupling, signifying a link between the chemical bond–forming reactions that generate ATP (‘chemi’) and membrane transport processes (‘osmotic’).” — Chapter 14
미토콘드리아, 클로로플라스트, 세균(archaea + bacteria) 모두 공유하는 근본적인 에너지 변환 메커니즘.
두 단계 과정
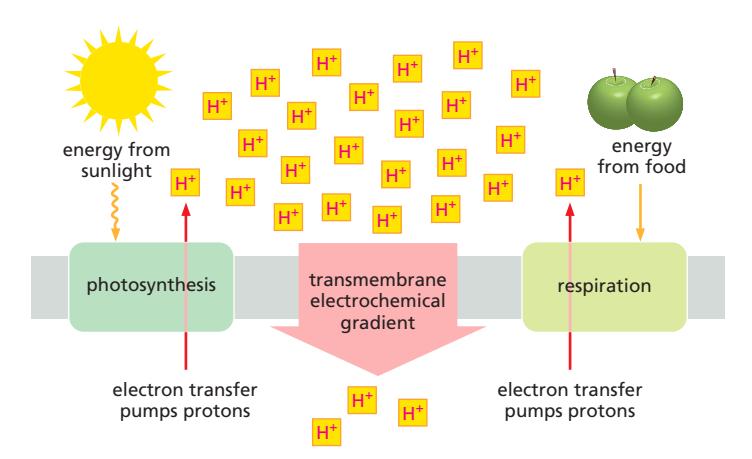 Figure 14-2: Stage 1 - Electrochemical proton gradient 형성.
Figure 14-2: Stage 1 - Electrochemical proton gradient 형성.
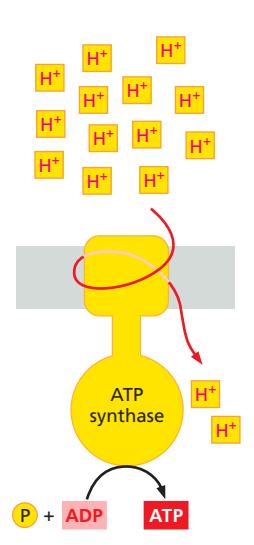 Figure 14-3: Stage 2 - ATP synthase에 의한 ATP 합성.
Figure 14-3: Stage 2 - ATP synthase에 의한 ATP 합성.
Stage 1: Proton Gradient 형성
- 전자(음식물 산화 또는 광에너지에서 유래)가 electron-transport chain을 따라 이동
- 각 전달 단계에서 방출된 에너지 → H⁺를 막을 가로질러 pumping
- Electrochemical proton gradient (proton-motive force, PMF) 형성
Stage 2: ATP 합성
- H⁺가 electrochemical gradient를 따라 ATP synthase를 통해 역류3
- ATP synthase가 이 에너지로 ADP + Pᵢ → ATP 합성
Electrochemical Proton Gradient 구성
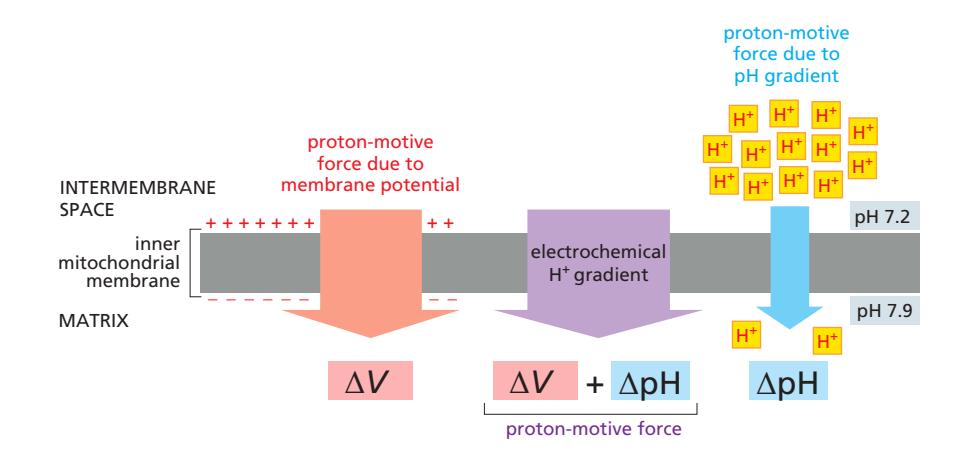 Figure 14-14: 미토콘드리아 inner membrane의 electrochemical proton gradient.
Figure 14-14: 미토콘드리아 inner membrane의 electrochemical proton gradient.
두 가지 성분:
- pH gradient (ΔpH): matrix (pH ~8) > crista space (낮은 pH) → H⁺를 matrix로 당기는 힘
- Membrane potential (ΔV): matrix (-) / crista space (+) → 양전하(H⁺)를 matrix로 당기는 힘
Total proton-motive force ≈ 180 mV (막전위 ~150 mV + pH gradient ~30 mV)
화학삼투의 보편성
세균에서의 응용:
- ATP synthase: 호기성 세균의 plasma membrane에서 동일 기능
- Proton gradient 활용: flagellar motor 회전, 영양소 수송 (symport), Na⁺ 방출
“The existence of such bacteria demonstrates a critical point: the principle of chemiosmosis is more fundamental than the proton-motive force on which it is normally based.” — Chapter 14
일부 호염기성 세균은 H⁺ 대신 Na⁺ 를 사용하여 chemiosmosis 수행.
관련 개념
- Proton pumping
- ATP synthesis
- Electron Transport Chain_MOC
- 미토콘드리아 단백질 수입의 에너지원 — 동일한 H⁺ 막전위가 TIM23을 통한 단백질 수입도 구동함
Footnotes
-
2023 기말 11번 — 전자 이동 시 H⁺가 matrix→IMS로 배출되는 원리(vectorial chemistry, conformational change)와 내막의 비대칭성에 의한 단방향 이동이 서술형 답안의 핵심 내용. ↩
-
2023 기말 12번 — Antimycin A로 Complex III 억제 시 cytochrome c가 환원되지 않아 Complex IV에 전자 공급이 없어지고, O₂ + 4H⁺ → 2H₂O 반응이 멈추어 산소 소비가 감소한다는 서술형 풀이의 핵심 내용. ↩
-
2022 기말 20번 — CCCP(proton uncoupler)가 proton gradient를 ATP 대신 열로 소산시켜 지방 산화를 증가시키는 비만 치료 원리 서술형 문항. ↩