Laminin
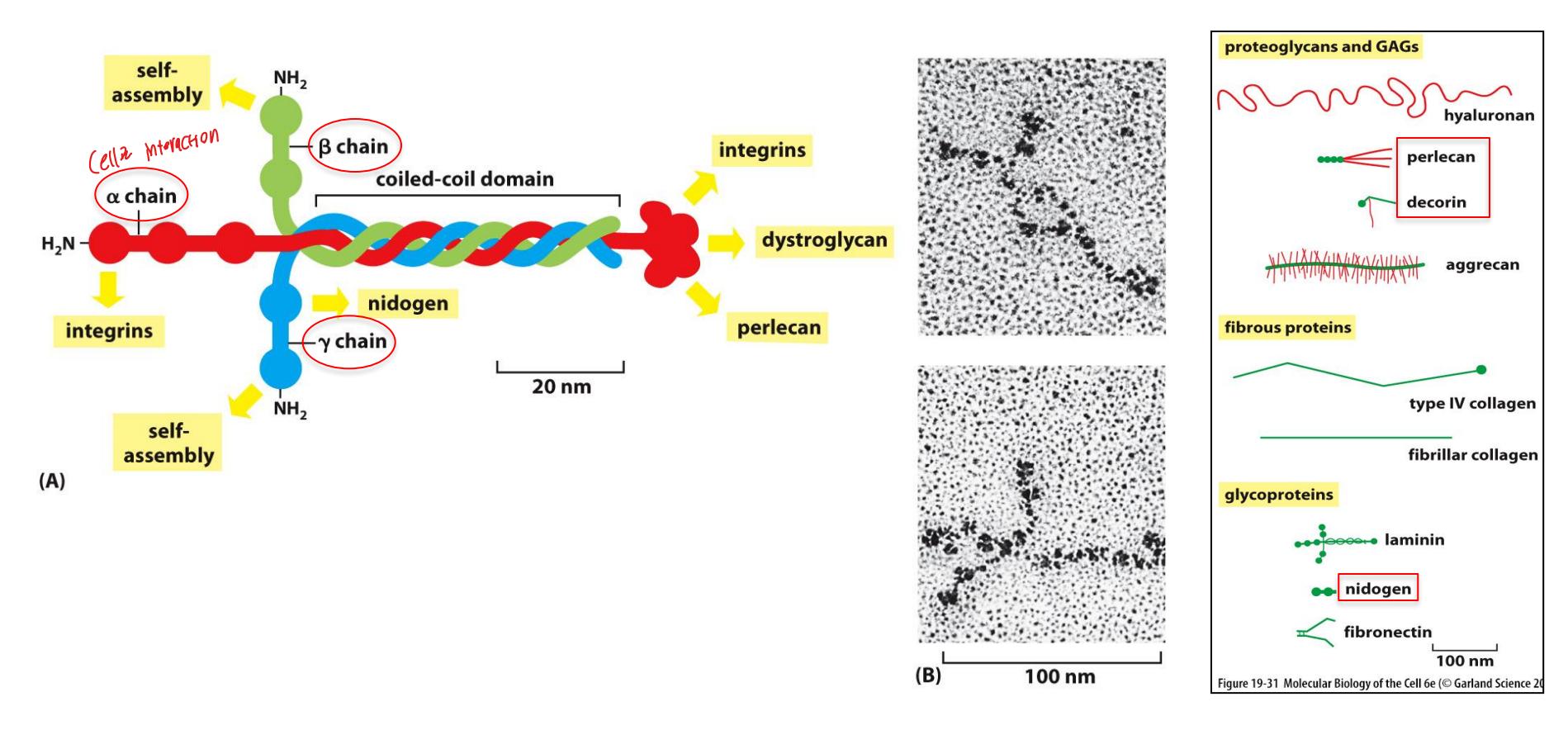 Laminin (glycoprotein)의 구조. α-chain, β-chain, γ-chain으로 구성된 heterotrimeric protein이다.
Laminin (glycoprotein)의 구조. α-chain, β-chain, γ-chain으로 구성된 heterotrimeric protein이다.
Laminin은 basal lamina의 주요 glycoprotein이며, basal lamina의 primary organizer이다.1
구조
- Heterotrimeric protein: 3개의 polypeptide chain (α, β, γ)이 disulfide bond로 연결
- 각 chain은 1500 amino acid 이상
- 비대칭 bouquet 형태: 3개 줄기가 밑에서 꼬여 있고 머리는 분리된 꽃다발 모양
- 여러 isoform 존재:
- α chain 5종류
- β chain 4종류
- γ chain 3종류
- 다양한 조합으로 여러 laminin 생성 가능 (laminin-111, laminin-332, laminin-211 등)
Basal Lamina에서의 역할
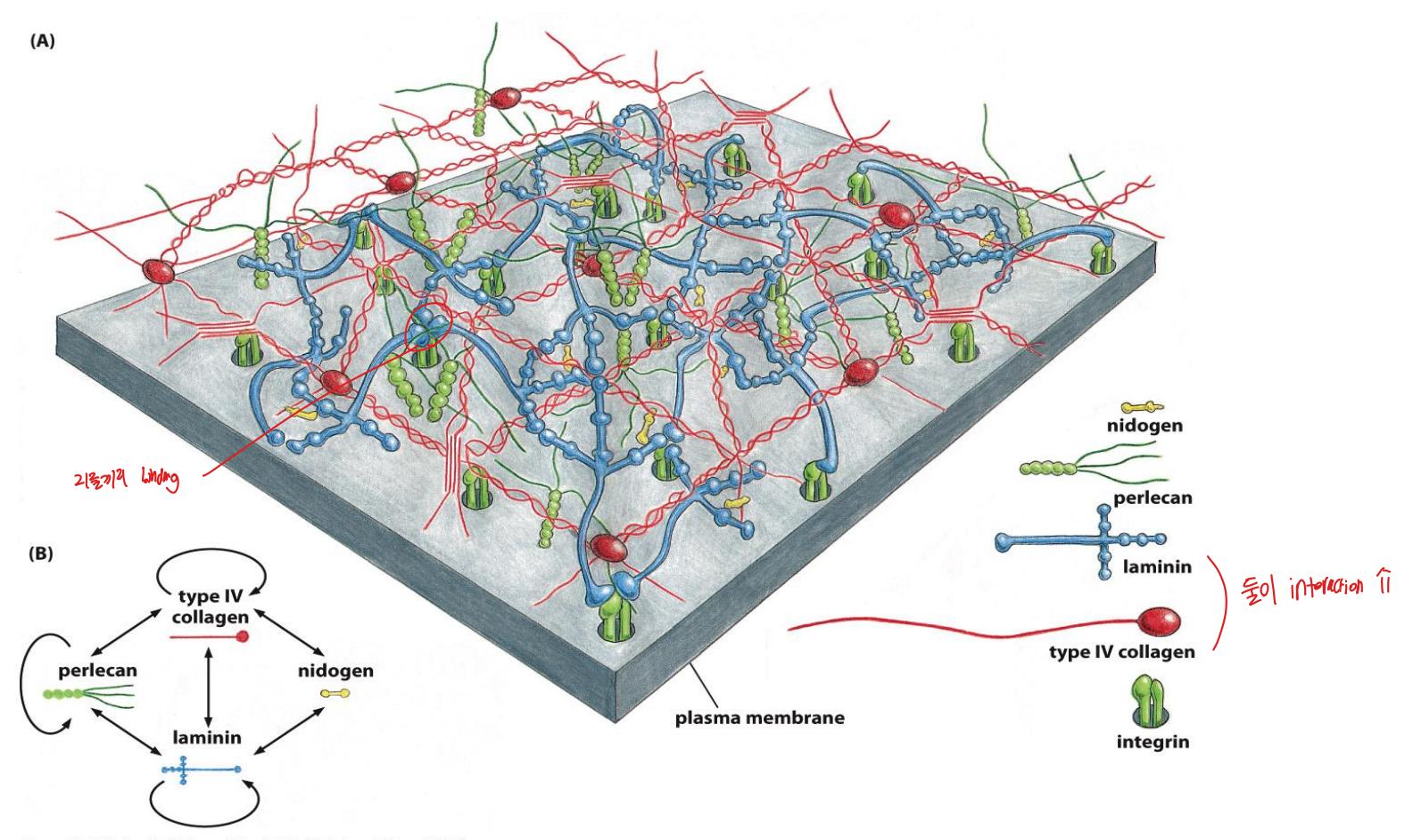 Basal lamina의 분자 구조 모델. Laminin이 type IV collagen, nidogen, perlecan과 상호작용하여 고도로 cross-linked된 단백질 및 proteoglycan network를 형성한다.
Basal lamina의 분자 구조 모델. Laminin이 type IV collagen, nidogen, perlecan과 상호작용하여 고도로 cross-linked된 단백질 및 proteoglycan network를 형성한다.
- 초기 발생 시: Basal lamina는 주로 laminin 분자로 구성된다.
- Laminin 분자들이 in vitro에서 스스로 network로 조립될 수 있다 (주로 머리 부분 상호작용).
- 세포 표면 수용체 (주로 integrin과 dystroglycan)가 laminin을 발로 잡고 있어, 머리가 상호작용하여 2차원 network를 형성하도록 조직한다.
- 이 laminin network가 다른 basal lamina 구성요소들의 조립을 조율한다.
Laminin γ1 chain은 대부분의 laminin heterotrimer의 구성요소이며, 이것이 없는 쥐는 basal lamina를 만들지 못해 배아 발생 중 사망한다.
결합 부위
Laminin은 여러 결합 부위를 가진다:
- Proteoglycan 결합→
- nidogen 결합 → 이 둘이 lamina network와 collagen network를 견고하게 함
- Cell-surface receptor (integrin, dystroglycan) 결합
관련 질환
Laminin 결합 이상은 다음과 같은 질환을 유발할 수 있다:
- Muscular dystrophy (근이영양증)
- Lethal skin blistering disease (junctional epidermolysis bullosa, 치명적 피부 수포 질환)
- Nephrotic syndrome (신장 필터 결함)
특히 피부에서 laminin-332는 skin basal lamina의 핵심 구성요소이며, 이 유전자에 결함이 있으면 epidermis가 dermis에 제대로 부착되지 못해 junctional epidermolysis bullosa (연접부수포성표피박리증)라는 심각한 수포 질환을 유발한다.
Footnotes
-
2023 기말 30번 — laminin이 basal lamina의 primary organizer로서 collagen IV, nidogen, perlecan과 함께 basal lamina 핵심 구성요소임이 정답 근거로 활용됨. ↩