Collagen
Collagen은 fibrous protein의 family로 모든 다세포 동물에서 발견된다. 포유류에서 **전체 단백질 질량의 약 25%**를 차지하는 가장 풍부한 단백질이다.1
구조적 특징
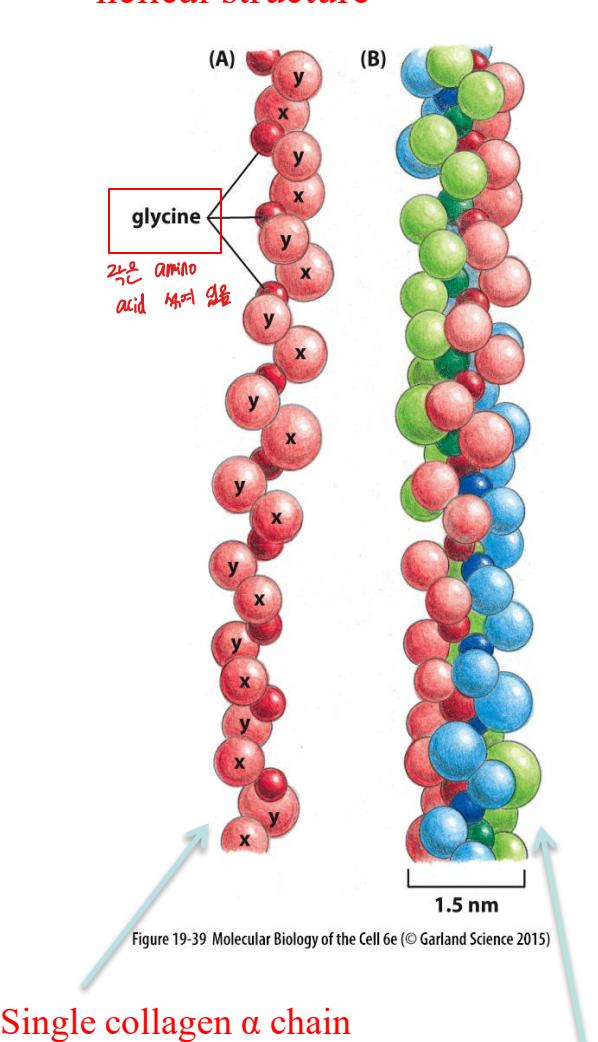
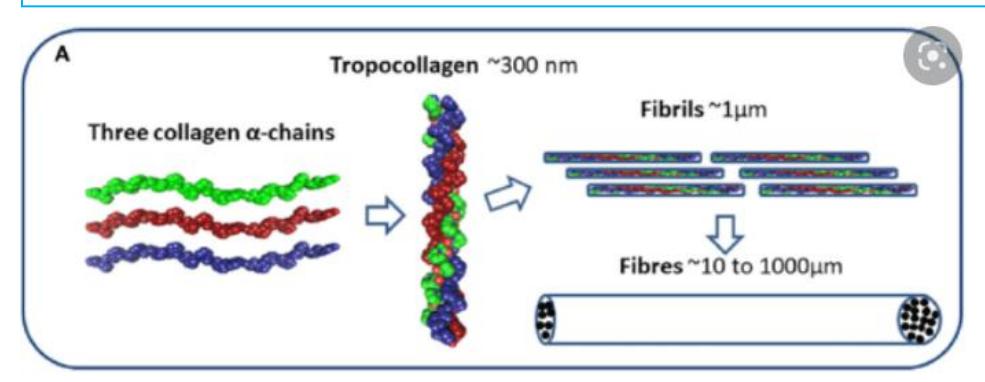 Collagen의 구조. 긴(1000 AA), triple-stranded helical structure. 3개의 amino acid가 한 turn을 이루며, Gly-X-Y triplet 서열을 반복한다.
Collagen의 구조. 긴(1000 AA), triple-stranded helical structure. 3개의 amino acid가 한 turn을 이루며, Gly-X-Y triplet 서열을 반복한다.
- Triple-stranded helical structure: 3개의 collagen polypeptide chain (α chain)이 rope처럼 superhelix를 형성
- 길이: 약 1000 amino acid
- 반복 서열: Gly-X-Y triplet (X는 주로 proline, Y는 주로 hydroxyproline)
- Proline과 glycine이 매우 풍부: Glycine이 매 3번째 아미노산으로 나타나며, 작은 크기 덕분에 3개 사슬이 촘촘히 결합 가능
- 콜라겐은 Hydroxylysine 잔기에 Glucose와 Galactose가 결합하는 당단백질. 이 과정은 콜라겐의 삼중 나선을 안정화하고 섬유 형성을 돕기 위해 꼭 필요.
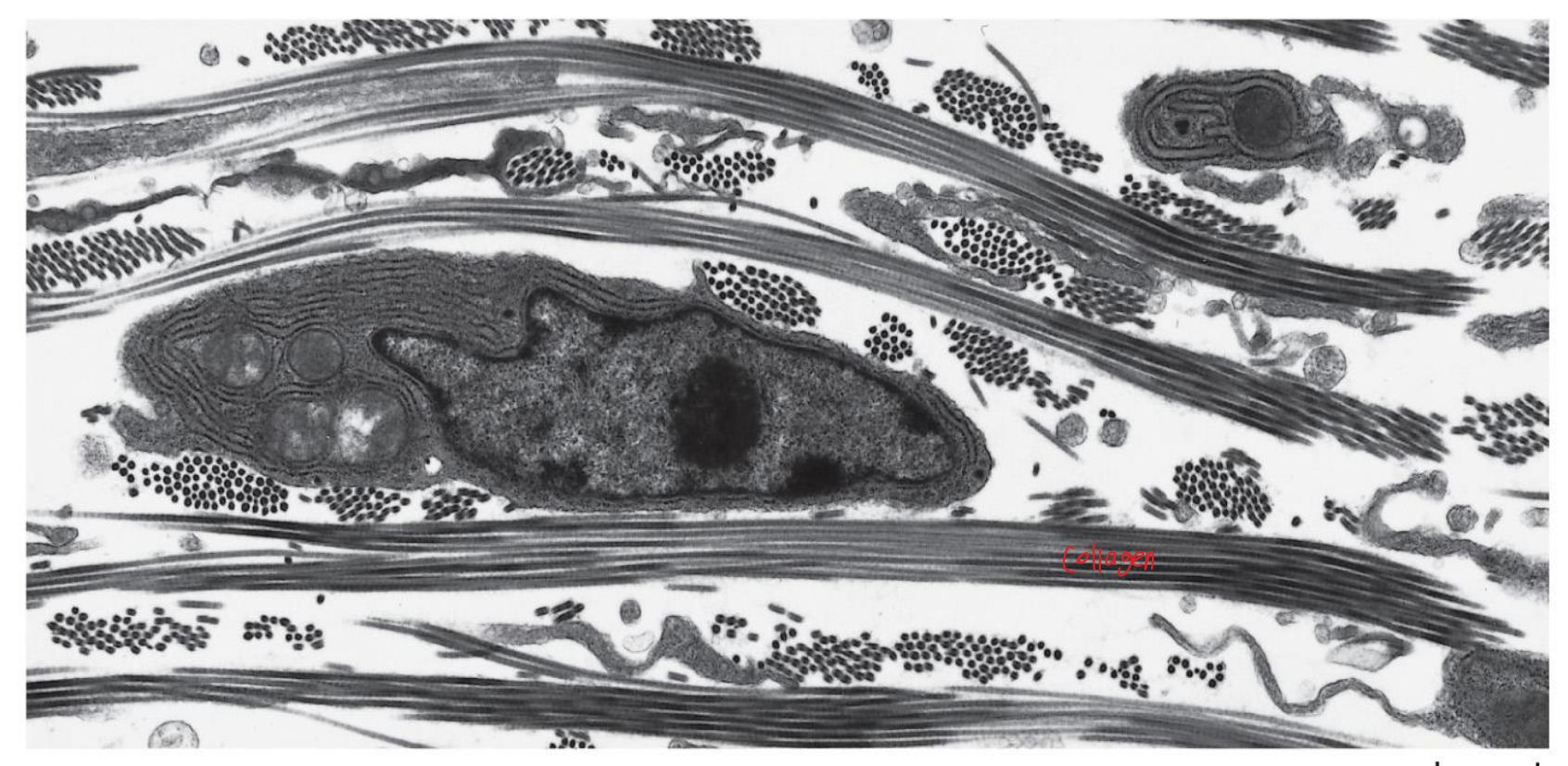 배아 닭 피부 결합조직의 fibroblast를 둘러싼 collagen fibril2. Collagen은 ECM의 구조적 지지를 제공하며, 경직성과 신장 저항성 덕분에 피부, 힘줄, 뼈, 인대에 이상적인 matrix이다.
배아 닭 피부 결합조직의 fibroblast를 둘러싼 collagen fibril2. Collagen은 ECM의 구조적 지지를 제공하며, 경직성과 신장 저항성 덕분에 피부, 힘줄, 뼈, 인대에 이상적인 matrix이다.
Types of Collagen (Table 19-2 기반)
| TABLE 19–2 Some Types of Collagen and Their Properties | ||||
|---|---|---|---|---|
| Type | Polymerized form | Tissue distribution | Mutant phenotype | |
| Fibril-forming (fibrillar) | I | Fibril | Bone, skin, tendons, ligaments, cornea, internal organs (accounts for 90% of body collagen) | Severe bone defects, fractures (osteogenesis imperfecta) |
| II | Fibril | Cartilage, intervertebral disc, notochord, vitreous humor of the eye | Cartilage deficiency, dwarfism (chondrodysplasia) | |
| III | Fibril | Skin, blood vessels, internal organs | Fragile skin, loose joints, blood vessels prone to rupture (vascular Ehlers–Danlos syndrome) | |
| V | Fibril (with type I) | As for type I | Fragile skin, loose joints (classical Ehlers– Danlos syndrome) | |
| XI | Fibril (with type II) | As for type II | Myopia, blindness | |
| Fibril-associated | IX | Lateral association with type II fibrils | Cartilage | Osteoarthritis |
| XII | Lateral association with type I fibrils | Tendons | Skeletal and muscle abnormalities | |
| Network-forming | IV | Sheetlike network | Basal lamina | Kidney disease (glomerulonephritis), deafness |
| VII | Anchoring fibrils | Beneath stratified squamous epithelia | Skin blistering | |
| Transmembrane | XVII | Nonfibrillar | Hemidesmosomes | Skin blistering |
| Proteoglycan core protein | XVIII | Nonfibrillar | Basal lamina | Myopia, detached retina, hydrocephalus |
| 인간 유전체는 42개의 서로 다른 collagen α chain을 암호화하는 유전자를 포함하며, 이들의 다양한 조합으로 약 40가지 타입의 collagen 분자가 형성된다. |
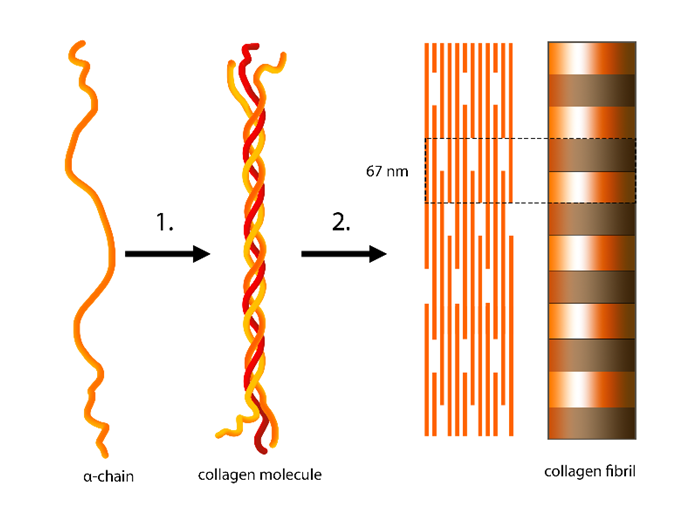
Fibril-forming (Fibrillar) Collagens
분비 경로(ER → Golgi → 세포 표면)를 거쳐 extracellular space로 분비된 후 collagen fibril로 조립되는 collagen들이다.3 Fibril은 직경 10~300 nm, 길이 수백 μm의 얇고 긴 구조이며, 더 큰 cable-like bundle (collagen fiber)을 형성할 수도 있다.
| Type | Tissue Distribution | Mutant Phenotype |
|---|---|---|
| Type I | 뼈, 피부, 힘줄, 인대, 각막, 내부 장기 (체내 collagen의 90%) | 심각한 뼈 결함, 골절 (osteogenesis imperfecta)4 |
| Type II | 연골, 추간판, 척삭, 눈의 유리체 | 연골 결핍, 왜소증 (chondrodysplasia) |
| Type III | 피부, 혈관, 내부 장기 | 약한 피부, 느슨한 관절, 혈관 파열 (Ehlers-Danlos syndrome) |
| Type V | Type I과 함께 fibril 형성 | Type I과 유사 분포 |
| Type XI | Type II와 함께 fibril 형성 | Type II와 유사 분포 |
 |
Fibril-associated Collagens
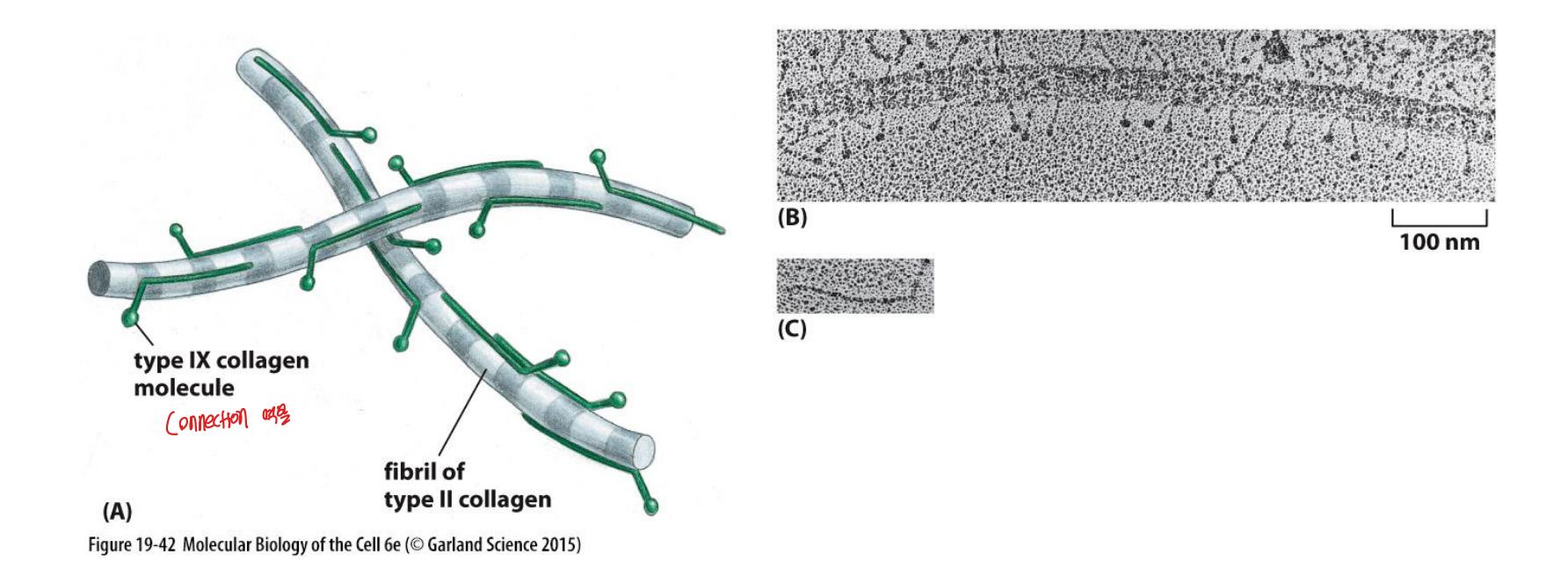 Type IX collagen. Fibril-associated collagen이 collagen fibril 표면에 주기적으로 결합하는 방식.
Type IX collagen. Fibril-associated collagen이 collagen fibril 표면에 주기적으로 결합하는 방식.
Fibril-associated collagen (예: type IX, XII)은 fibrillar collagen과 다른 특성을 가진다:
- 구조적 차이: Triple-stranded helical 구조가 1~2개의 짧은 nonhelical domain에 의해 중단되어, fibrillar collagen보다 유연하다.
- 분비 후 절단 없음: Propeptide를 유지한다.
- Fibril 표면 결합: 스스로 fibril을 형성하지 않고, fibrillar collagen이 형성한 fibril 표면에 주기적으로 결합한다.
- Type IX: Type II collagen fibril (cartilage(연골), cornea(각막), vitreous(유리체)에 결합)
- Type XII: Type I collagen fibril (tendon(힘줄) 등)에 결합
기능: Collagen fibril 간 상호작용, fibril과 다른 matrix macromolecule 간 상호작용을 매개하여 fibril의 조직화를 돕는다.
| Type | Tissue Distribution | Mutant Phenotype |
|---|---|---|
| Type IX | 연골(Cartilage) (Type II fibril에 lateral association) | 골관절염(Osteoarthritis) |
Network-forming Collagens
Fibril이 아닌 sheet-like network를 형성하는 collagen들이다.
| Type | Form | Tissue Distribution | Mutant Phenotype |
|---|---|---|---|
| Type IV | Sheet-like network | Basal lamina | 신장 질환 (glomerulonephritis), 난청 |
| Type VII | Anchoring fibrils | 중층 편평 상피 아래 | 피부 수포 |
Type IV Collagen은 basal lamina의 필수 구성요소이다:
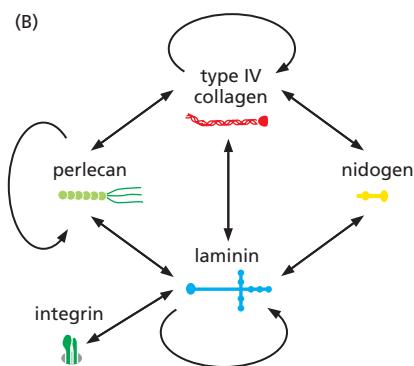 Basal lamina의 분자 구조. Type IV collagen 분자가 terminal domain를 통해 상호작용하여 유연한 felt-like network를 형성한다. 이것이 laminin, nidogen, perlecan과 결합하여 basal lamina에 인장 강도를 부여한다.
Basal lamina의 분자 구조. Type IV collagen 분자가 terminal domain를 통해 상호작용하여 유연한 felt-like network를 형성한다. 이것이 laminin, nidogen, perlecan과 결합하여 basal lamina에 인장 강도를 부여한다.
Type IV collagen은 fibrillar collagen과 달리:
- Triple-stranded helical 구조가 20곳 이상에서 중단되어 여러 번 꺾일 수 있다.
- Terminal domain를 통해 상호작용하여 flexible, sheet-like network를 형성한다.
- Basal lamina에 tensile strength를 제공한다.
Type IV collagen의 돌연변이는 Alport syndrome 같은 신장 질환을 유발한다.
기타 Collagen Types
| Type | Form | Tissue Distribution | Mutant Phenotype |
|---|---|---|---|
| Type XVII (Transmembrane) | Nonfibrillar | Hemidesmosome | 피부 수포 |
| Type XVIII (Proteoglycan core protein) | Nonfibrillar | Basal lamina | 근시, 망막 박리, 수두증 |
Footnotes
-
2023 기말 27번 — fibroblast가 합성하는 collagen이 체내 단백질의 약 25% 차지, COL1A1 돌연변이 → osteogenesis imperfecta(골형성부전증)이 정답 근거로 활용됨. ↩
-
원섬유. ↩
-
2022 기말 22번 — fibroblast 내 collagen 합성(ER-Golgi) 및 세포 외 assembly(propeptide 제거→tropocollagen→fibril→cross-link) 서술형. ↩
-
2022 기말 14번 — Osteogenesis imperfecta 유발 ECM: collagen(COL1A1 돌연변이). 정답 ③. ↩