integrin_MOC
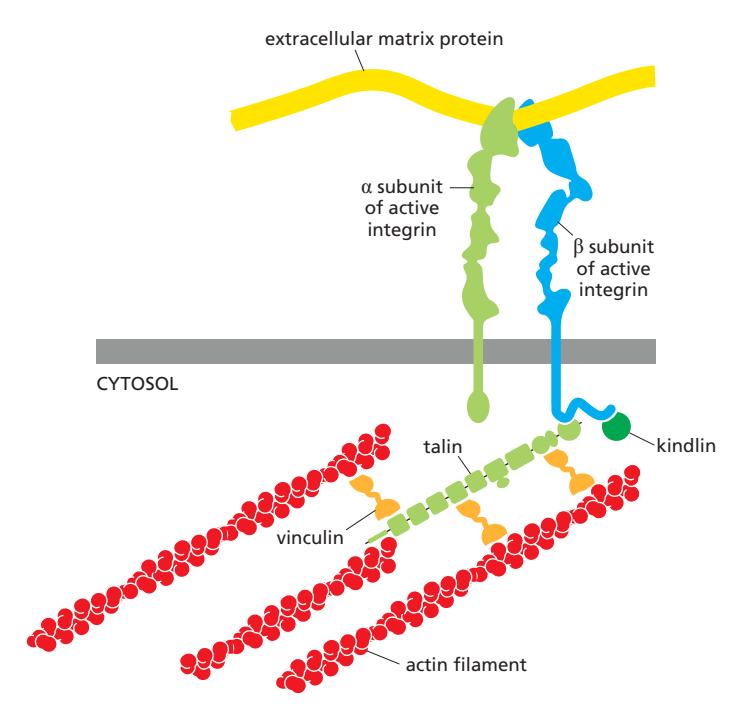 Active integrin 분자의 subunit 구조. Extracellular matrix를 actin cytoskeleton에 연결한다. N-terminal head가 extracellular protein (예: fibronectin)에 부착하고, C-terminal intracellular tail (특히 β subunit)이 adaptor protein과 결합하여 actin filament와 상호작용한다.
Active integrin 분자의 subunit 구조. Extracellular matrix를 actin cytoskeleton에 연결한다. N-terminal head가 extracellular protein (예: fibronectin)에 부착하고, C-terminal intracellular tail (특히 β subunit)이 adaptor protein과 결합하여 actin filament와 상호작용한다.
Integrin은 동물 세포가 extracellular matrix에 결합하는 데 사용하는 주요 cell-surface receptor이다.12 Transmembrane linker로서 ECM과 cytoskeleton을 연결한다.
기본 구조
- Heterodimer: α subunit과 β subunit이 비공유결합으로 결합
- 두 subunit 모두 plasma membrane을 관통하는 glycoprotein
- 짧은 C-terminal tail (intracellular)
- 큰 N-terminal domain (extracellular)
기능
Extracellular Binding
- ECM 단백질의 특정 amino acid sequence motif에 결합
- RGD sequence (Arg-Gly-Asp): fibronectin 등에서 발견되는 주요 결합 motif3
- LDV sequence: 다른 integrin 결합 motif
- Laminin과 collagen의 특정 서열
Intracellular Attachment
- 대부분의 integrin: Actin filament에 연결 (adaptor protein을 통해)
- 특수 integrin (α6β4): Intermediate filament에 연결 (hemidesmosomes)
다양성과 특이성
신호 전달
Integrin은 단순한 기계적 linker가 아니라 양방향 신호 전달 기능을 가진다:
- Outside-in signaling: ECM 결합 → 세포 내부로 신호 전달
- Inside-out signaling: 세포 내 신호 → integrin 활성화 (→ Activation of Integrins by intracellular signaling)45
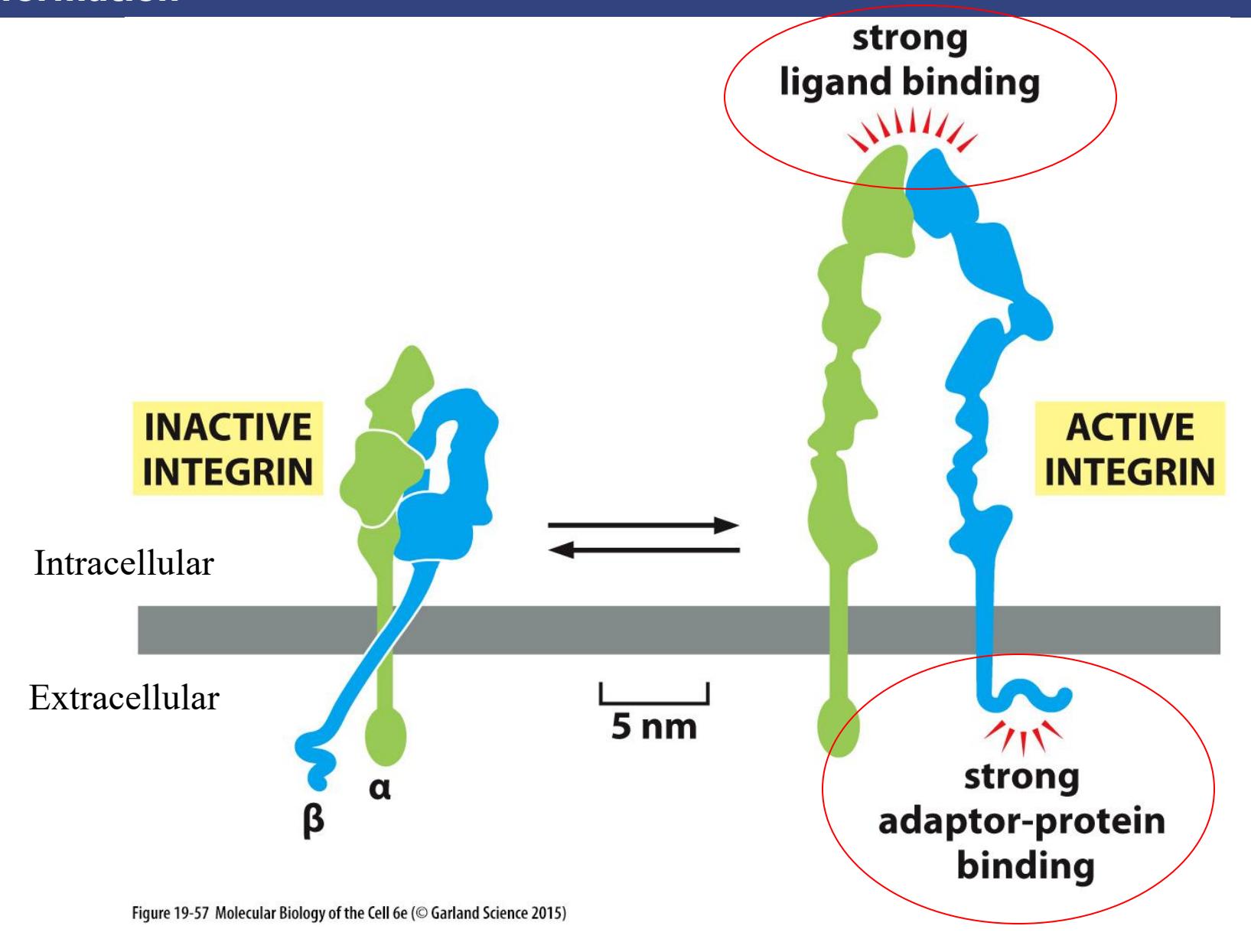 Integrin의 active와 inactive conformation. Inactive (folded) 상태에서 active (extended) 상태로 전환되며, 이 conformational change가 extracellular 및 intracellular binding site를 동시에 노출시킨다.
Integrin의 active와 inactive conformation. Inactive (folded) 상태에서 active (extended) 상태로 전환되며, 이 conformational change가 extracellular 및 intracellular binding site를 동시에 노출시킨다.
세포-세포 상호작용에서의 Integrin6
관련 질환
관련 단백질
하위 항목
- Types of Integrins
- Integrins in Cell-to-Cell interaction
- Activation of Integrins by intracellular signaling
- Glanzmann Thrombasthenia
- Leukocyte Adhension Deficiency
- Related proteins/ (폴더)
Footnotes
-
2022 기말 12번 — ⑤번 선지: focal adhesion(integrin 기반 cell-ECM adhesion)은 desmoglein-3과 무관 (오답). ↩
-
2022 기말 14번 — ①번 선지: integrin은 세포막의 ECM receptor(transmembrane linker)로 ECM 자체가 아님 (오답). ↩
-
2023 기말 28번 — fibronectin RGD(Arg-Gly-Asp) → integrin 결합이 정답 근거로 활용됨. ↩
-
2023 기말 31번 — talin이 integrin β-subunit에 직접 결합하여 actin cytoskeleton과 연결하는 내용이 정답 근거로 활용됨. ↩
-
2023 기말 32번 — inactive integrin(bent/closed, α-β clasp) vs active integrin(extended/open, α-β 분리) 구조 차이가 정답 근거로 활용됨. ↩
-
2022 기말 17번 — WBC extravasation에서 P-selectin(lectin domain)이 rolling 단계를 시작. 정답 ②. ↩