Disulfide Bond Formation
Disulfide bond (S–S bond)는 두 개의 cysteine residue의 sulfhydryl (SH) group 사이에 형성되는 공유 결합이다. 이 결합은 protein을 안정화시켜 혹독하고 가변적이며 chaperone이 없는 세포 외 환경을 더 잘 견딜 수 있게 한다.
ER에서의 Disulfide Bond 형성
Disulfide bond는 주로 Endoplasmic Reticulum lumen에서 형성된다. Extracellular space 또는 secretory와 endocytic pathway의 organelle lumen에 노출되는 protein domain의 거의 모든 cysteine은 disulfide bond를 형성한다.
Protein Disulfide Isomerase (PDI)
**Protein disulfide isomerase (PDI)**는 ER resident protein으로, free sulfhydryl group을 산화시켜 disulfide bond를 형성하는 반응을 촉매한다.
PDI의 메커니즘

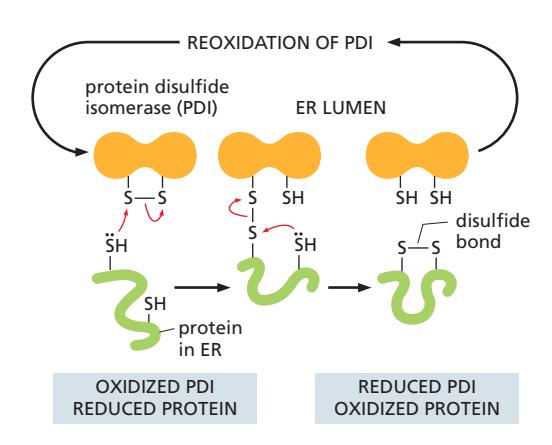
위 그림은 ER에서 disulfide bond가 형성되는 과정을 보여준다.
단계별 과정:
-
초기 상태:
- Substrate protein이 free sulfhydryl (SH) group을 가진 cysteine 포함
- PDI가 intramolecular disulfide bond 보유
-
전자 전달:
- PDI의 disulfide bond가 substrate protein의 free sulfhydryl group으로부터 전자를 받음
- 이 과정에서 PDI와 substrate 사이에 intermolecular mixed disulfide bond 형성
-
Disulfide bond 형성:
- Substrate의 두 번째 free sulfhydryl group이 전자를 mixed disulfide bond에 기부
- 결과: Substrate protein이 산화됨 (disulfide bond 형성)
- PDI는 환원됨 (reduced state)
-
PDI의 재산화:
- 다른 ER enzyme이 reduced PDI를 reoxidize함
- PDI가 다음 cycle을 위해 준비됨
Disulfide Bond의 재배열 (Rearrangement)
Protein이 종종 여러 개의 cysteine을 포함하기 때문에, 처음에는 잘못 pairing될 수 있다. PDI는 이 문제를 해결한다:
기능:
- PDI는 protein의 disulfide bond를 올바르게 folding될 때까지 재배열 (rearrange)함
- 이는 PDI enzyme이 역방향으로 작동하여 immature protein의 잘못 paired된 disulfide를 reduce할 수 있기 때문
Bidirectional activity:
- PDI는 oxidoreductase로 분류됨
- Client protein에서 disulfide bond의 형성 또는 분해를 모두 촉매 가능
PDI Family
ER lumen은 PDI family의 여러 member를 포함한다:
특화된 기능:
- 일부는 disulfide bond를 reducing하는데 특화됨
- 이는 misfolded protein을 완전히 unfold하는데 사용됨
- Unfold된 protein은 degradation을 위해 cytosol로 retrotranslocation됨
ER Lumen의 Oxidizing Environment
Disulfide bond 형성은 ER lumen의 oxidizing environment 유지에 의존한다.
Cytosol과의 대조
Cytosol:
- Reducing environment 유지
- Cytosol에 노출된 domain에서는 disulfide bond가 매우 드물게 형성됨
- Cytosolic domain의 sulfhydryl group은 정상적으로 disulfide bond 형성 안 함
- Reducing environment가 이러한 group을 reduced (–SH) form으로 유지
ER Lumen:
- Oxidizing environment
- Disulfide bond 형성에 유리
생물학적 중요성
Protein 안정화
Disulfide bond는 folded state of protein을 안정화시킨다:
이점:
- Protein이 harsh extracellular environment를 더 잘 견딜 수 있음
- Variable condition에 대한 저항성
- Chaperone-free environment에서의 안정성
Transmembrane Protein에서의 분포
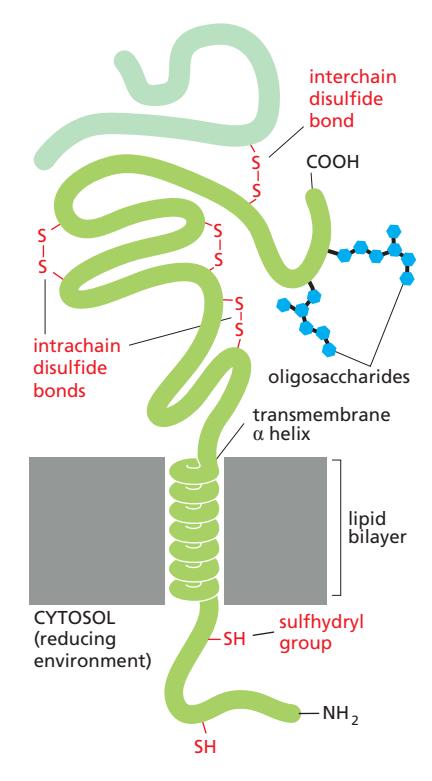
동물 세포의 대부분의 transmembrane protein은 N-linked glycosylation됨:
- Oligosaccharide chain과 disulfide bond가 모두 membrane의 noncytosolic surface에 위치
- Sulfhydryl group이 disulfide bond 형성 (intrachain 또는 interchain)
- Cytosolic domain의 sulfhydryl group은 정상적으로 disulfide bond 형성 안 함
Quality Control에서의 역할
Disulfide bond 형성과 재배열은 Protein folding in ER quality control의 일부이다:
BiP와의 협력:
- BiP (hsp70 family chaperone)와 함께 작동
- Incompletely folded protein 감지
- Protein이 올바르게 fold될 때까지 ER에 retention
Calnexin/Calreticulin과의 협력:
- 일부 ER chaperone (ERp57)은 calnexin 및 calreticulin과 협력
- Free sulfhydryl group 인식 (incomplete disulfide bond formation의 신호)
- Incompletely folded protein을 ER에 retain
Secreted Protein에서의 중요성
Secreted protein과 extracellular domain을 가진 protein의 경우:
- Disulfide bond가 구조적 안정성 제공
- Proteolytic degradation에 대한 저항성 증가
- Functional conformation 유지