Structured Illumination Microscopy (SIM)
개요
회절 한계를 극복하는 첫 번째 superresolution 접근법으로, 약 50 nm의 resolution을 가진 fluorescence imaging 방법이다. 이는 conventional bright-field microscopy의 약 4배 resolution에 해당한다. 광학현미경에 속함.
회절 한계의 극복
Light microscopy의 변형들은 모두 classic diffraction limit에 의해 제약받아 약 0.2 μm(200 nm)까지만 분해능을 가진다(Figure 9-5 참조). SIM은 회절한계를 극복한 것은 아니고 트릭을 사용해 우회했다고 이야기할 수 있다.
SIM의 원리
기본 개념
SIM은 grated 또는 structured pattern의 빛으로 sample을 조명하여 회절 한계를 극복한다. Microscope의 물리적 설정과 작동은 상당히 복잡하지만, 일반적인 원리는 moiré pattern(모아레 패턴) 생성과 유사하게 생각할 수 있다.
Moiré Pattern(모아레 패턴)
Moiré pattern은 서로 다른 각도나 mesh 크기를 가진 두 grids를 겹쳐 만든 interference pattern이다. 조명 grid와 sample features가 결합되어 interference pattern을 만들며, 여기서 grid spacing보다 작은 features가 더 큰 patterns로 변환된다.
Figure 9-27: Structured Illumination Microscopy 원리

(A) 미지의 구조로부터의 pattern: 원래 구조의 pattern을 보여줌 (B) 정의된 grid pattern: 알려진 grid pattern (C) Moiré pattern: 이 둘을 결합하면 resulting moiré pattern이 A(원래 pattern)에서 쉽게 보이는 것보다 더 많은 정보를 포함함
원리: 알려진 pattern(B)이 더 높은 spatial frequencies를 가지면 더 나은 resolution을 얻을 수 있음. 그러나 광학적으로 생성할 수 있는 spatial patterns도 회절 제한을 받기 때문에, SIM은 resolution을 약 2배 정도만 개선할 수 있다.1
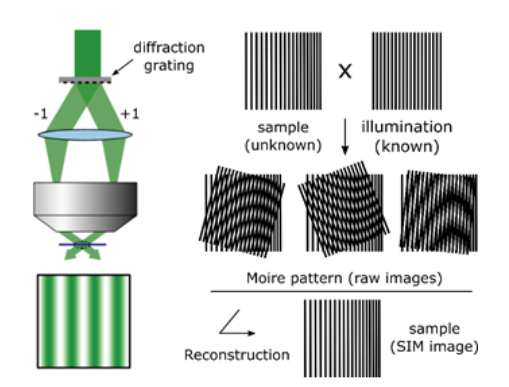
작동 메커니즘
Image Acquisition
Classical limit을 넘어서는 원래 features가 optical system에 의해 imaging될 수 있도록 변환됨. Computer image processing은 이들을 classical limit의 2배까지 resolution을 가진 이미지로 복원할 수 있다.
Grid Illumination 과정
문제: Grid의 dark stripes에 있는 sample 부분은 조명되지 않아 imaging되지 않음 해결: Imaging을 여러 번(일반적으로 3번) 반복. 각 이미지 사이에 grid를 grid spacing의 일부만큼 이동시킴
방향성 고려: Interference effect는 grid bars 방향에 가까운 image components에서 가장 강함. 따라서 모든 방향에서 동등한 enhancement를 얻기 위해 전체 과정을 grid pattern을 일련의 각도로 회전시키며 반복함.
최종 단계: 이 모든 개별 이미지들을 computer로 수학적으로 결합하여 enhanced superresolution image 생성1
SIM의 특징
다양성 (Versatility)
주요 장점: 어떤 fluorescent dye나 protein과도 사용 가능 3D 데이터: 연속적인 focal planes에서 캡처한 SIM images를 결합하여 three-dimensional data sets 생성 가능
Resolution
개선 정도: Conventional light microscopy 대비 약 2배 향상 한계: 광학적으로 생성 가능한 spatial patterns도 회절 제한을 받음
Figure 9-28: SIM을 이용한 3D 데이터 생성

표본: Maize cell의 pachytene 단계 meiotic chromosomes의 three-dimensional projections 염색: Synaptonemal complexes의 paired lateral elements를 보여줌
(A) Conventional Fluorescence Microscopy: Chromosome set이 cohesin에 대한 fluorescent antibody로 염색됨. 두 lateral elements 사이의 거리가 약 200 nm(회절 한계)이기 때문에 각 complex를 구성하는 두 lateral elements가 분해되지 않음.
(B) 3D SIM Image: 향상된 resolution으로 각 lateral element(약 100 nm 폭)를 명확히 분해할 수 있으며, 각 개별 쌍의 두 chromosomes가 서로 coil하는 것을 볼 수 있음.
(C) 색상 추적: 전체 nucleus에 대한 complete three-dimensional data set이 가능하므로, 각 개별 chromosome 쌍의 경로를 추적하고 인위적으로 다른 색상을 할당할 수 있음.
다른 Superresolution 기술과 비교
vs Confocal Microscope: Confocal은 회절 한계 내(200 nm), SIM은 약 100 nm resolution vs STED: STED는 약 20 nm resolution 가능하지만 특수한 photoswitchable probes 필요 vs PALM/STORM: 이들도 약 20 nm resolution이지만 더 긴 acquisition time과 특수 probes 필요
응용 분야
Chromosome Structure: Meiotic chromosomes의 synaptonemal complexes (Figure 9-28) Cell Biology: 회절 한계보다 작지만 10 nm까지는 아닌 구조들 Live Cell Imaging: 다른 superresolution 기술보다 빠른 imaging Tissue Imaging: 두꺼운 표본에서 3D reconstruction
기술적 고려사항
Grid Pattern: 적절한 spatial frequency 선택 각도와 위상: 여러 각도와 위상에서 imaging 필요 Computational Power: 복잡한 image reconstruction 알고리즘 Illumination 균일성: 균일한 grid pattern 조명 필요
요약
핵심 원리: Structured illumination과 moiré effect를 이용하여 회절 한계 극복, 약 2배 resolution 향상 주요 특징: 모든 fluorescent probes 사용 가능, 3D imaging 가능, 살아있는 세포에 적용 가능 Resolution: 약 100 nm (conventional의 2배) 응용: Chromosome structure, subcellular organelles, living cell dynamics 한계: 제한된 resolution 향상, 복잡한 image processing, photobleaching
참고 문헌
Chapter 9: Visualizing Cells and Their Molecules, Section: “Superresolution Fluorescence Techniques Can Overcome Diffraction-limited Resolution”, Related Figures: 9-27, 9-28, Related concepts: deconvolution, Confocal Microscope
Footnotes
-
2023 중간 14번 — 선지 ②(SIM은 공간 패턴으로 회절 한계에서 벗어날 수 있다) 오답 근거: SIM은 약 2배 향상에 그치며 회절 한계를 완전히 벗어나지 못함. 선지 ④(SIM은 한 번의 빛 조사로 고해상도 이미지 획득) 오답 근거: 여러 각도/위상으로 반복 촬영 후 수학적 결합이 필요. ↩ ↩2