Chapter 13-2: Intracellular Membrane Traffic 정리본
6주차 강의노트 기반 | 출처: chapter 13 강의 II 2026.pdf
1. Lysosome
Lysosome은 세포 내 소화의 주요 장소이다.
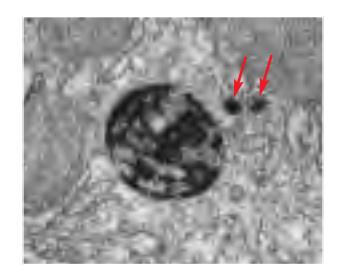
구조적 특징
- 내부 pH ~4.5–5.0 유지 (강산성)
- **V-type ATPase (H⁺ pump)**가 ATP hydrolysis 에너지로 H⁺를 lumen으로 펌핑
- 막 단백질은 대부분 highly glycosylated → lysosomal protease로부터 보호
- Transport 단백질: 분해 산물(amino acid, sugar, nucleotide)을 세포질로 운반
Lysosomal Hydrolase
- 산성 환경(pH 4.5–5.0)에서 최적 활성
- Hydrolase가 cytosol로 방출되더라도 중성 pH(~7.2)에서는 활성이 낮아 세포 손상 제한
- 종류: protease, lipase, nuclease, glycosidase 등
Lysosome의 형태적 다양성
전형적인 “classical” lysosome은 내용물이 거의 소화된 후 남은 잔류물만 포함한 상태이다.
2. Lysosomal Hydrolase 수송: M6P Receptor System
M6P receptor system은 TGN에서 lysosomal hydrolase를 endosome으로 전달하는 가장 잘 이해된 sorting 메커니즘이다.
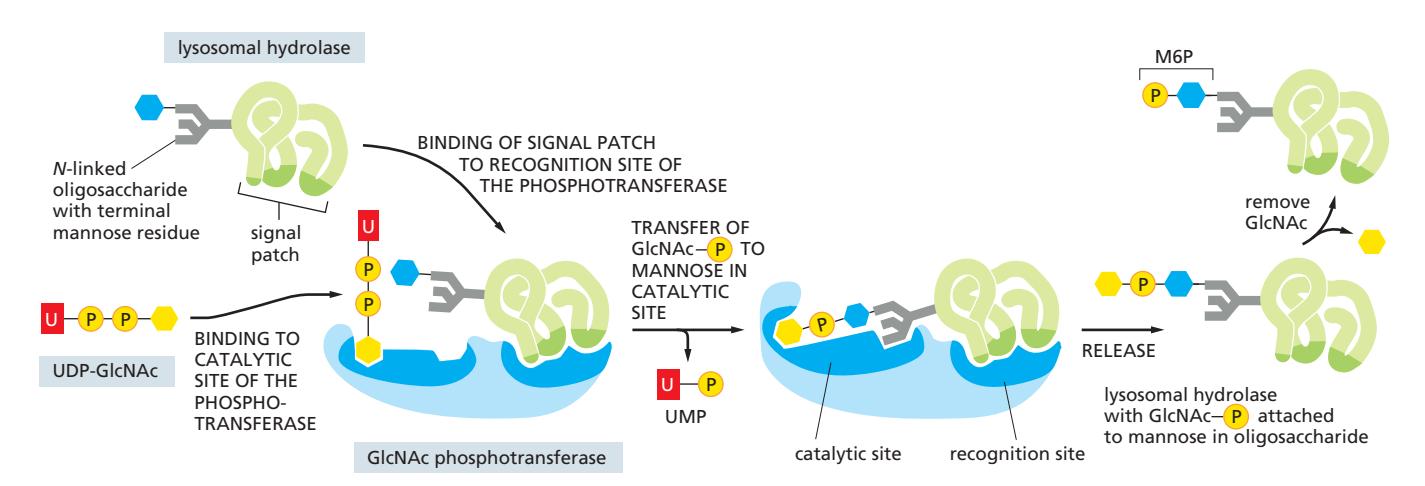
M6P Tag의 부착
- Cis Golgi network에서 GlcNAc phosphotransferase가 lysosomal hydrolase의 N-linked oligosaccharide를 인식
- Two-step modification → Mannose-6-phosphate (M6P) 노출
- 각 hydrolase에 multiple M6P tag 부착 → M6P receptor에 high affinity
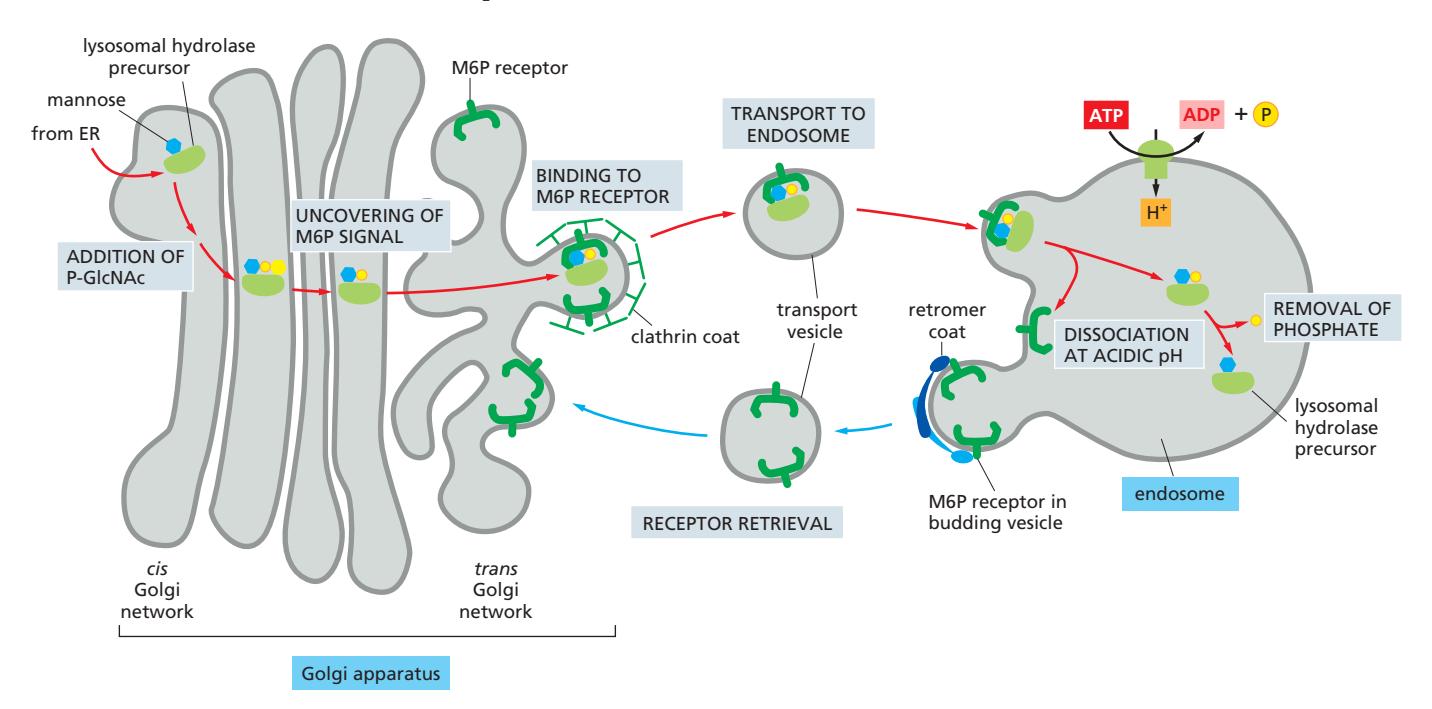
M6P Receptor의 역할
- Transmembrane protein (TGN에 위치)
- Lumen 쪽에서 M6P group 인식 → lysosomal hydrolase 결합
- Cytosolic 쪽에서 clathrin coat의 adaptor protein 결합
- Clathrin-coated vesicle로 hydrolase packaging
pH-dependent 결합
| 구획 | pH | M6P receptor 상태 |
|---|---|---|
| TGN | 6.5–6.7 | M6P에 강하게 결합 |
| Early endosome | ~6.0 | M6P로부터 방출 |
Receptor 재활용
- Endosome의 낮은 pH → hydrolase가 receptor에서 분리
- M6P에서 phosphate 제거 (hydrolase가 receptor와 함께 TGN으로 돌아가지 않도록)
- 빈 M6P receptor → retromer-coated vesicle로 회수 → TGN 복귀
- M6P receptor 재사용
KDEL receptor (COPI vesicle) vs. M6P receptor (clathrin/retromer vesicle): 같은 pH-sensitive 원리이지만 다른 coat 사용
Lysosomal Storage Disease
I-cell Disease (Inclusion-cell Disease)
I-cell disease는 가장 심한 형태의 lysosomal storage disease이다:
- 원인: GlcNAc phosphotransferase 결함 → M6P tagging 불가
- 결과: Lysosomal hydrolase가 lysosome으로 배달되지 않고 혈액으로 분비됨
- Lysosome에 거의 모든 hydrolytic 효소 결여
- 소화되지 않은 기질이 축적 → lysosome이 큰 inclusion 형성 (효소 없는 쓰레기 vesicle)
- 모든 기관계 영향, 개인은 6–7세를 넘기지 못함
- Hepatocyte는 M6P-independent pathway를 가져 예외적으로 정상 작동
Hurler’s Disease
Hurler’s disease는 I-cell disease와 달리 개별 lysosomal hydrolase의 structural gene mutation으로 발생:
- 특정 유형의 glycosaminoglycan (GAG) chain을 분해하는 데 필요한 lysosomal 효소가 결함적이거나 결여됨
- 해당 효소만 기능하지 않아 GAG 분해물이 lysosome에 축적
- I-cell disease와 달리 특정 효소 하나의 결함 (M6P tagging 자체는 정상)
3. Endosome Maturation
Endosome maturation은 early endosome이 시간이 지나면서 late endosome으로 변화하는 과정이다.
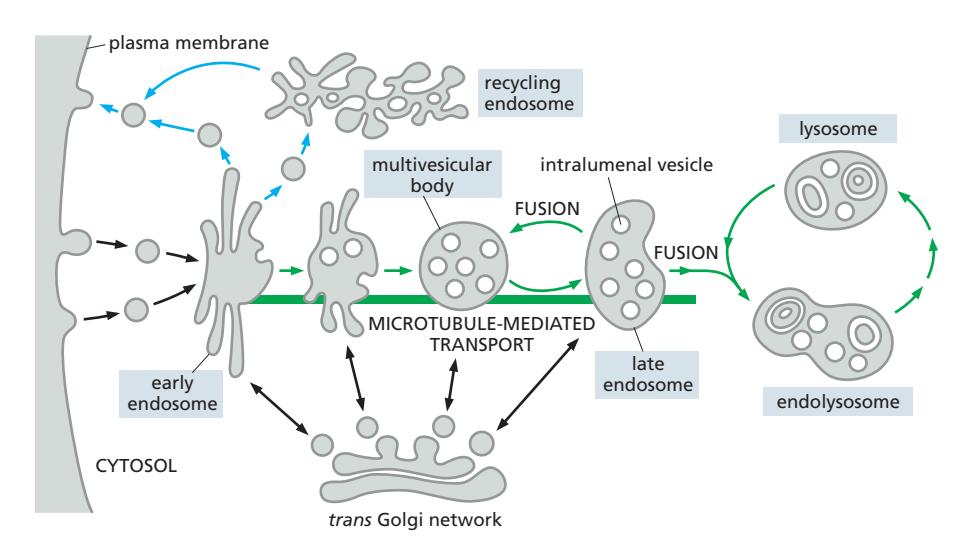
과정
Early endosome (pH ~6.0):
- Tubular + vacuolar domain 보유
- 약 10분간 들어오는 endocytic vesicle 수용
- Tubular domain: 대부분의 membrane 표면 / Vacuolar domain: 대부분의 부피
Maturation 단계별 변화:
- 형태 변화: Tubular domain이 plasma membrane으로 재활용 / Vacuolar domain 수정
- 이동: Dynein motor에 의해 microtubule을 따라 핵 쪽으로 이동
- Lysosome 단백질 전달: TGN에서 새로 합성된 lumenal hydrolase + V-type ATPase 전달
- Acidification: V-type ATPase가 H⁺ pump → organelle이 더욱 산성화 → hydrolase 점점 활성화
- Intralumenal vesicle 형성: Endocytosed signaling receptor가 내부 vesicle로 격리 → receptor signaling 정지
Rab5→Rab7 전환Rab Cascades
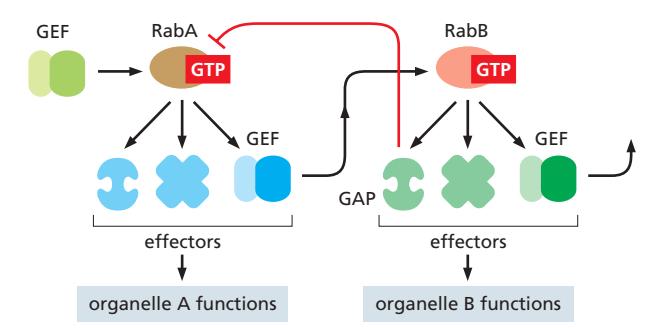
- 시간이 지남에 따라 Rab5-associated patch → Rab7-associated patch로 교체
- Early endosome (Rab5) → Late endosome (Rab7)
- Rab7 effector 세트가 Rab5 effector와 달라 organelle 성질 변화
- 일방향적이고 비가역적: Rab의 자기증폭 특성으로 역전 불가
Lysosome-Late Endosome Cycle
Lysosome은 late endosome과 융합하여 endolysosome이 되고, 분해가 끝나면 다시 lysosome이 되는 cycle 형성.
따라서 lysosome과 late endosome/endolysosome은 명확히 구분하기 어려운 연속적인 변화 과정.
- 내용물이 분해되는지 여부는 pH 차이에 따라 결정
4. Multivesicular Body (MVB)와 ESCRT
ESCRT complex가 intralumenal vesicle (ILV) 형성을 담당한다.
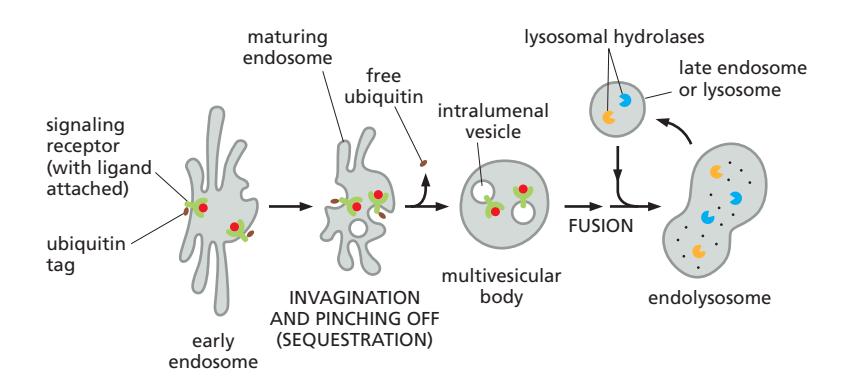
Multivesicular Body
Endosome이 성숙함에 따라:
- 막의 patch가 endosome lumen으로 invaginate
- Pinch off하여 intralumenal vesicle (ILV) 형성. Exosome이라고도 불림
- 세포간 신호로 작용하거나 약물 전달 경로에 이용되기도 함
- Receptor의 cytosolic face의 signal을 차단하기 위함
- 이러한 endosome을 **Multivesicular Body (MVB)**라고 함
- ESCRT (Endosomal Sorting Complex Required for Transport) protein complex에 의해 생성
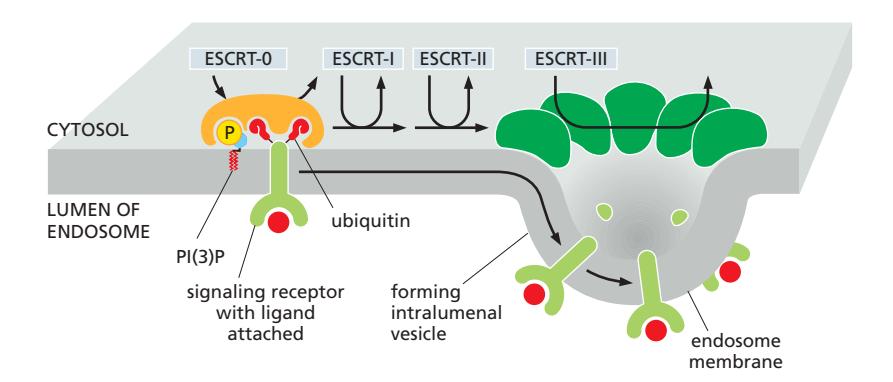
ESCRT의 순차적 작용
- ESCRT-0: Ubiquitin tag + PI(3)P 동시 인식 → 막에 처음 결합, cargo를 다음으로 전달
- ESCRT-I: cargo 받아 ESCRT-II로 전달
- ESCRT-II: cargo를 특정 막 영역에 농축, ESCRT-III 모집
- ESCRT-III: 막에 multimeric assembly 형성 → 막 bend → invagination 매개
ESCRT docking 요구사항: PI(3)P + ubiquitylated cargo 단백질 둘 다 필요
Ubiquitin 제거: Intralumenal vesicle이 닫히기 전에 ubiquitin marker를 제거 → 세포질로 반환하여 재사용
막 굴곡의 방향
ESCRT가 추진하는 ILV budding은 막의 cytosolic 표면에서 멀어지는 방향으로 발생
- 이는 Clathrin coat의 방향과 반대 (clathrin은 cytosolic 쪽으로 구부림)
Late endosome → lysosome 융합 후 ILV 내 ubiquitinated receptor 분해
5. Retrieval Pathway (Endosome에서)

Early endosome의 tubular extension에서 transport vesicle이 budding:
- 선택된 막 단백질 회수 → plasma membrane으로 반환
- 직접 반환 또는 recycling endosome을 거쳐 반환
6. Endocytosis의 종류
Endocytosis는 plasma membrane 성분, fluid, 용질, 거대분자를 흡수하는 과정이다.
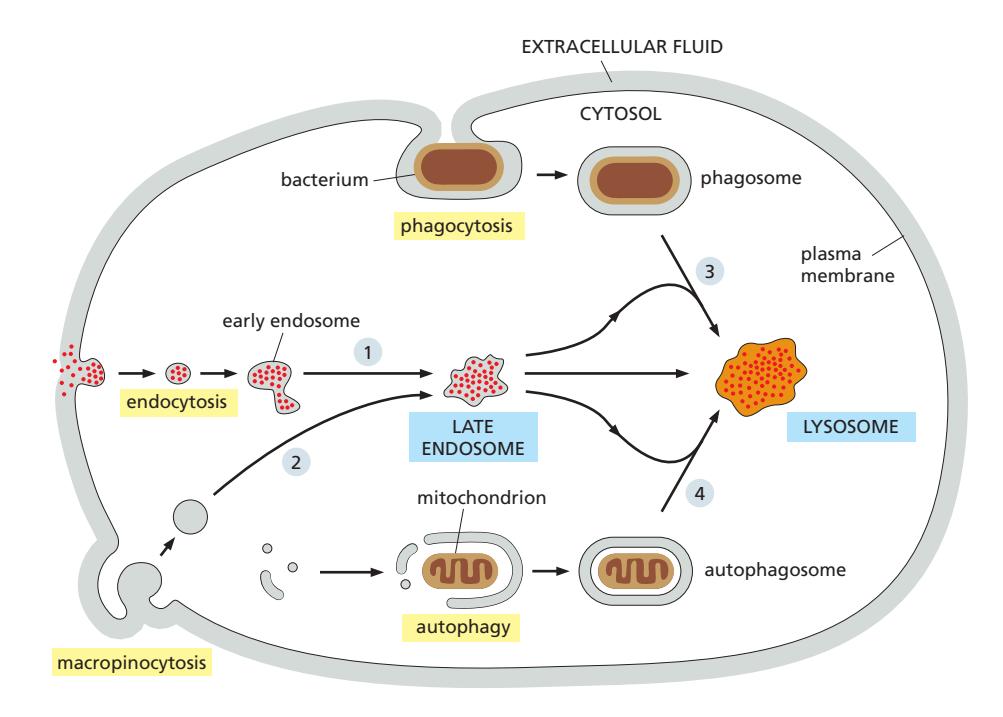
Pinocytosis의 종류
(1) Clathrin-mediated Endocytosis
- 가장 흔한 형태
- Clathrin-coated pit → coated vesicle → coat shed → early endosome 융합
- 배양 fibroblast: 분당 ~2500개 coated vesicle 생성
- Clathrin-coated pit: 총 plasma membrane의 약 2% 차지, 수명 ~1분
(2) Caveolar Endocytosis
Caveolae는 clathrin-independent membrane invagination이다.
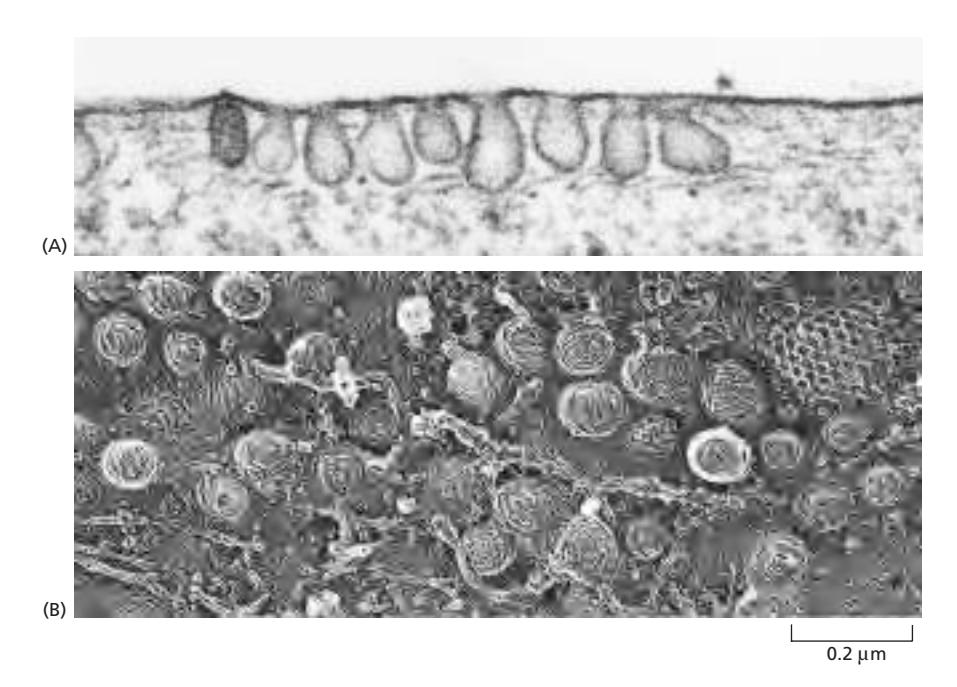
- Caveolae: flask 모양의 invagination
- 구성: Cholesterol + Glycosphingolipid + GPI-anchored protein → lipid raft 유형
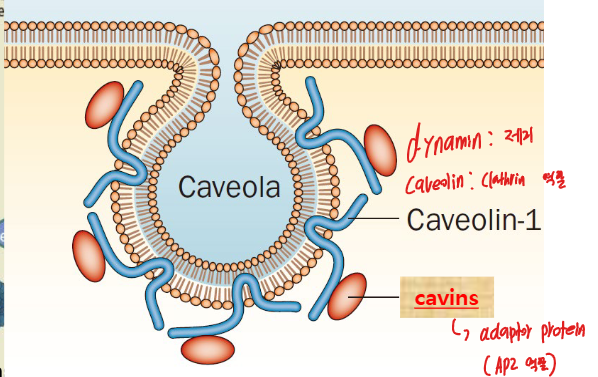
- Caveolin (coat protein): 특이한 integral membrane protein; hydrophobic loop을 cytosolic 쪽에서 막에 삽입 (막을 가로지르지 않음)
- Cavin (adaptor protein): caveolin에 결합하여 구조 안정화
- 일반적으로 정적 구조 (extra plasma membrane의 저장소)
- 기계적 힘 시: cavin scaffold 빠른 disassembly → 막 표면적 일시적 증가
(3) Macropinocytosis
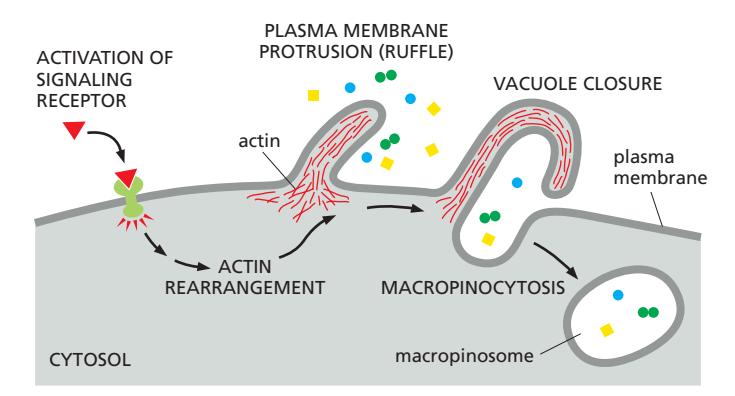
- Macropinocytosis: plasma membrane이 돌출하여 주변 세포외 fluid를 macropinosome으로 둘러싸는 과정
- Clathrin-independent endocytosis
- 비선택적 과정: 세포외 fluid와 그 안의 거대분자·입자를 비특이적으로 trap
- Macropinosome에 receptor가 포함되지 않음 → receptor recycling 불필요
- Actin reorganization으로 membrane ruffling이 일어나며 fluid를 삼킴
형성 과정:
- Cell-surface receptor 활성화 (growth factor, integrin ligand 등)
- Actin polymerization → membrane ruffle 형성
- Ruffle의 끝이 서로 또는 세포막과 융합 → macropinosome 형성
분해 경로:
- Macropinosome은 재활용 없이 오직 분해만 진행
- Acidification → late endosome 또는 endolysosome과 융합
- Ras oncogene 활성화에 의해 자극 → 암세포에서 증가 (영양소 획득)
7. Receptor-mediated Endocytosis: LDL 사례
Receptor-mediated endocytosis는 특정 ligand를 선택적으로 농축하여 흡수하는 효율적 경로이다.
Selective Concentrating Mechanism
- Clathrin-coated pit 자체가 receptor에 연결된 AP2가 모여 형성되므로 receptor가 농축
- 특정 ligand의 내재화 효율을 100배 이상 증가
- 세포외 fluid의 minor component도 대량 흡수 가능
LDL Receptor의 작동
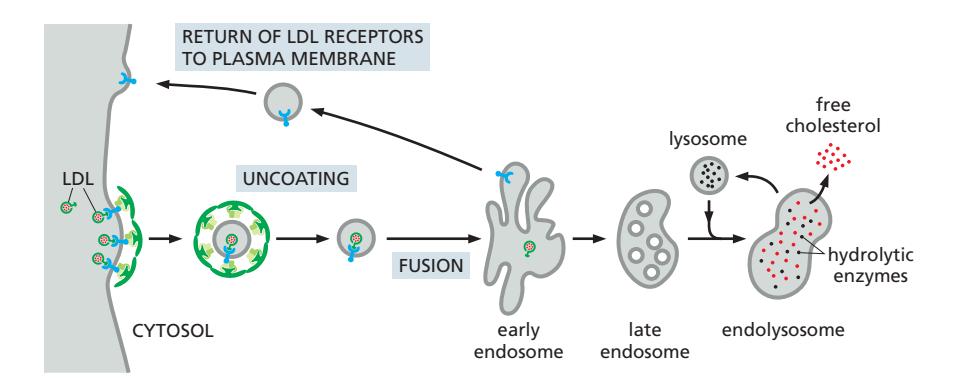
- LDL receptor: plasma membrane에 존재
- Cytoplasmic tail의 endocytosis signal → AP2 결합
- AP2가 PI(4,5)P₂에 결합하여 unlocked → cargo binding site 노출
- AP2가 clathrin triskelion 모집 → coated pit 형성
- Dynamin에 의해 pinch off → coated vesicle
- Coat shed → early endosome 융합
LDL의 처리
- Early endosome의 낮은 pH → LDL이 receptor에서 방출
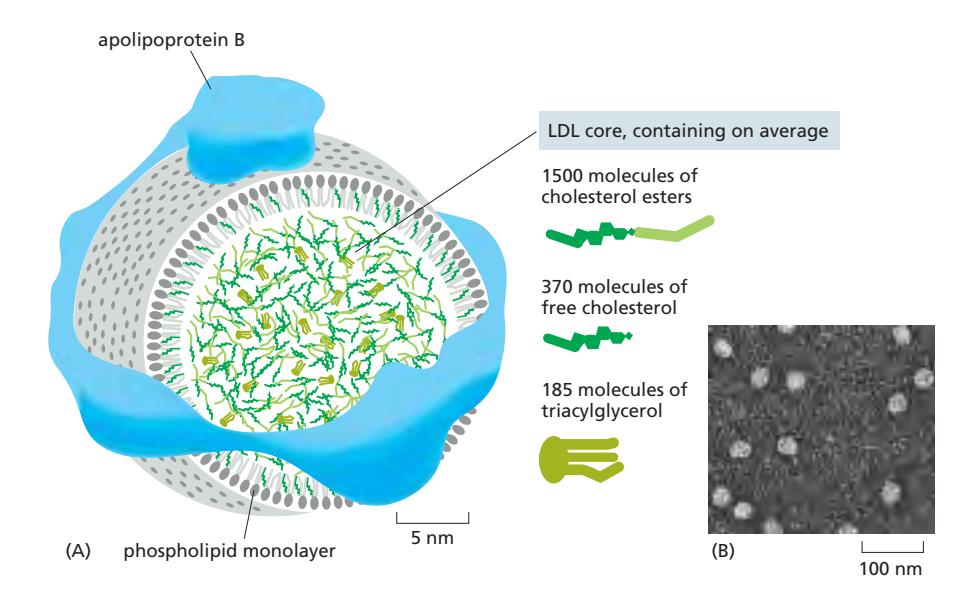
- LDL → Late endosome → Lysosome
- Lysosome: cholesterol ester → free cholesterol (막 합성에 사용)
- LDL receptor: early endosome tubular region → plasma membrane으로 재활용
8. Exocytosis
Exocytosis는 transport vesicle이 plasma membrane과 융합하여 내용물을 세포 외부로 방출하는 과정이다.
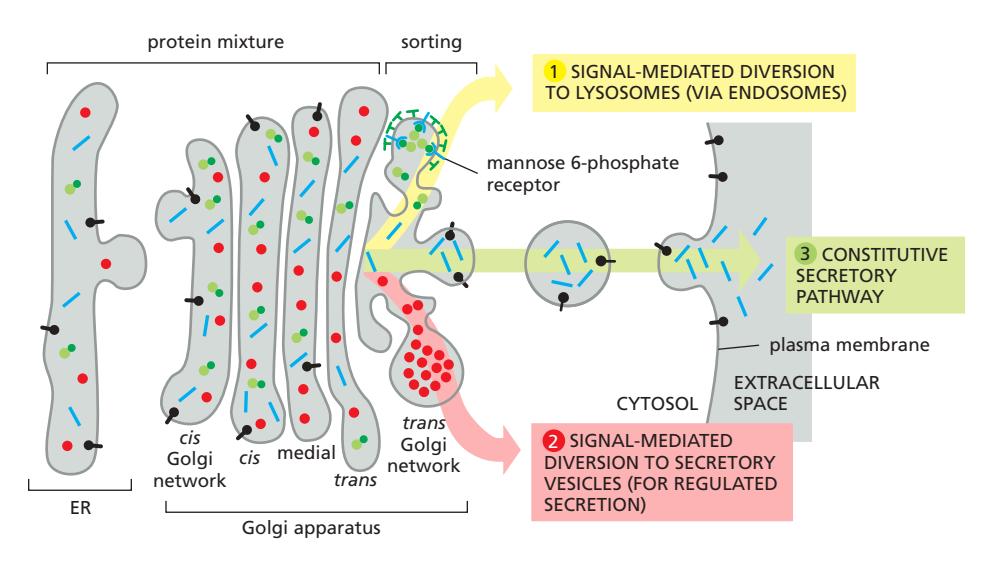
두 가지 경로
1. Constitutive Secretory Pathway (default)
- 모든 세포에서 지속적으로 작동
- 특별한 신호 없이 자동으로 진행
- Plasma membrane 성분, ECM 단백질 전달
2. Regulated Secretory Pathway
- 특수화된 분비 세포에만 존재
- Extracellular signal에 의해 조절 → Ca²⁺가 주요 trigger
- Secretory vesicle에 cargo를 저장 → 신호 시 방출
- Hormone, neurotransmitter, digestive enzyme 등 분비
Secretory vesicle 형성과 성숙:
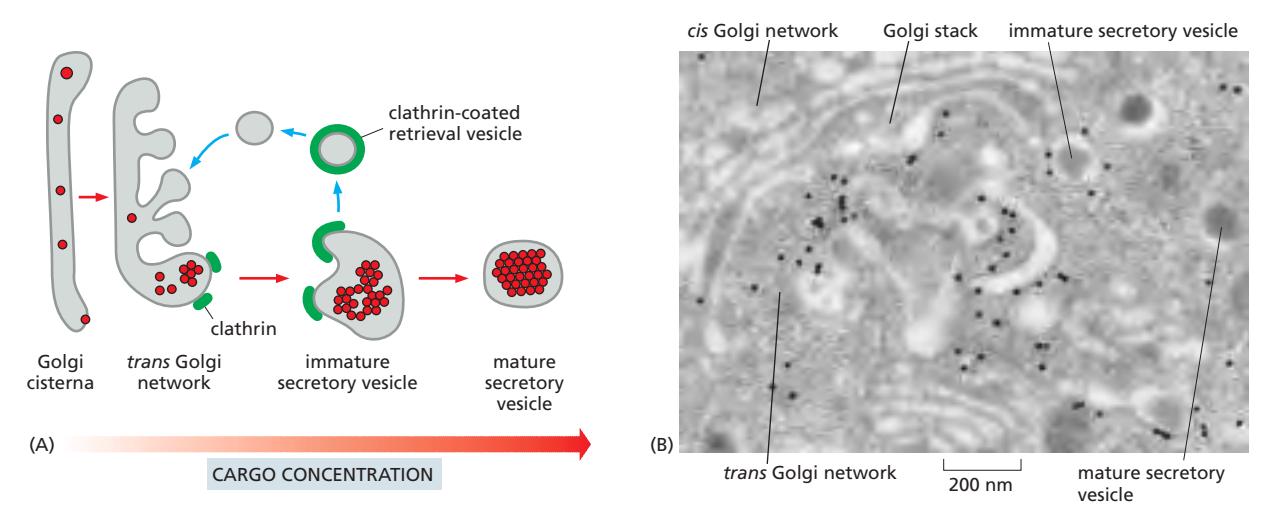
- TGN에서 aggregation: 낮은 pH와 높은 Ca²⁺ 환경이 분비 단백질 응집 촉진 (aggregation hypothesis); 또는 Chromogranins/Secretogranins 같은 granins이 sorting scaffold 역할 (sorting receptor 가설)
- Immature vesicle 형성: aggregate를 둘러싼 membrane budding; 초기에 clathrin coating 존재
- Mature secretory vesicle: clathrin 이탈, 분비 단백질 응축
Ca²⁺-triggered exocytosis:
- 신호 수신 → voltage-gated Ca²⁺ channel 개방
- Ca²⁺ influx → cytosolic Ca²⁺ 농도 급증
- Ca²⁺가 synaptotagmin에 결합 → SNARE complex 활성화 → membrane fusion
Regulated Exocytosis가 Plasma Membrane을 확장하는 경우
4 examples:
- Cytokinesis 중 세포 분열
- Phagocytosis
- Membrane 손상 시 repair
- Fly embryo의 cellularization
9. Secretory Protein의 Proteolytic Processing
Proteolytic processing은 많은 분비 단백질이 비활성 전구체(precursor)로 합성되어 활성화되는 과정이다.
 Processing의 생물학적 이유:
Processing의 생물학적 이유:
- 보호 기능: 세포 내부에서 premature activation 방지 → 세포 손상 방지 (예: digestive enzyme은 secretory vesicle/extracellular space에서만 활성)
- 크기 제한 극복: Enkephalin(5 aa) 같은 짧은 neuropeptide는 co-translational ER entry에 필요한 최소 길이에 미달 → polyprotein으로 합성 후 cleavage
- Tissue-specific enzyme 조절: 같은 precursor라도 세포 유형별 다른 processing enzyme → 다른 최종 산물
- 다양성 생성: 하나의 유전자에서 다양한 polypeptide 생성
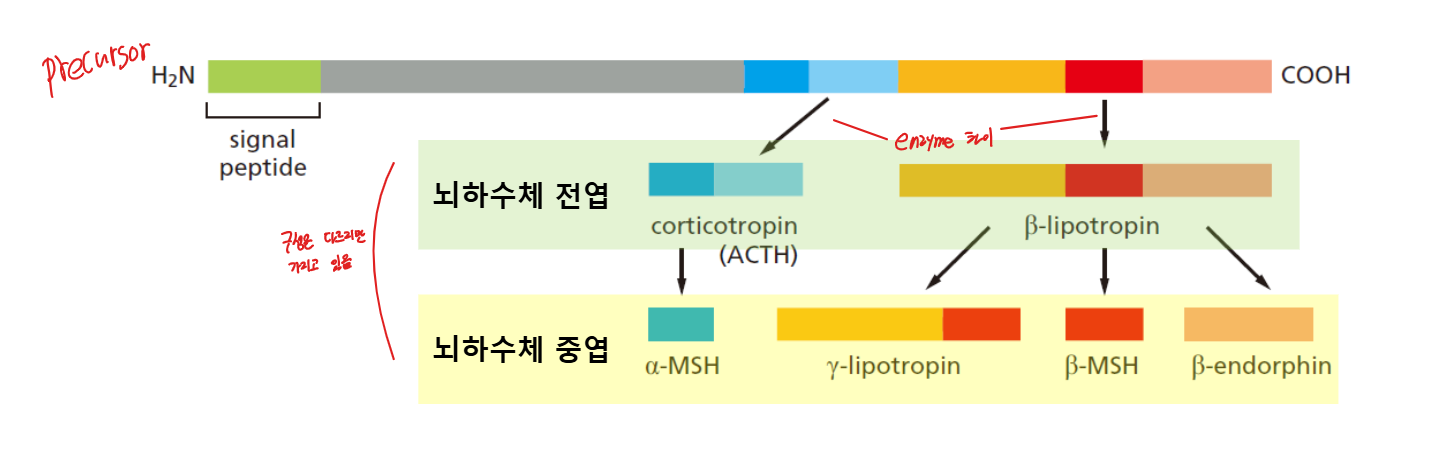
Polyprotein 예시: Proopiomelanocortin (POMC)
동일한 precursor가 서로 다른 세포에서 다른 enzyme에 의해 다른 최종 산물 생성:
- 뇌하수체 전엽 (Anterior pituitary): Corticotropin (ACTH), β-lipotropin
- 뇌하수체 중엽 (Intermediate pituitary): α-MSH, γ-lipotropin, β-MSH, β-endorphin
Processing 장소:
- ER: signal peptide 제거
- Golgi: 일부 초기 cleavage
- Secretory vesicle: 주요 processing 장소 (acidic pH가 protease 활성화)
- Extracellular space: 일부 최종 activation
Proinsulin → Insulin 예시: B chain - C peptide - A chain → Arg-Arg site cleavage → C peptide 제거 → active insulin (B+A chain, disulfide bond)
10. Synaptic Vesicle
Synaptic vesicle은 신경세포에서 neurotransmitter를 저장하고 millisecond 단위로 방출하는 특수화된 secretory vesicle이다.
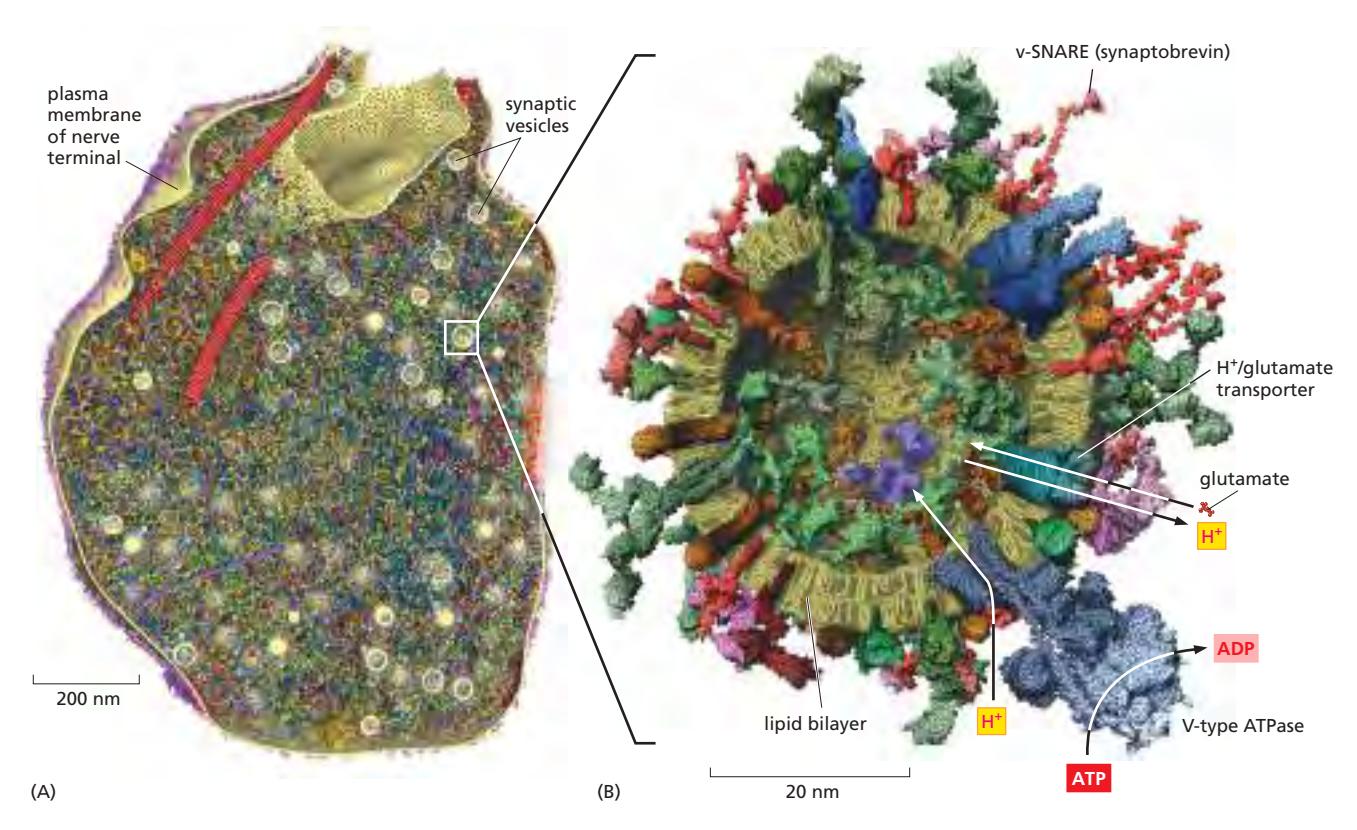
구조
- 직경: 약 50 nm
- Major membrane protein:
- Synaptobrevin (v-SNARE): 가장 풍부, 약 70 copies/vesicle, membrane fusion 필수
- V-type ATPase: H⁺ pump, neurotransmitter loading에 필수
- Neurotransmitter transporter: H⁺ gradient 이용한 antiport
- Cargo: small-molecule neurotransmitter (acetylcholine, glutamate, GABA 등) 약 1,800 molecules
형성: Local Recycling
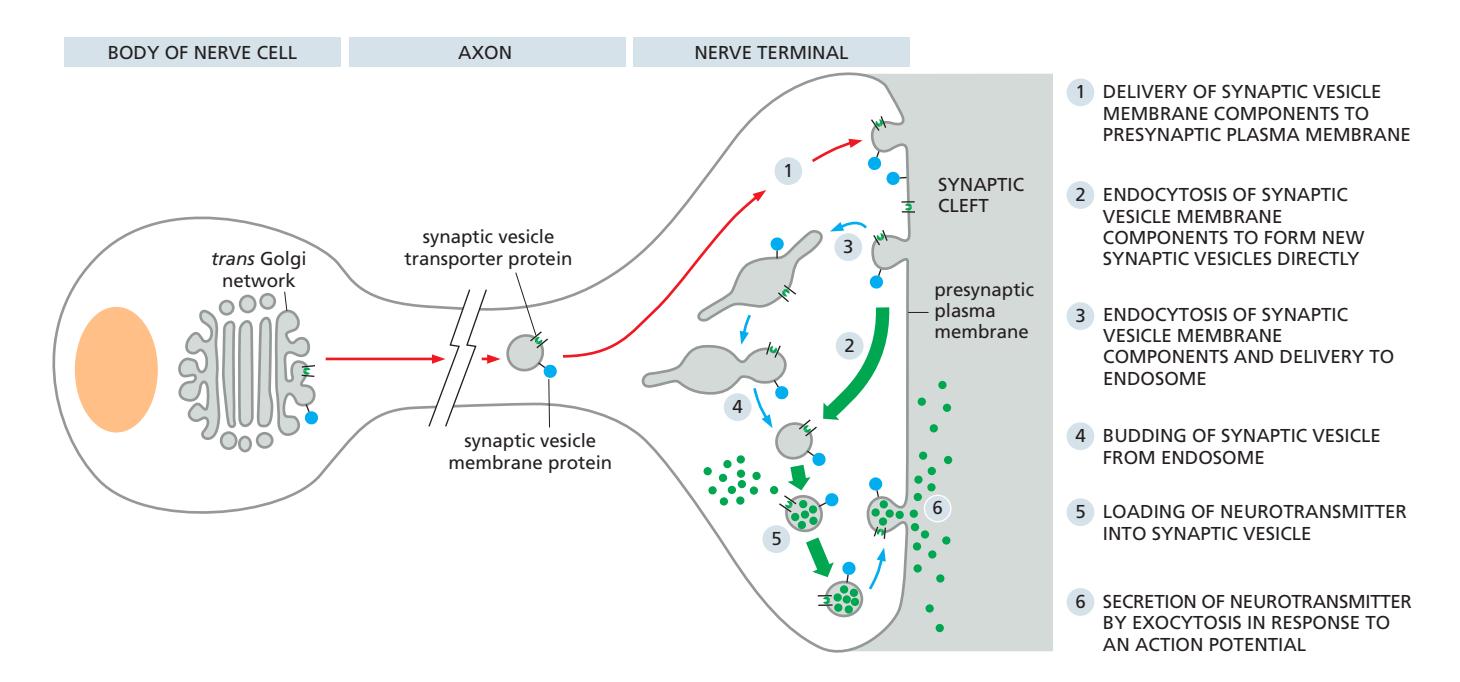
일반적인 secretory vesicle과 달리 local recycling을 통해 형성됨 즉, cytosol의 작은 neurotransmitter를 antiport를 통해 local에서 공급. ER에서 넣어져서 오는 것이 아님.
속도의 중요성:
- 신경세포는 초당 1000회 이상 발화 가능
- 빠른 vesicle 재생성 필요 → local recycling으로 해결 2 - 5 - 6 경로가 가장 빠르고 흔함 3 - 4 - 5 - 6 경로가 느리고 보조적인 경로
Priming 메커니즘
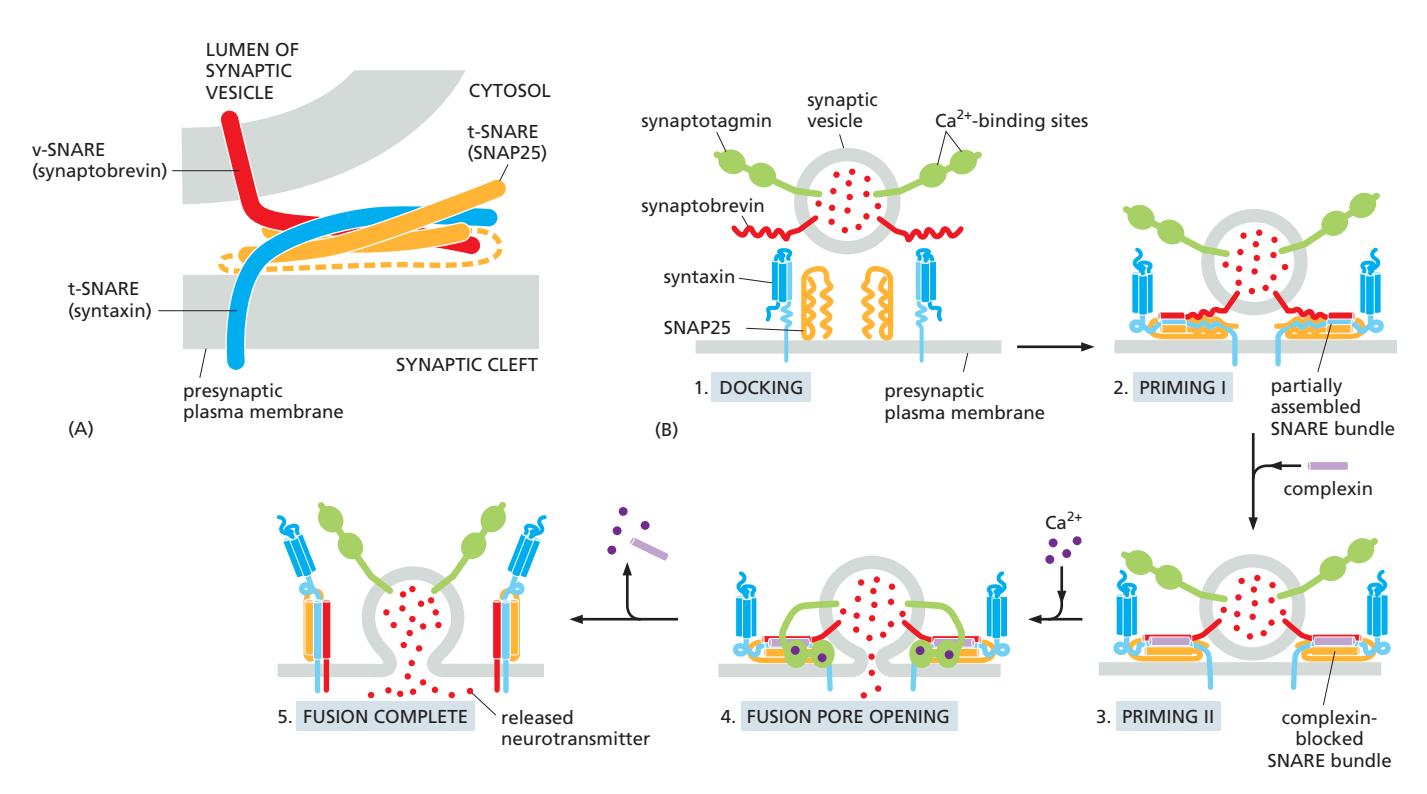
- Vesicle docking: Rab protein + tethering protein으로 presynaptic membrane에 결합
- SNARE partial assembly (Priming I): synaptobrevin + syntaxin + SNAP25가 부분적으로 assemble
- Complexin binding (Priming II): SNARE complex에 결합하여 complete zippering 방지 → metastable state 유지
- Ca²⁺ influx: synaptotagmin 활성화 → complexin displacement → SNARE fully zipper → rapid fusion
11. Polarized Cells에서의 Sorting
극성 세포(예: 상피세포)는 apical과 basolateral domain으로 단백질을 선택적으로 전달한다.
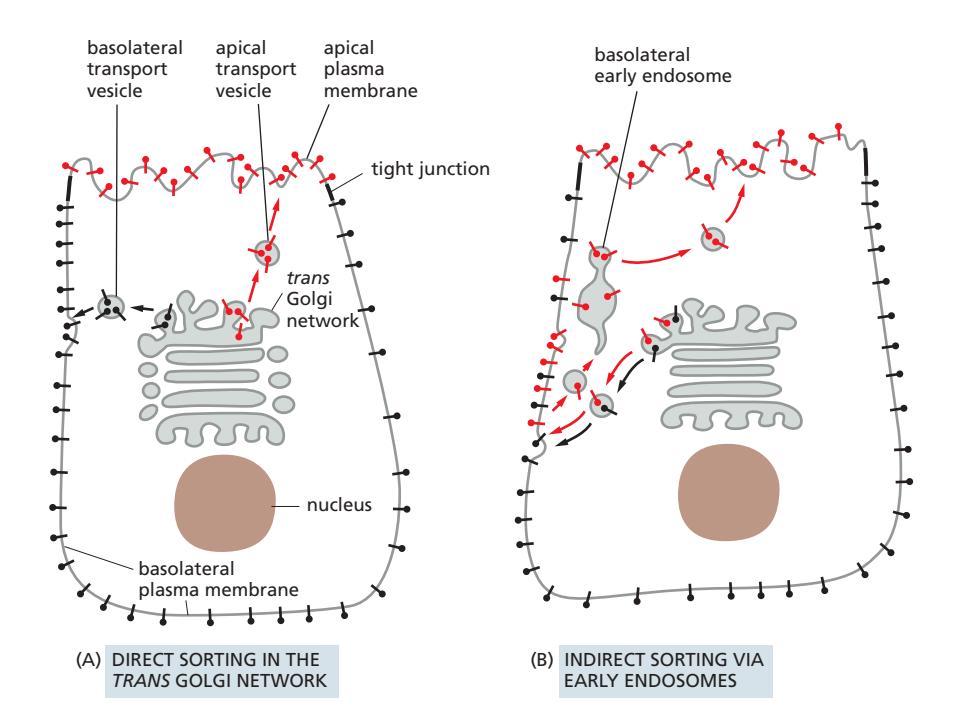
Tight Junction
- Apical domain과 basolateral domain의 경계 유지
- 단백질이 두 domain 사이를 자유롭게 이동하지 못하도록 차단
A: Direct Sorting (주요 경로)
TGN에서 직접 각 domain으로 분류:
B: Indirect Sorting (Transcytosis)
일부 단백질이 먼저 한 domain으로 전달된 후 endocytosis로 회수되어 반대 domain으로 재전달:
- 예: Hepatocyte에서 일부 apical protein이 먼저 basolateral로 → endocytosis → apical domain으로 재전달
- Signal이 두 단계 모두에서 작용
11. 전체 Intracellular Traffic 통합 흐름
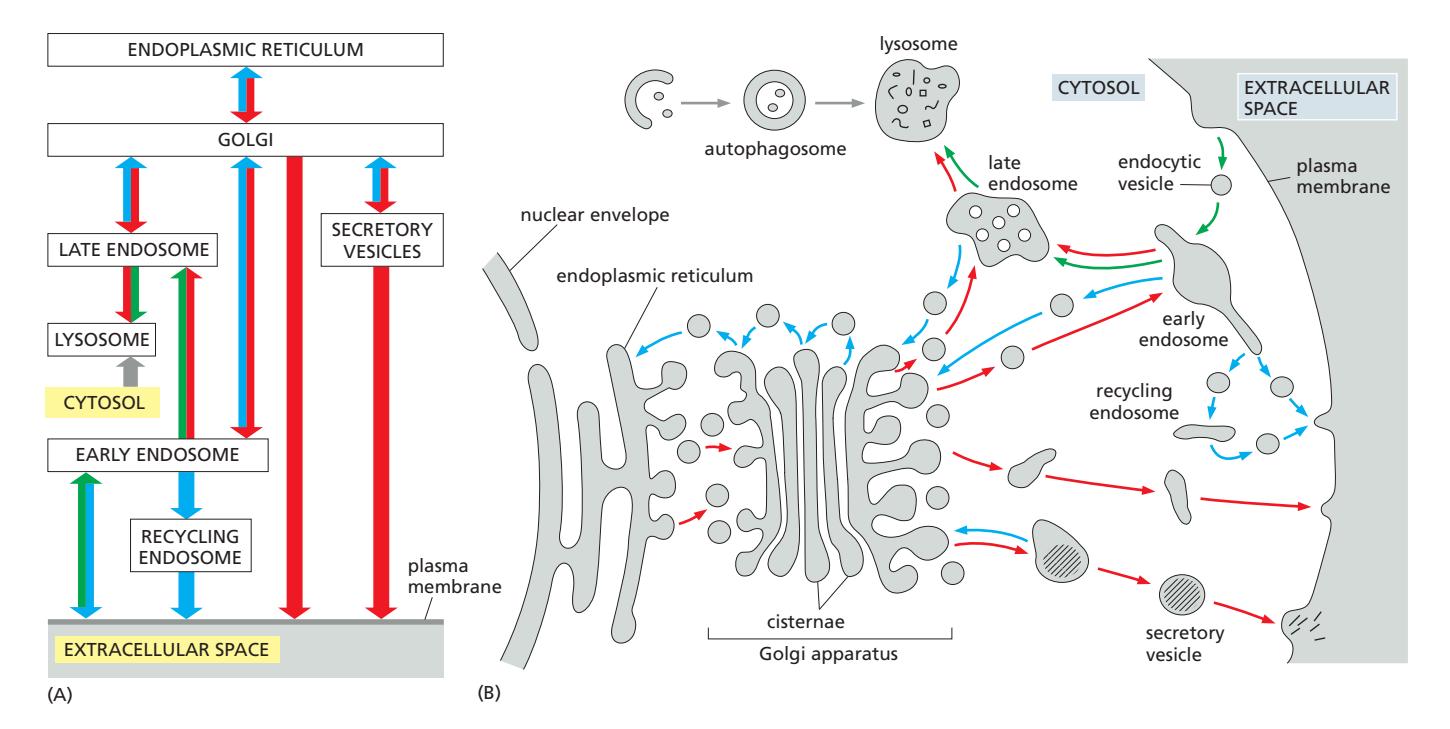
TGN
↙ ↘
M6P receptor Constitutive/Regulated secretion
↓
Early endosome (Rab5, pH ~6.0)
↙ ↘
Recycling Late endosome (Rab7, pH ~5.5)
to PM ↓ (MVB/ESCRT)
Intralumenal vesicle 형성
↓
Endolysosome / Lysosome (pH 4.5–5.0)
관련 내용 노트
- Lysosome 구조와 기능
- Lysosomal hydrolase
- M6P receptor system
- Endosome maturation
- ESCRT protein complex
- Rab5→Rab7 cascade
- Endocytosis 개요
- Receptor-mediated endocytosis (LDL)
- Caveolar endocytosis
- Macropinocytosis
- Exocytosis 개요
- Constitutive vs. regulated secretory pathway
- Synaptic vesicles
- Secretory protein proteolytic processing
- TGN에서의 direct sorting
- SNARE protein