Amphiphilic Molecule
Amphiphilic molecule (또는 amphipathic molecule)은 hydrophilic (“물을 좋아하는”) 또는 polar 부분과 hydrophobic (“물을 싫어하는”) 또는 nonpolar 부분을 모두 가진 분자이다. 세포막의 모든 lipid molecule은 amphiphilic 특성을 가지며, 많은 Membrane protein도 amphiphilic이다.
분자 구조
Amphiphilic molecule은 두 가지 구별되는 화학적 영역으로 구성된다:
Hydrophilic End (Polar End)
특성:
- “물을 좋아하는” 특성
- Charged group 또는 uncharged polar group 포함
- 물 molecule과 favorable interaction 형성 가능
상호작용 메커니즘:
- Electrostatic interaction:
- Charged group이 물 molecule과 favorable electrostatic interaction 형성
- Hydrogen bonding:
- Polar group이 물 molecule과 hydrogen bond 형성
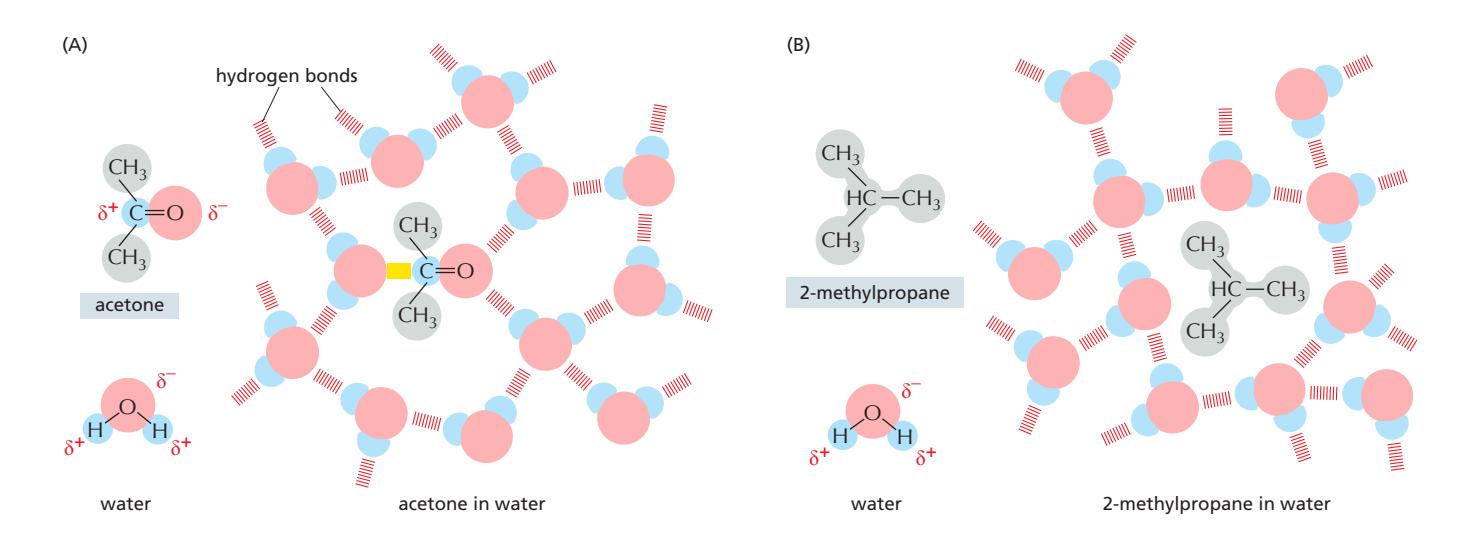 위 그림 (A)는 acetone (polar molecule)이 물과 어떻게 상호작용하는지 보여준다:
위 그림 (A)는 acetone (polar molecule)이 물과 어떻게 상호작용하는지 보여준다:
- Polar group이 물 molecule과 hydrogen bond 형성
- Hydrogen bond (빨간색으로 표시)
- Favorable electrostatic interaction (노란색으로 표시)
- δ-는 partial negative charge, δ+는 partial positive charge
- Polar atom은 색으로, nonpolar group은 회색으로 표시
- 이러한 favorable interaction으로 acetone은 물에 쉽게 용해됨
Hydrophobic End (Nonpolar End)
특성:
- “물을 싫어하는” 특성
- Uncharged and nonpolar atom으로 구성
- 물과 energetically favorable interaction 형성 불가
물과의 상호작용:
위 그림 (B)는 2-methylpropane (완전히 hydrophobic)이 물과 상호작용하는 모습을 보여준다:
-
Icelike cage 형성:
- Hydrophobic molecule이 물에 분산되면
- Adjacent water molecule이 icelike cage structure로 재배열
- 이 cage structure는 주변 물보다 more ordered
-
Entropic cost:
- Cage 형성이 free energy 증가시킴
- 따라서 2-methylpropane은 물에 거의 용해되지 않음
수용액에서의 자발적 배열
Amphiphilic molecule이 수용액에 노출되면 특정 방식으로 자발적으로 pack한다:
배열의 원리
Driving force:
- Hydrophobic tail의 물 노출을 최소화
- Hydrophilic head의 물 노출을 최대화
이 두 경향의 균형이 최적의 packing arrangement를 결정한다.
형성되는 구조
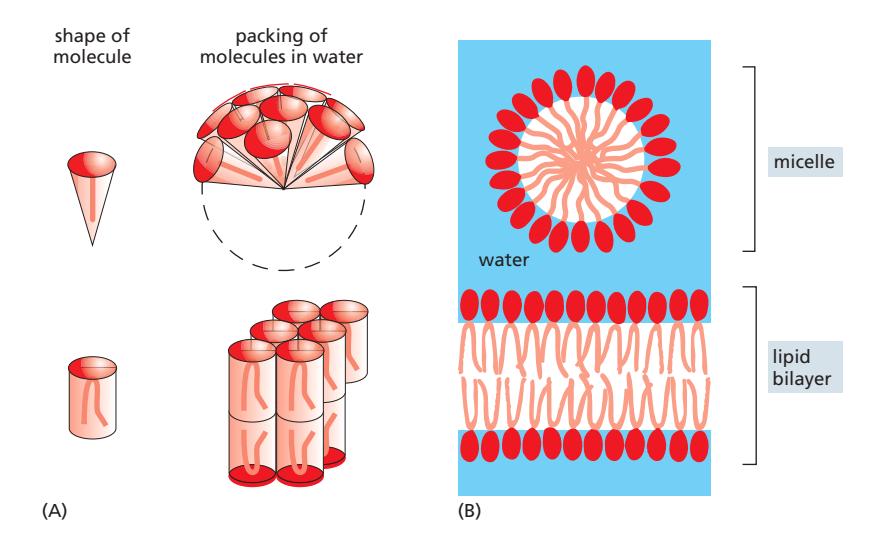
분자의 모양이 최종 구조를 결정한다:

위 그림은 amphiphilic molecule이 수용액에서 자발적으로 Micelle 또는 bilayer를 형성하는 과정을 보여준다.
Cone-shaped Molecule
특성:
- Head가 tail보다 상대적으로 큼
- 또는 tail이 매우 bulky
형성 구조: Micelle
- 구형 aggregate
- Hydrophobic tail이 내부를 향함
- Hydrophilic head가 물과 접촉하는 외부를 향함
- 단일층 배열
Micelle의 구조적 특징:

위 그림 (C)는 detergent molecule이 cone-shaped이기 때문에 bilayer 대신 micelle을 형성함을 보여준다.
실제 micelle은 그림보다 훨씬 더 불규칙한 구조:
- Packing constraint로 인해 hydrophobic tail이 부분적으로 물에 노출됨
- 끊임없이 변화하는 모양
Cylinder-shaped Molecule
특성:
- Head와 tail의 크기가 균형잡힘
- Phospholipid가 전형적인 예
형성 구조: Lipid bilayer
- 이중층 sheet
- Hydrophobic tail이 두 monolayer 사이에 sandwiched
- Hydrophilic head group이 양쪽 표면의 물을 향함

위 그림 (B)는 Micelle과 Lipid bilayer의 단면을 보여준다.
Self-sealing 특성
Amphiphilic molecule의 배열을 유도하는 동일한 힘이 bilayer의 self-sealing property도 제공한다:
메커니즘
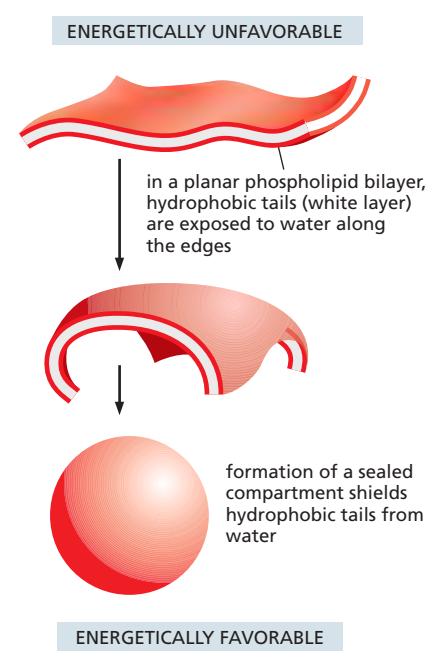
위 그림은 phospholipid bilayer가 자발적으로 닫혀 sealed compartment를 형성하는 과정을 보여준다.
단계:
- Bilayer에 small tear 발생
- Free edge 생성 → 물에 노출됨
- 이는 energetically unfavorable
- Hydrophobic tail이 물과 접촉하게 됨
- Lipid가 자발적으로 재배열하여 free edge 제거
- 중요: Free edge를 피하는 유일한 방법은 자신을 닫는 것
- 결과: Sealed compartment 형성
생물학적 의의: 이 remarkable behavior는 살아있는 세포 창조의 근본이다:
- Phospholipid molecule의 모양과 amphiphilic 특성에서 직접 유래
- 세포가 individual self-replicating unit으로 진화할 수 있게 함
Hydrophobic Effect
Amphiphilic molecule의 배열을 이해하려면 hydrophobic effect를 이해해야 한다:
Hydrophilic Molecule의 용해
Hydrophilic molecule (예: acetone)은 쉽게 물에 용해된다:
이유:
- Charged group 또는 uncharged polar group 포함
- 물 molecule과 favorable electrostatic interaction 형성
- 물 molecule과 hydrogen bond 형성
Hydrophobic Molecule의 비용해
Hydrophobic molecule (예: 2-methylpropane)은 물에 거의 용해되지 않는다:
이유:
- 모든 또는 거의 모든 atom이 uncharged and nonpolar
- 물 molecule과 energetically favorable interaction 형성 불가
- 물 속에 분산되면:
- Adjacent water molecule이 icelike cage로 재배열
- Cage structure가 주변 물보다 more ordered
- 이 형성이 free energy 증가 (entropic cost)
Free Energy 최소화
Clustering: Entropic free-energy cost는 다음과 같이 최소화된다:
- Hydrophobic molecule (또는 amphiphilic molecule의 hydrophobic portion)이 cluster 형성
- 영향받는 water molecule 수를 최소화
- 결과: 전체 free energy 감소
Amphiphilic molecule의 경우: 이 원리가 Phospholipid와 같은 amphiphilic molecule을 다음과 같이 pack하도록 유도:
- Hydrophobic tail끼리 cluster
- Hydrophilic head는 물과 접촉
- Micelle 또는 Lipid bilayer 형성
세포막의 Amphiphilic Component
Membrane Lipid
세포막의 모든 lipid molecule은 amphiphilic이다:
주요 membrane lipid:
-
- Polar head group (phosphate 포함)
- 두 개의 hydrophobic hydrocarbon tail
- Lipid bilayer의 주요 구성 성분
-
- Polar hydroxyl group (단일)
- Hydrophobic steroid ring과 hydrocarbon chain
- Bilayer에서 phospholipid와 상호작용
-
- Polar sugar group
- Hydrophobic lipid portion
- Cell surface에만 존재
Membrane Protein
많은 Membrane protein도 amphiphilic 특성을 보인다:
구조적 특징:
-
Hydrophobic region:
- Lipid bilayer를 통과
- Bilayer 내부의 lipid molecule의 hydrophobic tail과 상호작용
- 물로부터 sequester됨
-
Hydrophilic region:
- Membrane 양쪽의 물에 노출
- 수용성 domain 형성
예시:
- Transmembrane protein
- Amphipathic α helix를 가진 protein (cytosolic surface에 부착)
- Lipid-anchored protein
Detergent로서의 Amphiphilic Molecule
Detergent는 작은 amphiphilic molecule이다:
특성:
- 물에 lipid보다 훨씬 더 잘 녹음
- Variable structure
- Polar end가 ionic 또는 nonionic
Critical Micelle Concentration (CMC):
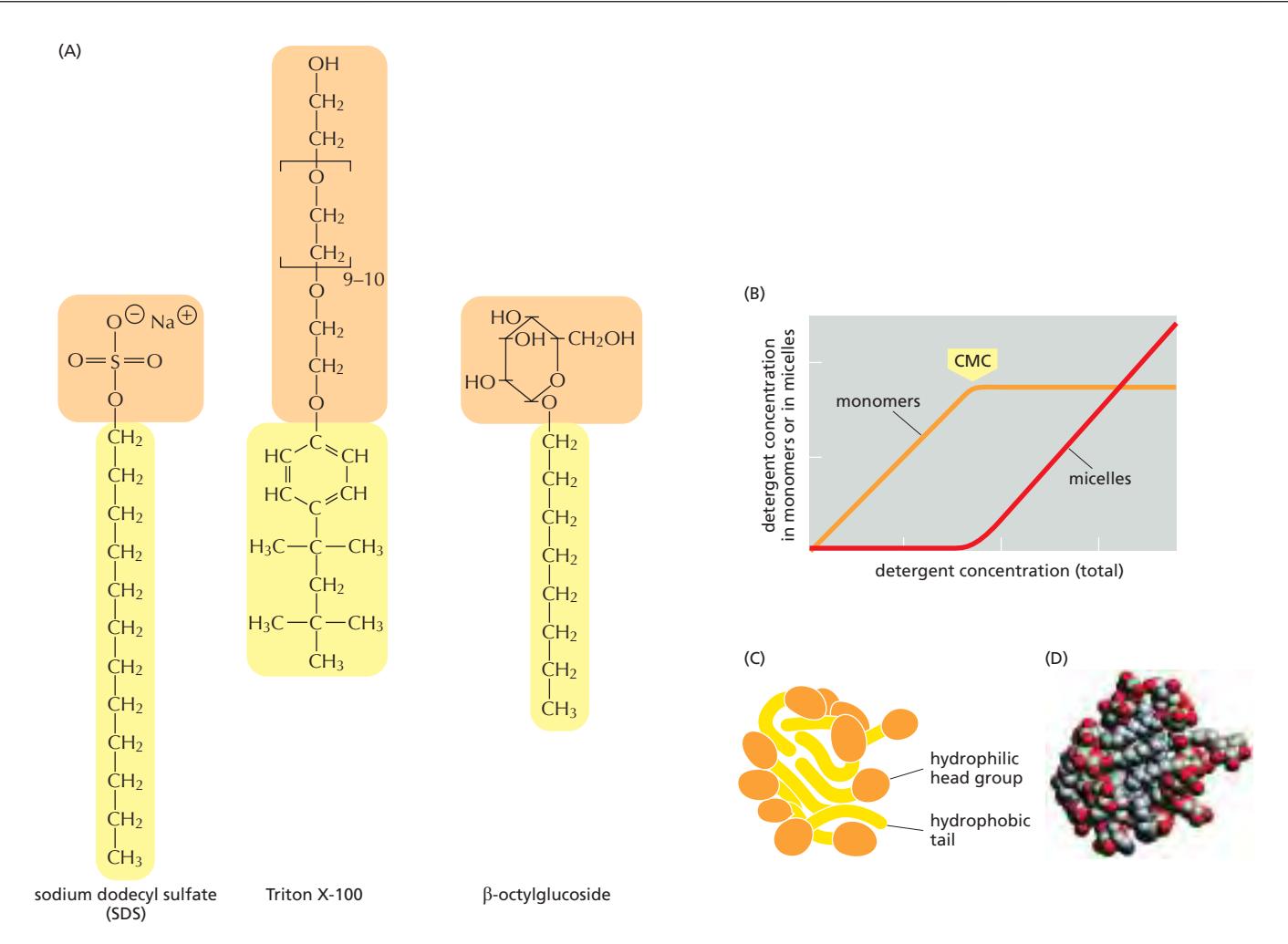
위 그림 (B)는 detergent concentration과 micelle 형성의 관계를 보여준다:
- 낮은 농도: 단량체로 용액에 존재
- CMC 이상: Aggregate하여 Micelle 형성
- CMC 이상에서 단량체 농도는 일정하게 유지
Membrane protein 가용화: Detergent의 amphiphilic 특성이 membrane protein 가용화에 이용됨
생물학적 중요성
Amphiphilic molecule의 특성은 생명의 근본적 특징을 제공한다:
1. Membrane 형성
- Lipid bilayer의 자발적 조립
- Sealed compartment 형성
- 세포 경계의 확립
- Organelle의 구획화
2. Membrane Function
- Selective permeability barrier
- Protein의 적절한 orientation
- Membrane domain 형성
3. Self-organization
- Template 없이 자발적 조립
- Thermodynamically stable 구조
- Self-sealing and self-healing property
4. Evolution
- Individual cell로서 진화 가능하게 함
- Self-replicating unit의 기초
- 복잡한 생명체의 발달 허용