Chapter 12-2: Intracellular Organization and Protein Sorting 정리본
이번 강의 범위
- PEROXISOMES
- THE TRANSPORT OF PROTEINS INTO MITOCHONDRIA AND CHLOROPLASTS
- THE TRANSPORT OF MOLECULES BETWEEN THE NUCLEUS AND THE CYTOSOL
1. 응용 사례: Cystic Fibrosis와 ER Quality Control
CFTR (Cystic Fibrosis Transmembrane conductance Regulator)
- ABC transporter 계열의 membrane 단백질; 상피세포에서 Cl⁻ 채널 역할
- 이온·수분 수송 → thin, hydrated mucus 유지
- ER에서 합성·폴딩, N-linked 당화, chaperone(BiP, calnexin)과 상호작용
낭포성 섬유증 (Cystic Fibrosis)
- 원인: ΔF508 돌연변이 — 508번 phenylalanine 결실
- 결과: ER에서 misfolding → **ERAD**에 의해 분해 → 세포막에 CFTR 없음
- Cl⁻ 분비 불가 → 수분 이동 감소 → 폐·췌장·장에 thick, dehydrated mucus 형성
- 유럽계 인구 약 2,500–3,500명 중 1명에서 발생
핵심: 단백질 품질 관리 시스템의 임상적 중요성을 보여주는 대표 사례
2. PEROXISOMES 기본 특성
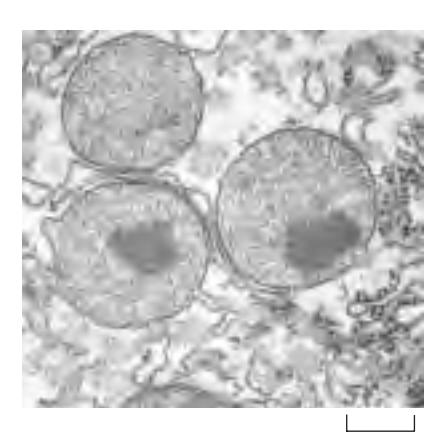 Fig 12-43. 쥐 간세포(rat liver cell)의 peroxisome EM 사진. Electron-dense crystalloid core는 주로 urate oxidase로 구성됨.
Fig 12-43. 쥐 간세포(rat liver cell)의 peroxisome EM 사진. Electron-dense crystalloid core는 주로 urate oxidase로 구성됨.
- **단일막(single membrane)**으로 둘러싸인 소기관
- DNA, ribosome 없음 → 모든 단백질은 핵 유전자로 암호화, 세포질에서 합성
- EM에서 catalase, oxidase 축적 → crystalloid core 관찰 가능
- 단백질은 folded 상태로 수입 가능 (미토콘드리아와 차이)
기능 1: 산화 반응 (Oxidation)
- Catalase: H₂O₂를 즉시 분해 + peroxidation 반응 수행
기능 2: Detoxification (해독; 간에서 중요)
- 알코올, 포름산, 독성 물질 분해
- 섭취한 ethanol의 약 25%를 peroxisome에서 **acetaldehyde(CH₃CHO)**로 산화
기능 3: Fatty Acid β-Oxidation
- 지방산 → acetyl-CoA → cytosol export
- 동물: 미토콘드리아 + peroxisome 분담 (peroxisome은 초장쇄 지방산, VLCFA 담당)
- 효모·식물: peroxisome only
3. Plasmalogen 합성
Plasmalogen 참조
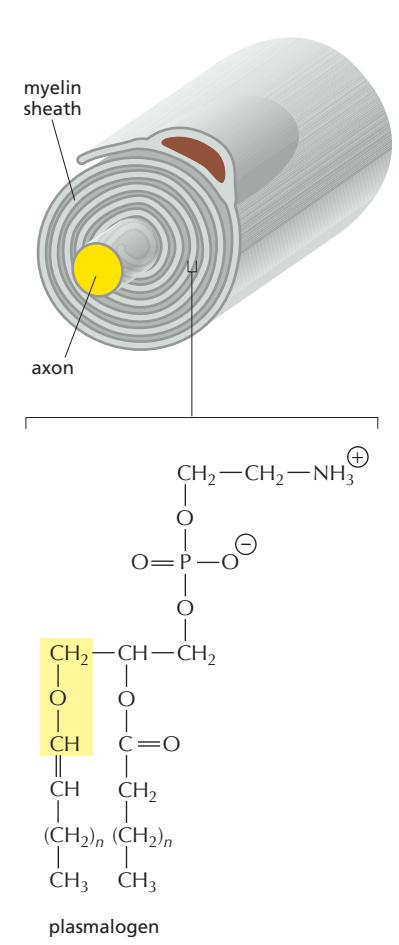 Fig 12-44. Plasmalogen 구조. sn-1 위치에 vinyl ether(-O-CH=CH-) 결합(ether 결합)이 특징. sn-2 위치는 ester 결합.
Fig 12-44. Plasmalogen 구조. sn-1 위치에 vinyl ether(-O-CH=CH-) 결합(ether 결합)이 특징. sn-2 위치는 ester 결합.
- Phospholipid의 한 종류
- Myelin sheath(수초) 인지질의 약 80–90% 차지
- 뇌 백질, 심장, 면역세포에서 풍부
- 막 안정성, 항산화 기능, 신호전달에 중요한 역할
- 합성의 첫 두 단계가 peroxisome에서 수행됨 (ether 결합 형성) → 이후 중간체는 ER로 이동하여 합성 완성
- Peroxisome 기능 장애 시 plasmalogen 합성 불가 → 신경, 근육, 호흡기, 심장 기능 이상 (Zellweger syndrome, Rhizomelic chondrodysplasia punctata)
4. Zellweger 증후군
- 원인: PEX 유전자 (주로 Pex1) 돌연변이 → peroxin(퍼옥시좀 형성·기능에 필수 단백질) 결함
- Cellular Changes: peroxisome 없음 또는 비정상; 세포는 막은 있으나 효소가 없는 “빈” peroxisome 포함; matrix protein import 실패; lipid metabolism 장애
| 대사 결과 | 기전 |
|---|---|
| VLCFA 축적 | Peroxisomal β-oxidation 감소 |
| Plasmalogen 감소 | Membrane structure/function 이상 |
| Oxidative stress 증가 | H₂O₂ detox 장애 |
임상 증상: Severe hypotonia, seizures, hepatomegaly/liver dysfunction, craniofacial dysmorphism (high forehead, flat face) → 대부분 infancy에 사망
§5. Peroxisome 단백질 수입
Protein import into Peroxisome 참조
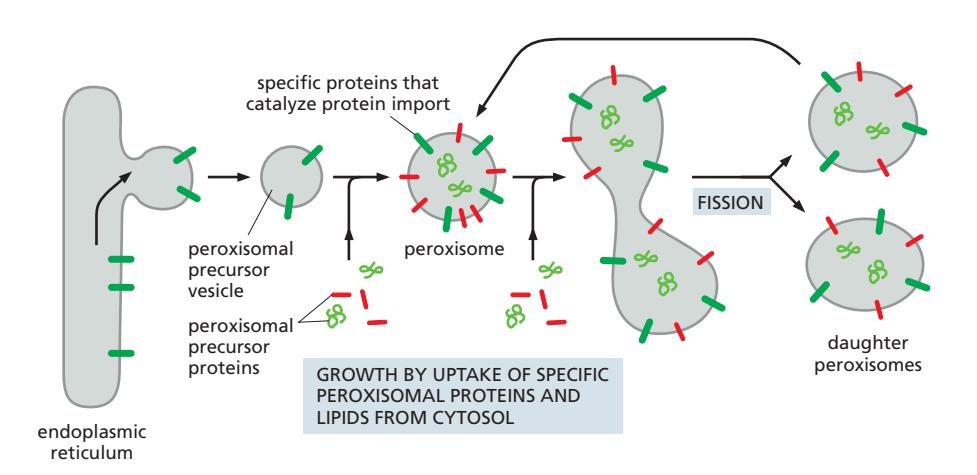 Fig 12-46. 퍼옥시좀 단백질 수입 경로. PTS1/PTS2 → Pex5/Pex7 receptor → Pex translocator → matrix.
Fig 12-46. 퍼옥시좀 단백질 수입 경로. PTS1/PTS2 → Pex5/Pex7 receptor → Pex translocator → matrix.
| Signal | 위치 | 수용체 |
|---|---|---|
| PTS1 | C-말단 3아미노산 (SKL 또는 유사) | Pex5 (cytosolic receptor) |
| PTS2 | N-말단 | Pex7 |
- 단백질은 folded 상태로, 보조인자 결합 상태로도 수입 가능
- Pex5 receptor는 cargo 동반 통과 후 ubiquitin화 → recycling
- 일부 peroxisome 막 단백질은 ER을 거쳐 막으로 이동
6. 미토콘드리아와 엽록체 구획 구조
000_Protein import into Mitochondria_MOC 참조
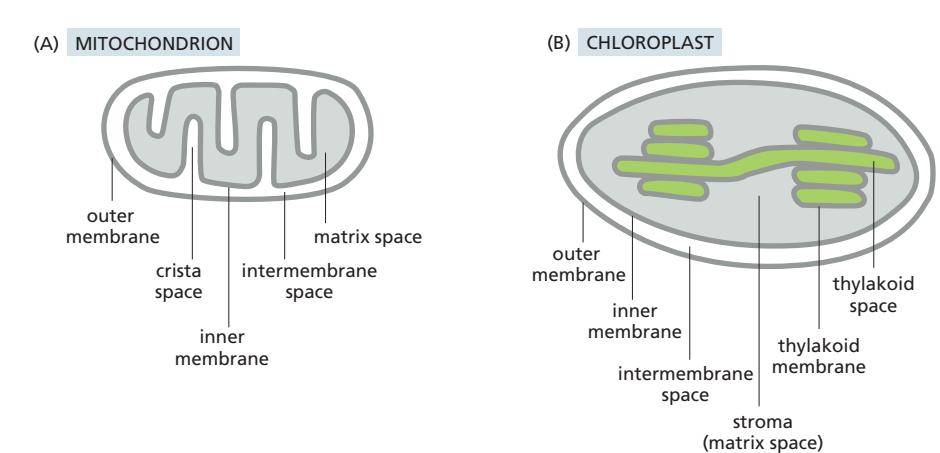 Fig 12-47. 미토콘드리아(A)와 엽록체(B)의 세부 구획 비교.
Fig 12-47. 미토콘드리아(A)와 엽록체(B)의 세부 구획 비교.
| 소기관 | 구조 | 주요 기능 |
|---|---|---|
| 미토콘드리아 | Outer membrane + IMS + inner membrane(cristae) + matrix | ATP 생산 (산화적 인산화); TCA 회로 |
| 엽록체 | Outer + IMS + inner + stroma + thylakoid membrane + thylakoid lumen | ATP + NADPH 생산 (광합성); Calvin 회로 |
- 미토콘드리아 cristae: inner membrane의 일부 → 산화적 인산화를 위한 표면적 증가
- 엽록체 thylakoid: inner membrane에 연결되지 않는 독립된 밀봉된 구획 (미토콘드리아와 차이)
- 단백질의 ~99%는 핵 유전자 암호화 → 세포질 합성 후 번역 후(post-translational) 수입
7. Translocator 복합체
Translocators in mitochondrial membrane 참조
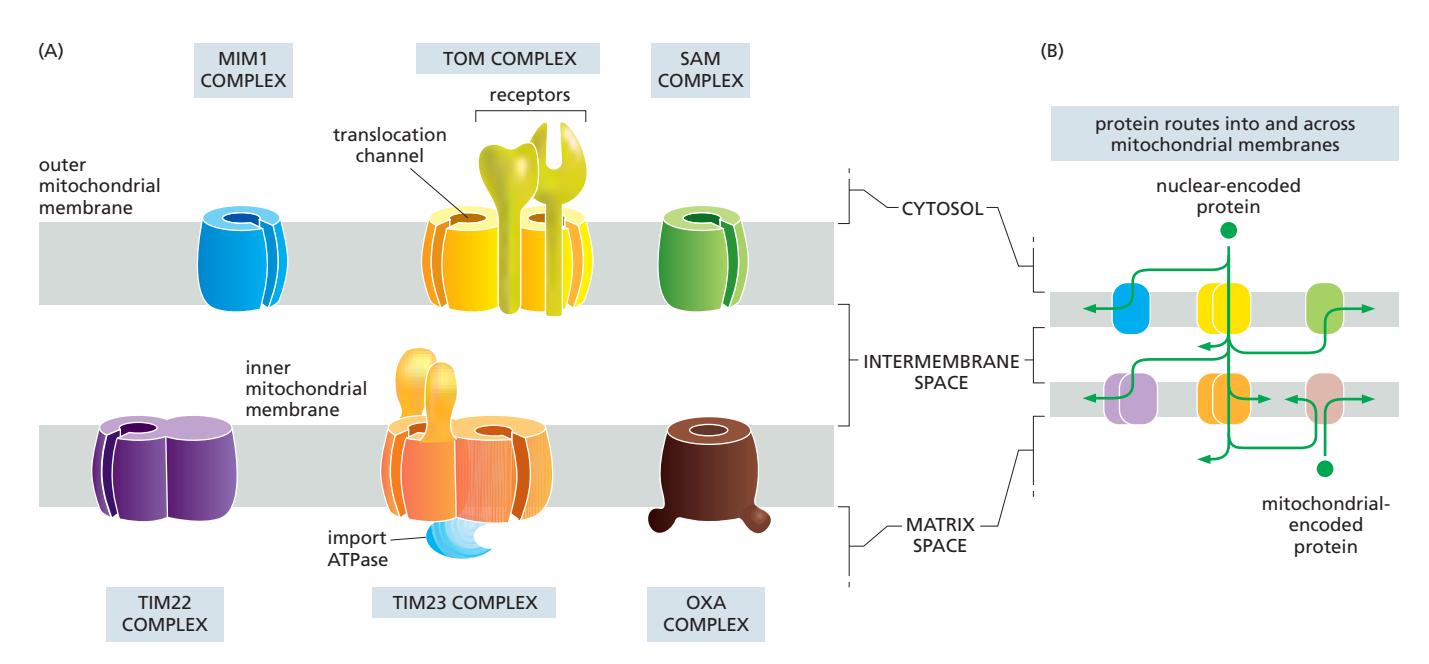 Fig 12-48. 미토콘드리아 막의 translocator 복합체 구조(A)와 경로(B).
Fig 12-48. 미토콘드리아 막의 translocator 복합체 구조(A)와 경로(B).
| 복합체 | 위치 | 역할 |
|---|---|---|
| TOM | Outer membrane | 모든 핵 암호화 단백질의 첫 번째 관문; cytosol에서 signal sequence 인식 → IMS로 수송; α-나선형 소수성 분절 단백질은 측면(lateral)으로 outer membrane에 방출 가능; β-barrel 단백질은 SAM complex로 넘겨짐 |
| TIM23 | Inner membrane | Matrix 단백질 및 일부 inner membrane 단백질 (lateral release) |
| TIM22 | Inner membrane | Multipass inner membrane 단백질 (대사물질 transporter 등) |
| SAM | Outer membrane | β-barrel 단백질 삽입·폴딩 (TOM → SAM 경로) |
| MIM | Outer membrane | α-helical outer membrane 단백질 삽입 |
| OXA | Inner membrane | 미토콘드리아 genome 암호화 단백질; matrix 쪽에서 접근 |
- 모든 핵 암호화 미토콘드리아 단백질은 반드시 unfolded 상태로 통과
8. Matrix 단백질 수입 — 7단계 메커니즘
000_Protein import into Mitochondria_MOC 참조
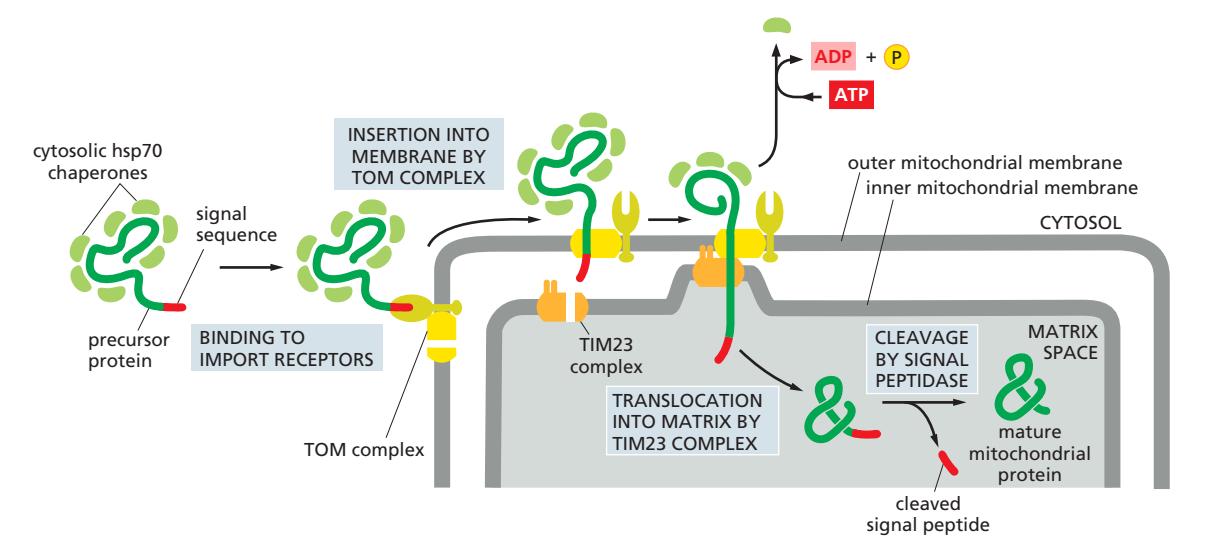
- Precursor 단백질이 cytosol에서 N-terminal signal sequence와 함께 합성
- Cytosolic hsp70이 결합 → unfolded 상태 유지 (조기 aggregation 방지)
- Signal sequence가 TOM complex에 결합 → outer membrane 통과
- TIM23 complex로 전달 → inner membrane 통과 개시
- Mitochondrial hsp70 (import ATPase)이 polypeptide chain을 ATP 가수분해로 matrix 방향으로 끌어당김
- Matrix 내 **MPP (Mitochondrial Processing Peptidase)**가 signal sequence 절단
- Mitochondrial hsp60으로 전달되어 최종 폴딩 완성
9. 수입의 3가지 에너지원
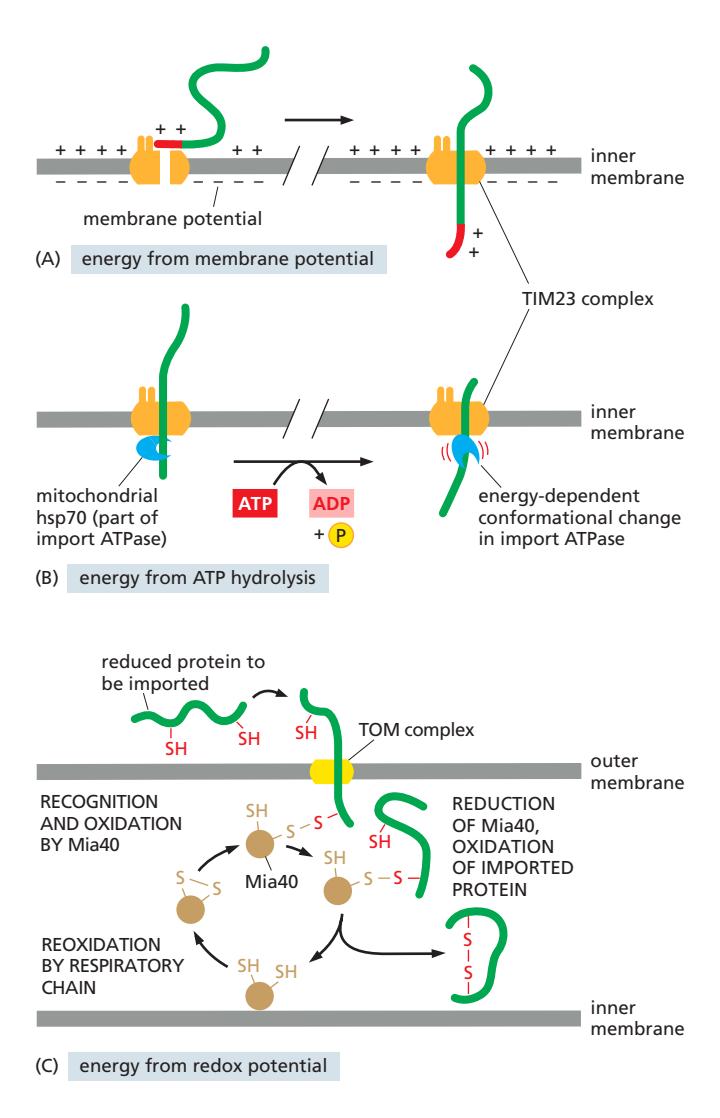 Fig 12-50. (A) 막전위 Δψ — TIM23 통과 구동. (B) Mitochondrial hsp70 + ATP — matrix로 끌어당김. (C) Mia40 redox — disulfide 형성으로 IMS 단백질 고정.
Fig 12-50. (A) 막전위 Δψ — TIM23 통과 구동. (B) Mitochondrial hsp70 + ATP — matrix로 끌어당김. (C) Mia40 redox — disulfide 형성으로 IMS 단백질 고정.
| 에너지원 | 위치 | 역할 |
|---|---|---|
| ATP (cytosolic hsp70) | 세포질 | Precursor를 unfolded 상태로 유지 |
| 막전위 Δψ | Inner membrane | 양전하 MTS를 matrix 방향으로 electrophoresis |
| ATP (mitochondrial hsp70) | Matrix (TIM23에 부착) | Polypeptide chain을 matrix로 끌어당김 (ratchet) |
| 산화환원 전위 (Mia40) | IMS | Cys에 disulfide 결합 → IMS 단백질 포획; 호흡사슬이 Mia40 재산화 |
TOM 통과에는 에너지 불필요. TIM23 = Δψ. Matrix 완전 수입 = ATP.
10. Inner Membrane 단백질 수송 경로 4가지
Transport into inner mitochondrial membrane 참조
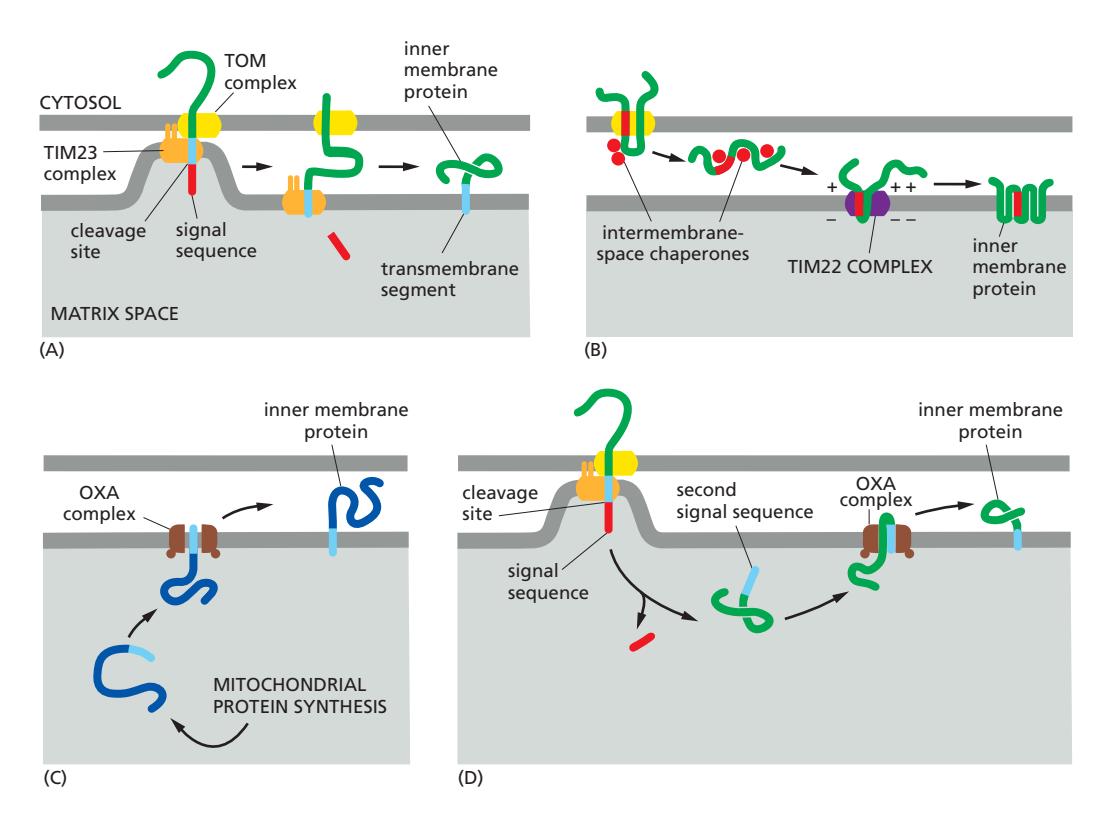 Fig 12-51 (A–D). Inner membrane 단백질 4가지 수입 경로.
Fig 12-51 (A–D). Inner membrane 단백질 4가지 수입 경로.
| 경로 | 메커니즘 |
|---|---|
| (A) TIM23 lateral release | N-terminal signal → TIM23 통과 후 소수성 TM domain이 inner membrane으로 측면 방출; signal 절단 |
| (B) TOM → matrix → OXA | N-terminal signal → matrix로 완전 수입 → MPP 절단 → 노출된 두 번째 소수성 signal이 OXA 경로로 inner membrane 삽입 |
| (C) TOM → TIM22 | Internal signal sequences가 TOM을 loop 형태로 통과; IMS chaperone이 안내 → TIM22가 multipass 단백질 삽입 |
| (D) OXA (미토콘드리아 genome) | 미토콘드리아 ribosome이 matrix에서 합성 → OXA 복합체가 직접 inner membrane에 삽입 |
11. Nuclear Envelope 구조
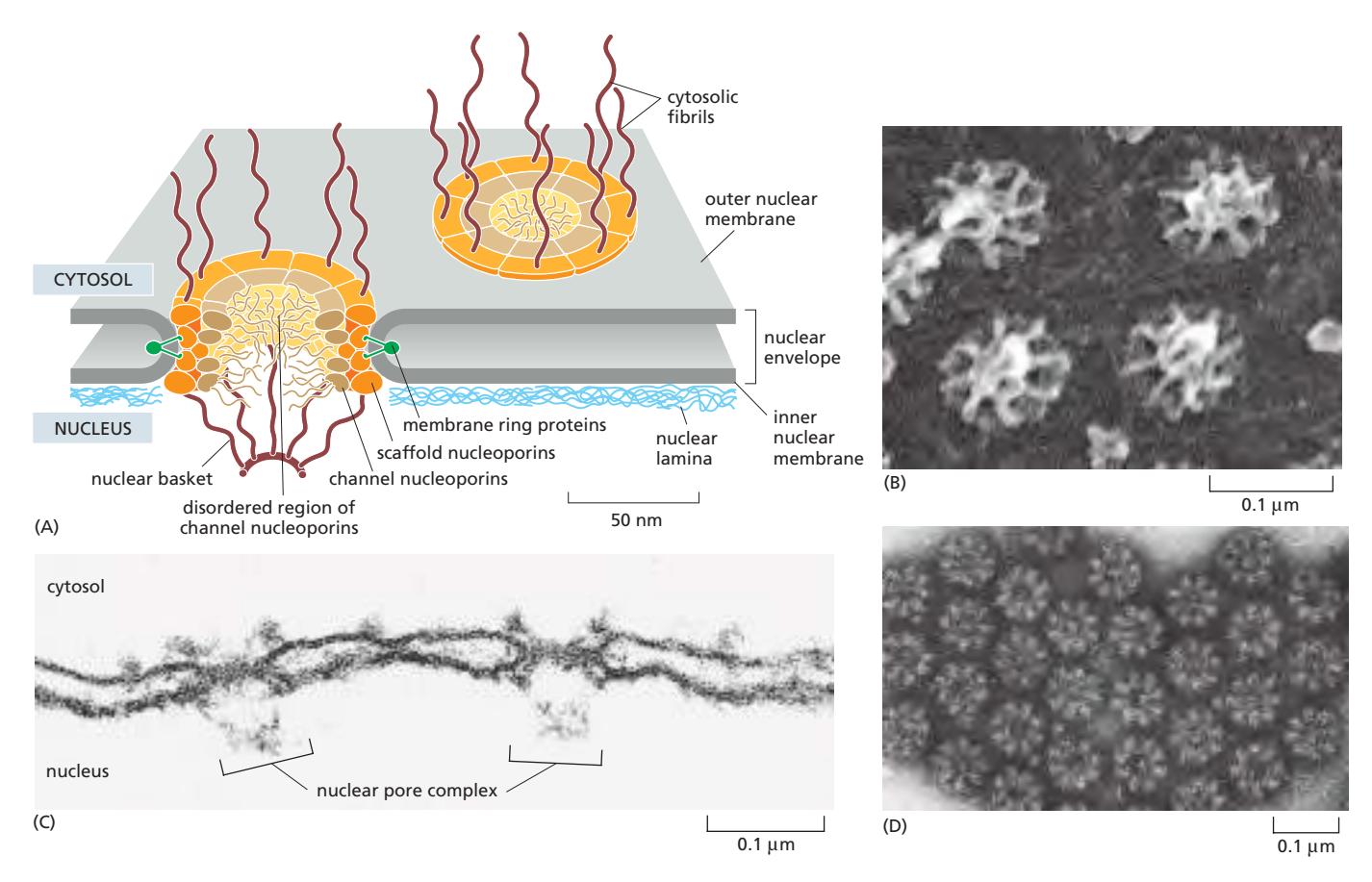 Fig 12-54A. 핵막과 NPC, nuclear lamina, nucleolus의 관계.
Fig 12-54A. 핵막과 NPC, nuclear lamina, nucleolus의 관계.
- Outer nuclear membrane: ER과 연속; 표면에 ribosome → rough ER와 동일한 성격
- Inner nuclear membrane: Nuclear lamina 결합 단백질 포함; chromatin 및 NPC와 연결
- Perinuclear space: 두 막 사이 공간; ER lumen과 연속
- Inner + outer membrane은 NPC 위치에서 융합하여 통로 형성
Nuclear Lamins (핵 라민)
- Inner nuclear membrane 안쪽 표면을 덮는 섬유성 단백질 meshwork → intermediate filament 단백질 계열
- 기능 4가지:
- 구조적 지지: Nuclear envelope에 기계적 안정성 제공
- Chromatin 부착 부위: 염색체와 결합
- NPC 고정: Nuclear pore complex의 위치 고정
- Cytoskeleton 연결: Transmembrane 단백질 복합체를 통해 세포질 cytoskeleton과 연결 → DNA-핵막-세포골격 구조 연결
- 유사분열 시 lamin 인산화 → lamina 분해 → 핵막 해체; 말기 탈인산화 → 재조립
Nucleolus (핵소체)
Nucleolus 참조
- 막 없이 biomolecular condensate로 존재; rRNA 전사·가공, 리보솜 조립이 일어나는 곳
- 리보솜 조립 사이클: cytosol에서 합성된 ribosomal protein → 핵으로 수입 → nucleolus에서 pre-rRNA와 조립 → pre-ribosomal particle이 NPC를 통해 세포질로 수출
- 내부는 동심 구획 구조: Fibrillarin (fibrillar component scaffold), Nucleophosmin (granular component scaffold) 등 scaffold 간 약한 친화력 차이로 다층 condensate 형성
- In vitro 실험: 두 단백질을 RNA와 함께 각각 별도로 혼합하면 각자 별도의 condensate 형성; 함께 혼합하면 하나의 condensate 안에 다른 condensate가 포함된 다층(layered) 구조 형성 → nucleolus 내부 동심 구획의 자기조립(self-assembly) 원리 증명
12. Nuclear Pore Complex (NPC) 구조
Nuclear Pore Complex (structure) 참조
 Fig 12-55A. NPC 구조 모식도.
Fig 12-55A. NPC 구조 모식도.
구성 및 크기
- ~30종 nucleoporin, 8/16/32 카피 → 총 500–1,000개 단백질 / 직경 ~120 nm
- 포유류 세포 NPC: 3,000–4,000개; 초당 최대 1,000개 거대분자 양방향 수송
Nucleoporin 분류
| 종류 | 기능 |
|---|---|
| Transmembrane ring | NPC를 nuclear envelope에 고정 |
| Scaffold nucleoporin | 층상 ring 구조 형성; 막 굴곡 단백질 역할 |
| Channel nucleoporin | FG repeat 포함 disordered 영역 → gel-like FG mesh (선택적 장벽) |
| Cytosolic fibrils | Import receptor 최초 모집 부위 |
| Nuclear basket | 핵쪽 fibrils가 distal end에 모여 바구니 형성; RNA processing/export 관련 |
대칭성
- 8중 회전 대칭 (8/16/32 copies)
- 2중 횡단 대칭 (twofold transverse symmetry): 핵쪽과 세포질쪽 구조 유사하나 기능 다름
13. NPC를 통한 수동 확산 vs 능동 수송
Nuclear Pore Complex (structure) 참조
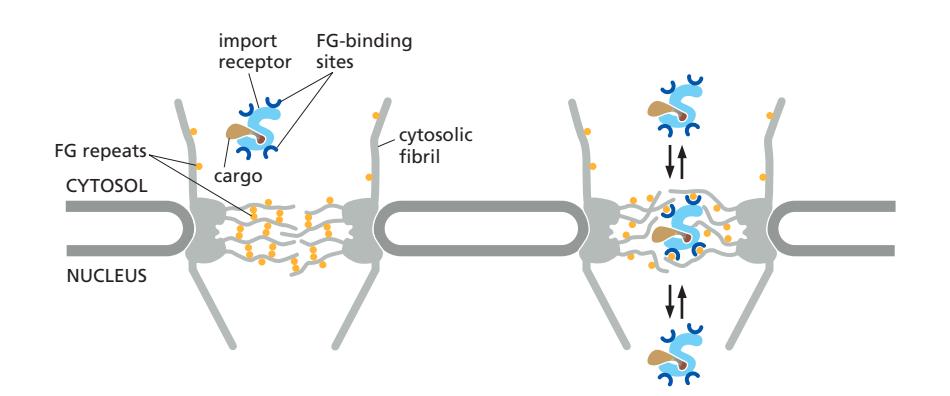 Fig 12-57. NLS를 입힌 금 입자(5–10 nm)의 NPC 통과 EM 시리즈. (A) 세포질 fibril에 접촉 → (B,C) NPC 중심 통과 → (D) 핵 면에 도달.
Fig 12-57. NLS를 입힌 금 입자(5–10 nm)의 NPC 통과 EM 시리즈. (A) 세포질 fibril에 접촉 → (B,C) NPC 중심 통과 → (D) 핵 면에 도달.
| 분자 크기 | 수송 방식 |
|---|---|
| < 5 kDa (~5 nm) | 자유 확산 (이온, 대사산물) |
| ~40 kDa 이하 (~9 nm) | 느린 수동 확산; 에너지·signal 불필요 |
| > ~60 kDa (>9–10 nm) / RNA | 수동 확산 불가; NLS/NES + energy 필요 |
| 성숙 세포질 ribosome (~30 nm) | NPC 통과 불가 → 단백질 합성은 세포질에 국한 |
- 능동 수송 단백질은 완전히 folded 상태로 통과 (미토콘드리아 수입과 달리 unfold 불필요)
14. Nuclear Localization Signal (NLS)
Nuclear Localization Signals 참조
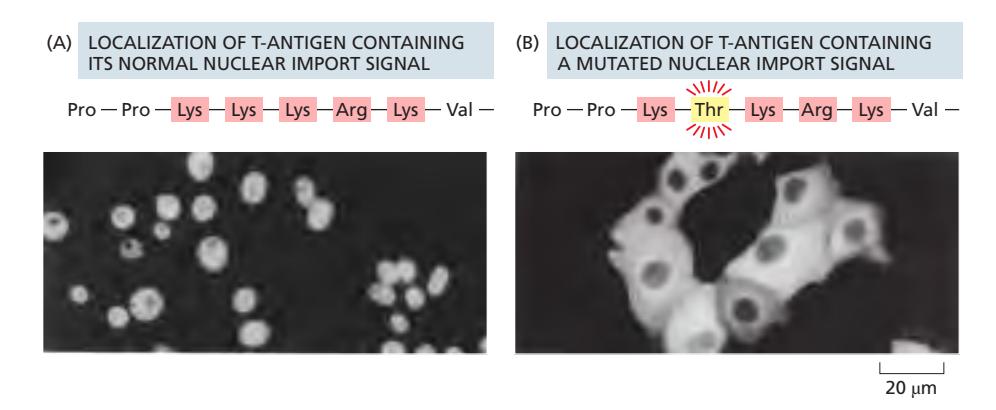 Fig 12-56. (A) 정상 NLS(Lys-rich) → 핵 축적. (B) Lys→Thr 변형 → 세포질에 잔류.
Fig 12-56. (A) 정상 NLS(Lys-rich) → 핵 축적. (B) Lys→Thr 변형 → 세포질에 잔류.
- Lys(K), Arg(R)이 풍부한 양전하 짧은 서열 (하나 또는 두 묶음)
- 예시 (SV40 T-antigen):
...Pro–Pro–Lys–Lys–Lys–Arg–Lys–Val... - 아미노산 서열의 거의 어느 위치에나 존재 가능
- 수입 후에도 절단되지 않고 유지 → 유사분열 후 핵 재조립 시 반복 수입 가능
- 다성분 복합체에서 한 subunit만 NLS 보유해도 복합체 전체 수입 가능
Nuclear Export Signal (NES)
- Leu(류신)이 풍부한 소수성 짧은 서열
- Exportin이 인식 → 단백질/RNA를 세포질로 수출
RNA 및 리보솜 단백질은 합성 후 NES를 통해 세포질로 이동; 전사인자는 필요할 때만 핵 안으로 수입
NLS vs NES 비교
| NLS | NES | |
|---|---|---|
| 역할 | 세포질 → 핵 | 핵 → 세포질 |
| 인식 | Nuclear import receptor | Nuclear export receptor |
| Ran-GTP 효과 | Cargo 해리 촉진 | Cargo 결합 촉진 |
| 제거 여부 | 제거 안 됨 | 제거 안 됨 |
| 아미노산 잔기 | Lys(K), Arg(R) 풍부 (양전하, 염기성) | Leu(L) 풍부 (소수성) |
- NLS + NES 모두 가진 단백질 → 핵-세포질 간 왕복(shuttling) 가능; 수입/수출 속도 비율이 정상 상태 위치 결정
15. Nuclear Import Receptor (Importin)
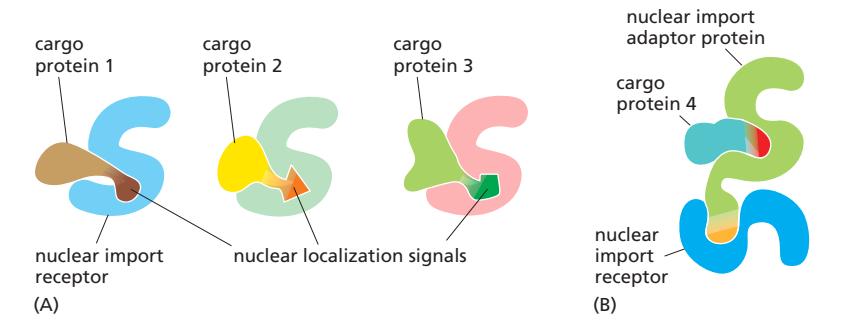 Fig 12-58. (A) 서로 다른 import receptor가 서로 다른 NLS를 인식. (B) Adaptor 단백질을 통한 간접 결합.
Fig 12-58. (A) 서로 다른 import receptor가 서로 다른 NLS를 인식. (B) Adaptor 단백질을 통한 간접 결합.
- Karyopherin 단백질 계열의 soluble cytosolic 단백질
- 서로 다른 NLS는 서로 다른 특정 import receptor가 인식
Importin α / β
| Subunit | 역할 |
|---|---|
| Importin α | NLS를 직접 인식하는 adaptor 역할; cargo와 결합 |
| Importin β | NPC의 FG repeat과 상호작용하여 통과 담당 |
Adaptor 단백질
- 일부 cargo는 NLS가 receptor에 직접 결합하지 못함 → adaptor 단백질 필요
- Adaptor는 import receptor와 구조적으로 유사; cargo의 NLS를 인식하고, cargo 결합 시에만 자체 NLS가 노출되어 receptor에 결합
FG Repeat와의 상호작용
- Import receptor는 FG repeat에 낮은 친화력으로 반복 결합/해리하면서 mesh를 통과
- 이를 통해 receptor에 결합한 cargo는 빠르고 효율적으로 핵 안으로 이동
16. GTP-GDP 사이클과 Ran GTPase
Ran-GTP cycle & Transport Through NPC 참조
- Ran: Guanosine 5’-Triphosphatase (GTPase) — molecular switch
| 조절 단백질 | 위치 | 작용 |
|---|---|---|
| RanGAP (GTPase-activating protein) | 세포질 | Ran-GTP → Ran-GDP 전환 촉진 |
| RanGEF (guanine nucleotide exchange factor) | 핵 chromatin | Ran-GDP → Ran-GTP 전환 촉진 |
→ 핵: Ran-GTP 높음 / 세포질: Ran-GDP 높음 의 농도 기울기 형성
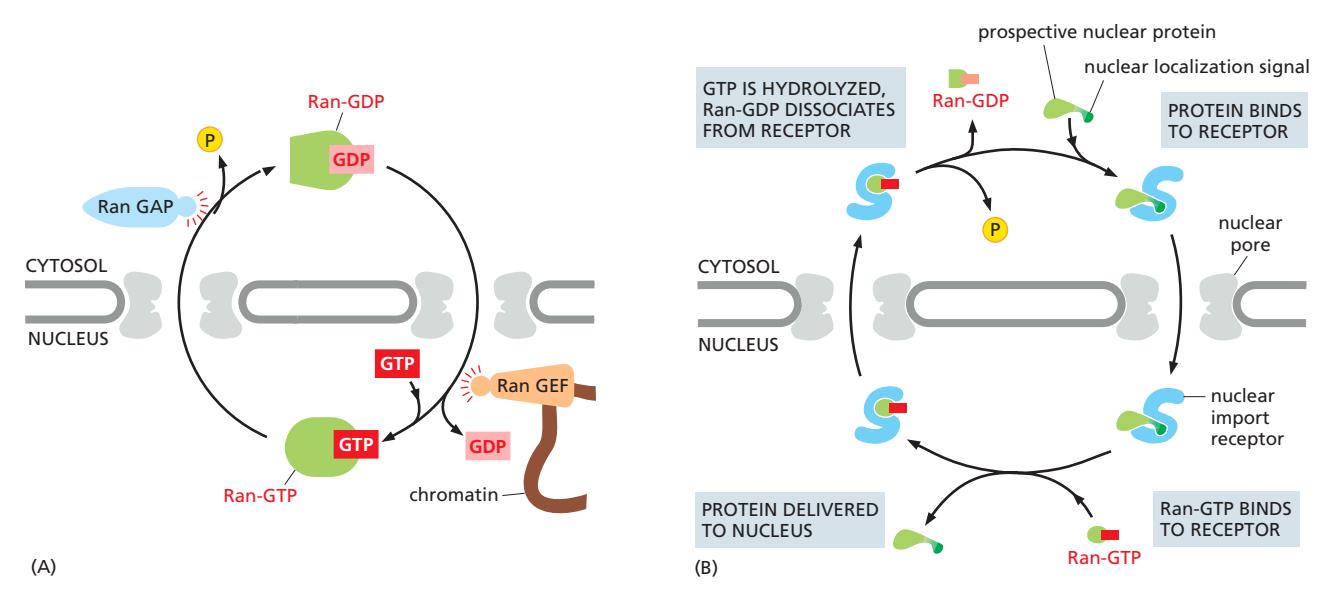 Fig 12-60. Ran-GDP/Ran-GTP 구획화. (A) RanGAP(세포질)/RanGEF(핵)의 위치 차이가 기울기를 유지. (B) 핵 수입에서 Ran-GTP의 역할 — 핵 안에서 receptor-cargo 결합을 해리.
Fig 12-60. Ran-GDP/Ran-GTP 구획화. (A) RanGAP(세포질)/RanGEF(핵)의 위치 차이가 기울기를 유지. (B) 핵 수입에서 Ran-GTP의 역할 — 핵 안에서 receptor-cargo 결합을 해리.
17. 핵 수입 (Nuclear Import) 메커니즘
Ran-GTP cycle & Transport Through NPC 참조
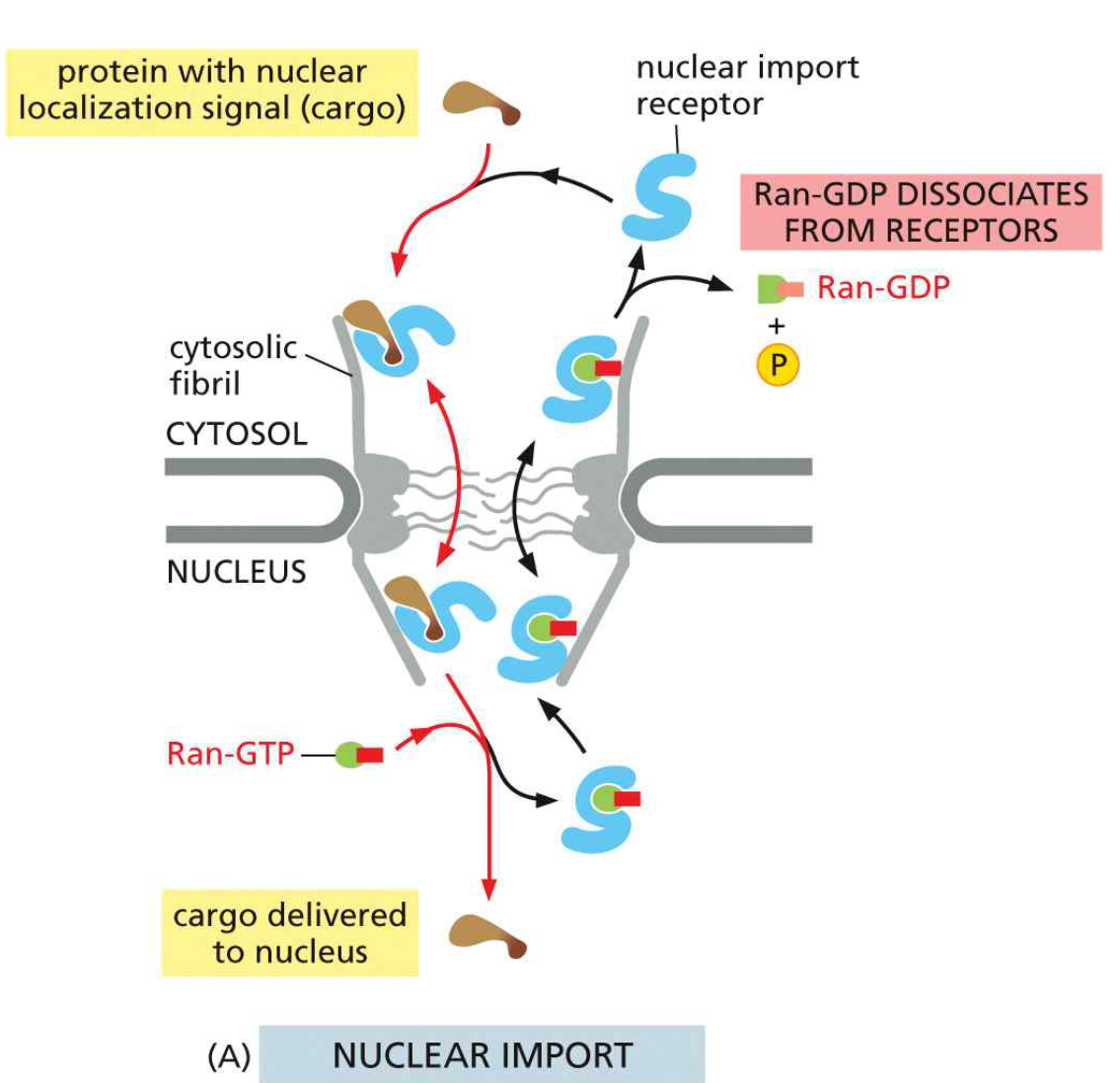
- 세포질에서 importin이 NLS cargo와 결합 (Ran-GDP 상태에서 친화력 높음)
- Importin–cargo 복합체가 NPC의 cytosolic fibrils에 결합
- FG repeat mesh를 통과하여 핵 안으로 이동
- 핵 안에서 Ran-GTP가 importin에 결합 → cargo 해리 (방출)
- Importin–Ran-GTP 복합체가 세포질로 되돌아감
- 세포질 RanGAP이 Ran-GTP → Ran-GDP 가수분해
- Ran-GDP가 importin에서 해리 → importin 재사용
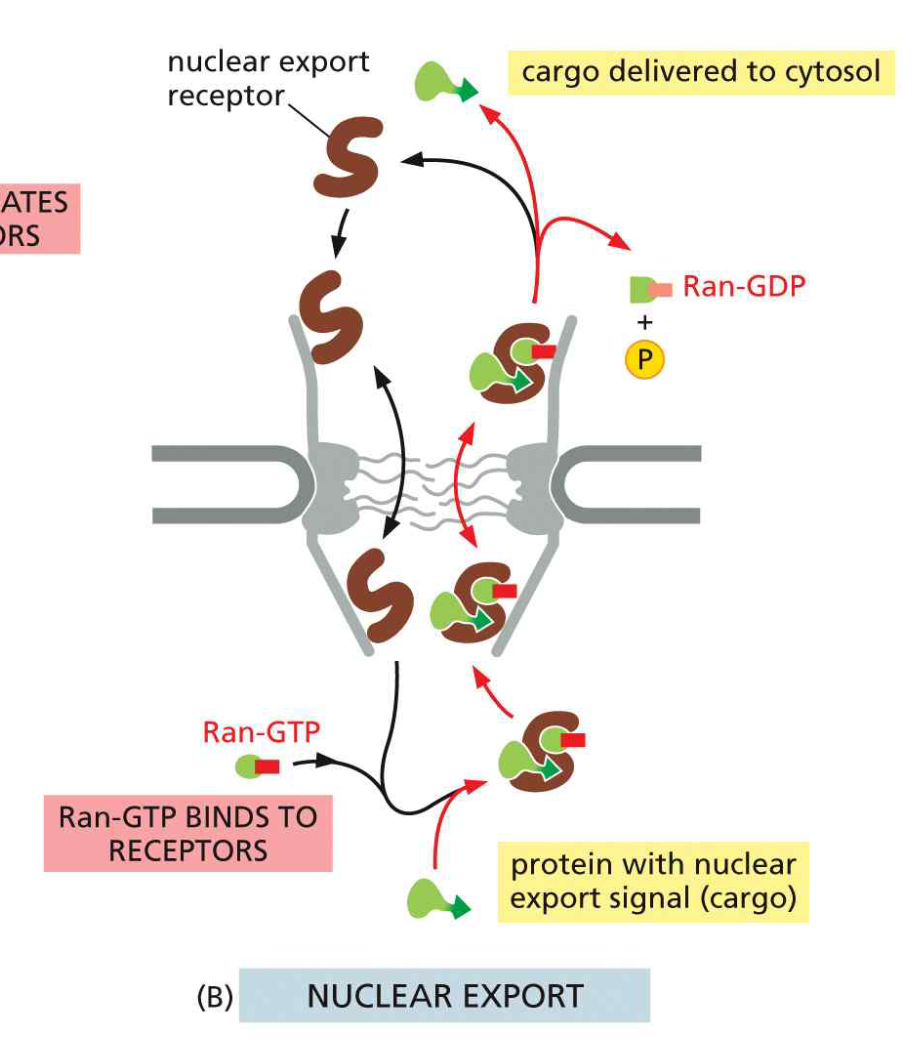
18. 핵 수출 (Nuclear Export) 메커니즘
- 핵 안에서 Ran-GTP가 exportin–NES cargo 결합을 촉진 (삼중 복합체 형성)
- Exportin–cargo–Ran-GTP 복합체가 NPC를 통해 세포질로 이동
- 세포질 RanGAP이 Ran-GTP → Ran-GDP 가수분해
- Exportin 구조 변화 → cargo와 Ran-GDP 모두 세포질에 방출
- Free exportin + Ran-GDP는 핵으로 재수입
Ran-GTP의 역할 정리: Import에서는 cargo 해리(release), Export에서는 cargo 결합(complex formation)
19. NPC 수송의 조절 — Dorsal protein (Drosophila)
Dorsal protein production control 참조
- 초기 초파리 배아는 다핵 공동세포질(syncytium) 상태
- Dorsal 단백질: 세포질 전체에 균일하게 합성되지만, 기능하려면 핵 안으로 들어가야 함
- 배아의 배쪽(ventral) 핵에는 Dorsal이 농축, 등쪽(dorsal) 핵에서는 배제
- → 핵 수송의 차별적 조절이 등-배 축(dorsal-ventral axis) 형성을 결정
20. NPC 수송의 조절 — NF-AT와 T 세포 활성화
Nuclear import control during T-cell activation 참조
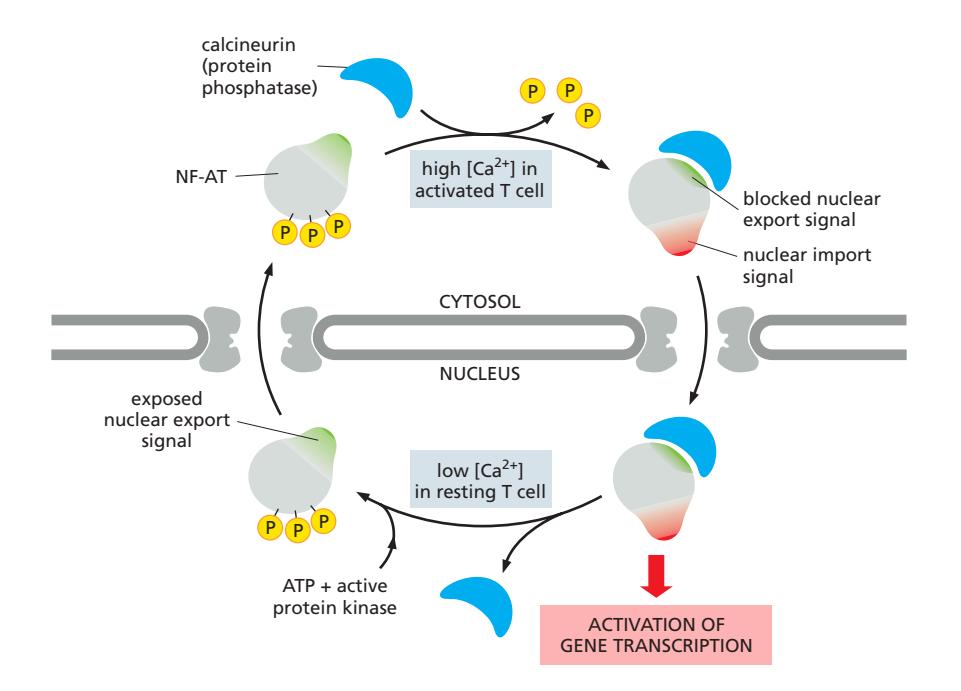 Fig 12-63. T 세포 활성화 중 NF-AT의 핵 수입 조절.
Fig 12-63. T 세포 활성화 중 NF-AT의 핵 수입 조절.
NF-AT (Nuclear Factor of Activated T cells): T 세포 활성화 관련 유전자 전사 조절 인자
| 상태 | 인산화 | NLS | NES | 위치 |
|---|---|---|---|---|
| 휴지 (resting) | 인산화됨 | 마스킹(inactive) | 노출(active) | 세포질 |
| 활성화 (activated) | 탈인산화됨 | 노출(active) | 마스킹(inactive) | 핵 |
활성화 과정:
- 항원 자극 → 세포 내 Ca²⁺ 농도 상승
- Calcineurin (Ca²⁺-dependent phosphatase) 활성화 → NF-AT 탈인산화
- NLS 노출 / NES 차단 → NF-AT–calcineurin 복합체가 핵으로 수입
- T 세포 활성화 유전자 전사 활성화
Off switch: Ca²⁺ 감소 → calcineurin 해리 → NF-AT 재인산화 → 세포질로 재이동
임상 적용: Cyclosporin A, FK506 (Tacrolimus) → calcineurin 억제 → NF-AT 핵 이동 차단 → T 세포 활성화 억제 → 면역억제제 (장기이식 거부 반응 방지)
21. 유사분열 시 핵막 분해와 재조립
Nuclear Envelope Disassembly 참조
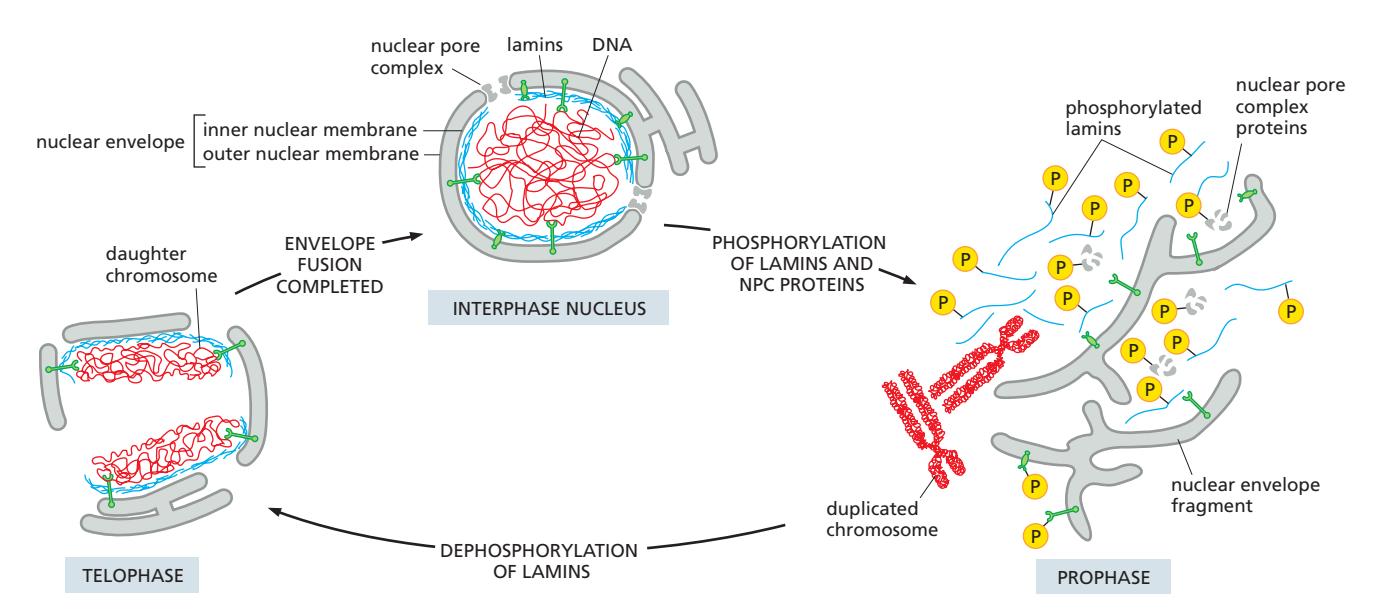 Fig 12-65. 유사분열 중 핵막과 nuclear lamina의 분해·재형성 과정.
Fig 12-65. 유사분열 중 핵막과 nuclear lamina의 분해·재형성 과정.
분해 (유사분열 시작 — Prophase)
- CDK1–cyclin B 활성화 (M phase)
- Lamin 인산화 → nuclear lamina 분해 → nuclear envelope 붕괴
- Nucleoporin, inner nuclear membrane 단백질도 인산화 → NPC 해체
- 핵막 단백질이 ER 막 전반으로 분산; 핵 단백질이 세포질과 혼합
재조립 (유사분열 말기 — Telophase)
- CDK1 불활성화 → lamin, nucleoporin 탈인산화
- RanGEF가 chromatin에 결합 유지 → 염색체 주변 Ran-GTP cloud 형성
- Ran-GTP가 위치 표지 → 염색체 표면에 NPC 단백질 모집 및 새 NPC 조립
- 탈인산화된 lamin이 chromatin에 재결합 → inner nuclear membrane 단백질 모집
- ER 막이 염색체 세트를 감싸며 측면 융합 → 봉합된 nuclear envelope 재형성 (engulfment)
- NLS 수입 재개 → 핵 단백질 구성 복원
세균·효모 등 많은 생물: closed mitosis (유사분열 중 핵막 유지, 핵 분열)
전체 비교 요약
| 소기관 | 수입 방식 | Signal | Targeting signal 제거 여부 | 에너지 |
|---|---|---|---|---|
| ER | Co-translational (대부분) | N-말단 signal sequence | 절단됨 (signal peptidase) | GTP (SRP/SR) |
| Peroxisome | Post-translational, folded | PTS1 (C-말단) / PTS2 (N-말단) | 유지 | ATP (Pex recycling) |
| Mitochondria | Post-translational, unfolded | MTS (N-말단, 양전하 α-나선) | 절단됨 (MPP) | Δψ + ATP |
| Nucleus | Post-translational, folded | NLS (Lys/Arg-rich) | 유지 | GTP (Ran cycle) |