ER-Associated Degradation (ERAD)
ER-associated degradation (ERAD)은 misfolded되거나 unassembled 단백질을 ER에서 cytosol로 retrotranslocation하여 proteasome에서 분해하는 quality control mechanism이다.1
개요
필요성
- Chaperone의 도움에도 불구하고 일부 단백질은 올바르게 접히지 못함
- Misfolded protein의 축적은 ER stress와 세포 독성 유발
- Unassembled subunit도 제거 필요
기본 원리
- Misfolded protein을 ER에서 제거
- Cytosol의 proteasome으로 분해
- ER의 protein-processing capacity 유지
ERAD 메커니즘
1. Substrate Recognition
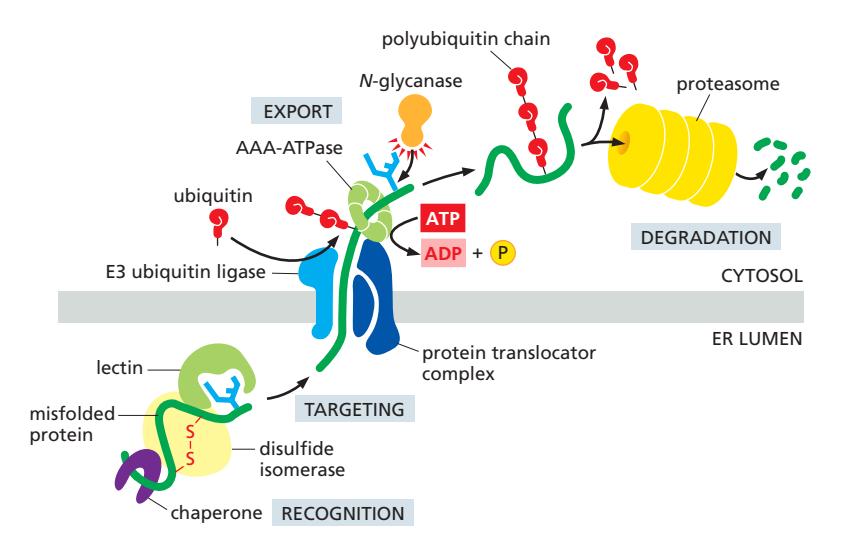
Recognition signals:
- Trimmed N-linked oligosaccharides (reduced mannose)
- Exposed hydrophobic regions
- Free sulfhydryl groups
- Unassembled oligomeric subunits
Recognition factors:
Lectins
- ER-lumenal lectin이 trimmed oligosaccharide 인식
- Binding site on membrane-embedded translocator
- Substrate를 retrotranslocation machinery로 guide
Chaperones
- BiP, Calnexin and Calreticulin
- Unfolded protein과 상호작용 유지
- Aggregation 방지
- ERAD machinery로 전달
Disulfide Isomerases
- PDI family members
- Disulfide bond 환원
- Polypeptide의 complete unfolding
- Linear chain이 translocator 통과 가능
2. Retrotranslocation
Translocator complexes:
- Multiple translocator 존재
- E3 ubiquitin ligase를 항상 포함
- Different subsets of misfolded protein 처리
- ER membrane에 embedded
Mechanism:
- Recognition: Misfolded protein이 translocator complex와 결합
- Unfolding: Chaperone와 disulfide isomerase가 단백질 unfold
- Threading: Unfolded polypeptide가 translocator channel 통과
- Export: Cytosol로 이동
3. Ubiquitylation
E3 ubiquitin ligase:
- Translocator complex의 일부
- Emerging polypeptide에 polyubiquitin 부착
- Cytosol 측면에서 작용
Function of ubiquitin:
- Proteasome recognition signal
- Backsliding into ER 방지
- AAA-ATPase의 binding handle
4. Extraction
AAA-ATPase:
- Hexameric ATPase complex
- Ubiquitylated substrate 인식
- ATP hydrolysis로 pulling force 제공
Process:
- Polypeptide를 translocator에서 완전히 추출
- Cytosol로 pulling
- Unfolded state 유지
5. Deglycosylation
N-glycanase:
- Cytosolic enzyme
- N-linked oligosaccharide를 en bloc 제거1
- Retrotranslocation 후 작용
6. Proteasomal Degradation
- Polyubiquitin tag가 proteasome으로 guide
- Proteasome에서 peptide로 분해
- Amino acid 재활용
Substrate Selection Mechanism
Time-Based Selection
Mannosidase timer:
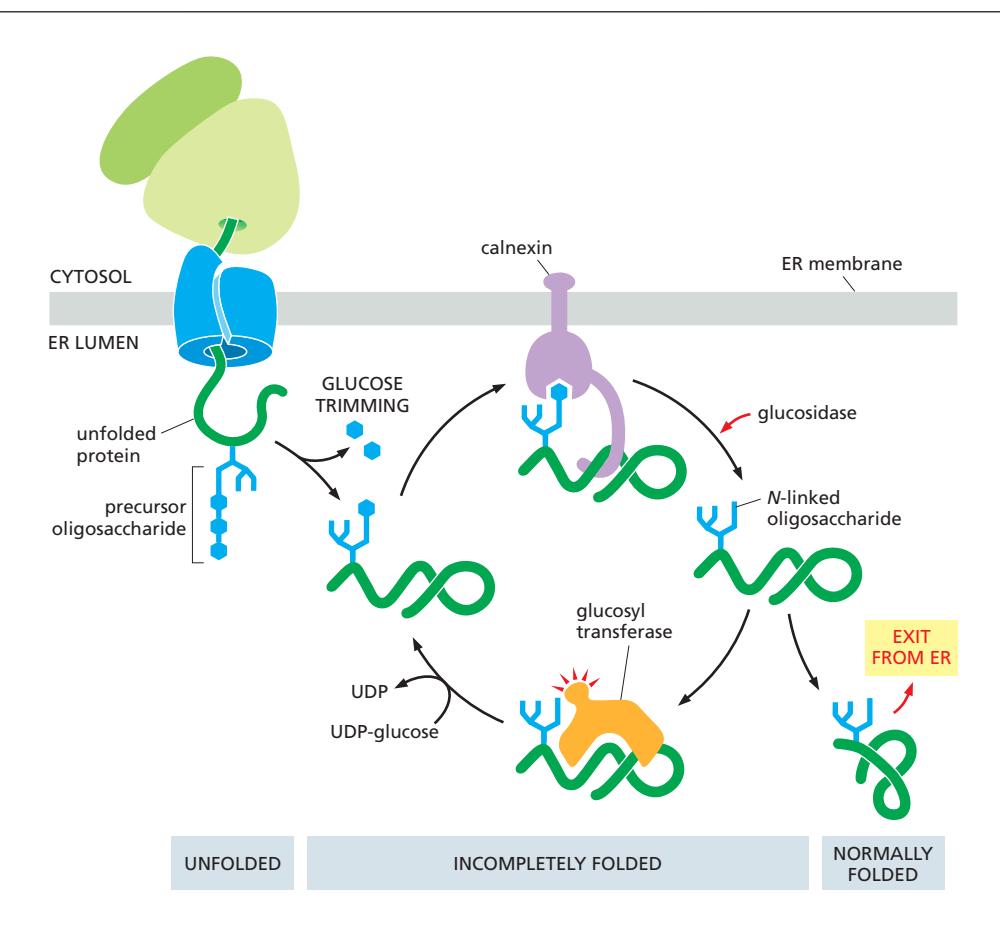
- 단백질이 ER에서 folding 시도
- Mannosidase가 천천히 terminal mannose 제거
- Trimmed oligosaccharide 생성
- ERAD lectin이 인식
Discrimination:
- Fast folding: Mannosidase 작용 전 ER 빠져나감 → 생존
- Slow folding: Mannose trimming 발생 → ERAD로 향함
State-Based Selection
Folding intermediates vs. Misfolded:
- Folding intermediate:
- Temporary unfolded region
- Chaperone와 일시적 상호작용
- 결국 properly fold될 가능성
- Misfolded protein:
- Persistent unfolded region
- Prolonged chaperone binding
- Mannose trimming
- ERAD로 routing
Multiple ERAD Pathways
Pathway Diversity
Different translocator complexes:
- 다양한 E3 ubiquitin ligase 포함
- Different substrate specificity
- Misfolding의 다양한 형태 처리
Substrate classes:
- ERAD-L (Lumen): Soluble lumenal protein
- ERAD-M (Membrane): Membrane protein with lumenal defect
- ERAD-C (Cytosol): Membrane protein with cytosolic defect
Membrane Protein ERAD
특별한 고려사항:
- Lateral exit from ER membrane
- Lipid bilayer 내에서 translocator engagement
- Transmembrane domain의 extraction
생리적 역할
1. Quality Control
- Defective protein 제거
- Only functional protein이 secretory pathway 진입
- Downstream organelle 보호
2. ER Capacity Maintenance
- Misfolded protein의 축적 방지
- ER lumen space 확보
- Chaperone availability 유지
3. Regulatory Degradation
- Short-lived regulatory protein 분해
- Metabolic enzyme의 feedback regulation
- Signal transduction component 조절
Pathological Implications
1. Genetic Diseases
- Cystic fibrosis의 원인
- Misfolded CFTR channel
- ERAD에 의해 과도하게 분해
- 일부 functional activity는 유지
2. Protein Aggregation Diseases
- ER quality control 실패
- Aggregate formation
- Cell toxicity
- Neurodegenerative disease
3. Viral Exploitation
- 일부 virus가 ERAD hijack
- MHC class I molecule을 degradation
- Immune evasion
ERAD와 UPR의 연결
Coordinated Response
UPR activation:
- Misfolded protein 축적
- IRE1, PERK, ATF6 경로 활성화
ERAD upregulation:
- ERAD component의 transcription 증가
- Degradation capacity 향상
- ER stress 완화
Feedback Loop
- ERAD 증가 → Misfolded protein 감소 → UPR 감소
- Persistent stress → Sustained UPR → Apoptosis
실험적 접근
Cell-Free System
- Microsome으로 ERAD 재구성
- Individual component의 역할 분석
- Mechanism 규명
Genetic Approaches
- ERAD component knockout
- Substrate accumulation 관찰
- Pathway dissection
관련 개념
- Protein folding in ER
- Oligosaccharides
- Unfolded Protein Response
- Mannosidase
- BiP
- Calnexin and Calreticulin
- Ubiquitin-proteasome system
Footnotes
-
2023 중간 26번 — ③ 옳음: 올바르게 접히지 않은 단백질은 ER에서 세포질로 retrotranslocation되어 N-linked glycosylation이 제거(N-glycanase)되고 polyubiquitination 후 proteasome에서 분해됨(ERAD 경로). ↩ ↩2