N-linked Glycosylation
개요
N-linked glycosylation은 preformed precursor Oligosaccharides가 단백질의 asparagine 잔기에 en bloc (한 덩어리로) 부착되는 과정이다. ER에서 일어나는 가장 흔한 glycosylation 형태이다.
Precursor Oligosaccharides 구조
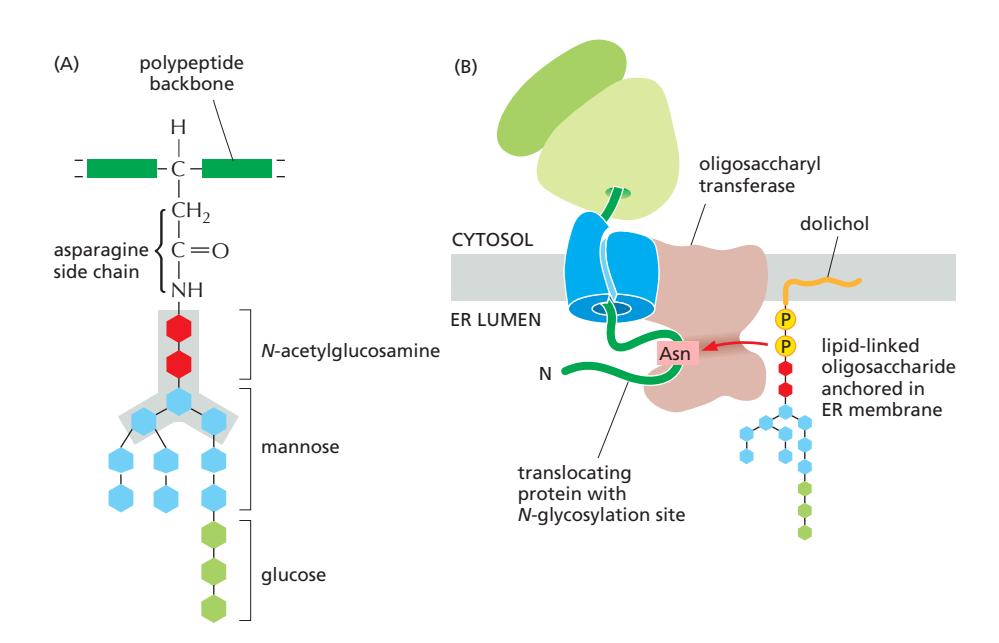
조성
총 14개의 sugar로 구성: - 2 N-acetylglucosamine (GlcNAc) - 9 Mannose (Man) - 3 Glucose (Glc)
구조: Glc₃Man₉GlcNAc₂
Core region
회색 상자로 표시된 5개 sugar:
- 2 GlcNAc
- 3 Mannose
중요성:
- Golgi에서의 extensive trimming 후에도 남는 부분
- 많은 glycoprotein에 공통적으로 존재
Dolichol 합성 과정
1. Dolichol Lipid Anchor
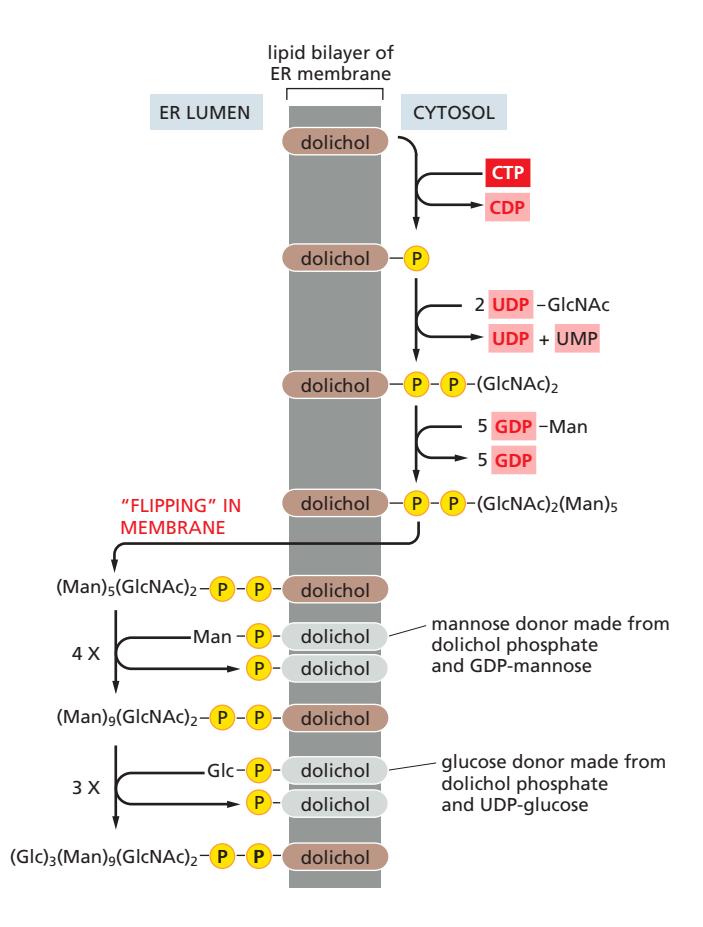
Dolichol의 특징:
- Polyisoprenoid lipid (22개의 5-carbon unit)
- 매우 소수성
- 막을 3번 이상 관통할 수 있는 길이
- Oligosaccharides를 막에 단단히 고정
부착 방식:
- Pyrophosphate bridge를 통해 첫 번째 sugar 연결
- High-energy bond → 단백질 전이 시 에너지원
2. 단계별 조립 (Step-by-step Assembly)
Cytosolic side (ER membrane의 세포질 쪽):
- First sugar → Dolichol-P
- Sugar-by-sugar addition
- GlcNAc₂Man₅까지 합성
Membrane flip:
- (Man)₅(GlcNAc)₂-lipid intermediate가 flipped
- Transporter에 의해 lumenal face로 이동
Lumenal side (ER lumen 쪽):
- 추가적인 sugar 부착
- Dolichol-P-glucose와 dolichol-P-mannose 사용
- 완전한 Glc₃Man₉GlcNAc₂ 구조 완성
3. Activated Sugar Donors
Cytosolic side:
- UDP-GlcNAc
- GDP-mannose
Lumenal side:
- Dolichol-P-glucose
- Dolichol-P-mannose (이들은 cytosol에서 합성된 후 flip됨)
단백질로의 전이
Oligosaccharyl Transferase(OST)에 의해
위치와 구조:
- ER membrane의 transmembrane enzyme complex
- Sec61 complex와 결합 : Co-translational하다!
- 13개의 transmembrane α-helix
- 큰 ER lumenal domain
기능적 배치:
- Active site가 ER lumen에 노출
- Nascent polypeptide와 dolichol-Oligosaccharides 모두 결합
전이 반응

Target sequence:
Asn-X-Ser/Thr
- Asn: Asparagine (attachment site)
- X: Any amino acid except proline
- Ser/Thr: Serine or Threonine
반응 메커니즘:
- Asparagine이 oligosaccharyl transferase의 tunnel로 진입
- Amide bond의 nitrogen이 평면 밖으로 비틀림
- 반응성 증가
- Oligosaccharides가 intact unit로 전이
- Dolichol-pyrophosphate 방출
Co-translational Modification이다
시기:
- Polypeptide가 ER lumen에 진입하는 즉시
- Translation이 진행되는 동안
- Signal sequence 제거와 동시 또는 직후
장점:
- 빠른 modification
- Folding 전에 완료
- Aggregation 방지
Processing in the ER
Glucose Trimming
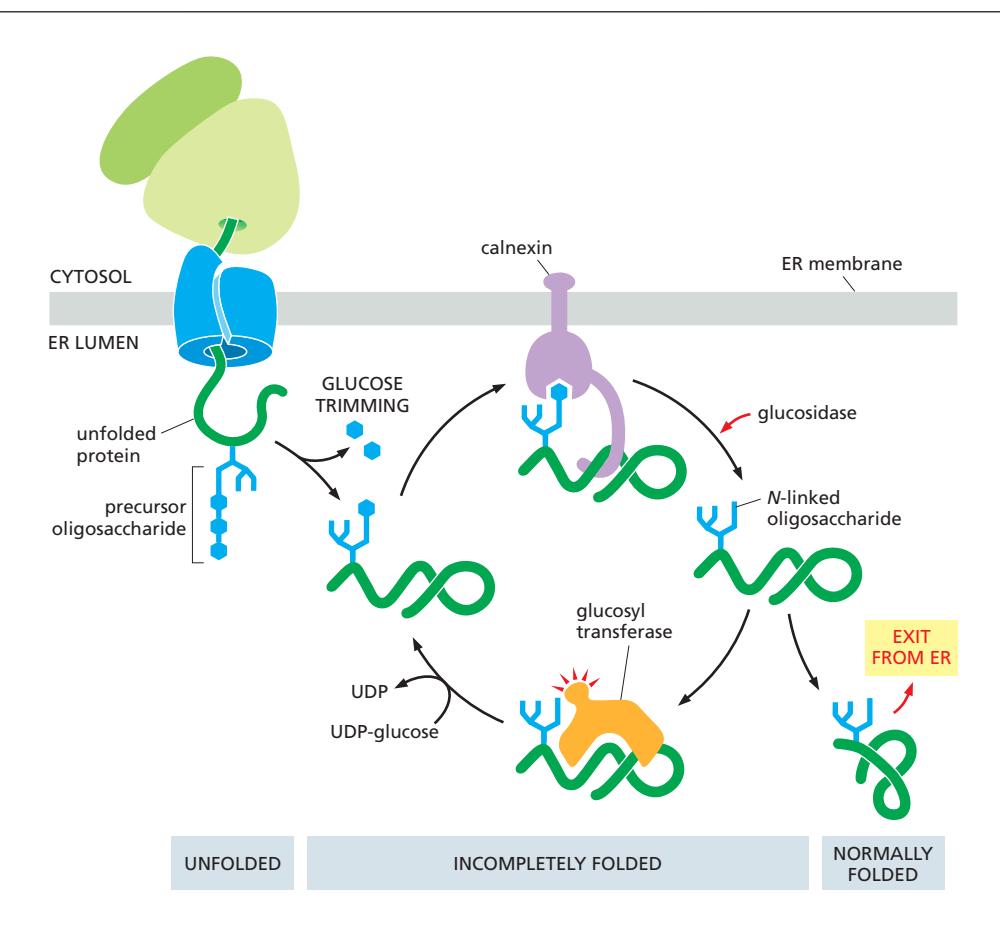
단계:
- glucosidase가 2개의 glucose 제거
- Glc₁Man₉GlcNAc₂ 생성(포도당 하나 남음)
- 이 구조가 Calnexin and Calreticulin에 의해 인식됨
Folding cycle:
Glc₃Man₉GlcNAc₂ (newly attached)
↓ (glucosidases)
Glc₁Man₉GlcNAc₂ (binds calnexin/calreticulin)
↓ (glucosidase)
Man₉GlcNAc₂ (released from calnexin/calreticulin)
↓ (glucosyl transferase, if misfolded)
Glc₁Man₉GlcNAc₂ (re-binds calnexin/calreticulin)
이 cycle은 Quality control of ER protein folding 참조
Mannose Trimming
시기: Protein이 ER에 오래 머무를 때
의미:
- Trimmed mannose = folding 문제 신호
- ER-associated degradation (ERAD) pathway로 전환
- Mannosidase가 terminal mannose 제거
Further Processing in Golgi
ER을 벗어난 후:
- Golgi에서 extensive modification
- 다양한 Oligosaccharides 구조 생성
- Complex, hybrid, high-mannose type으로 분류
(자세한 내용은 Golgi에서의 N-linked 당화 processing 참조)
N-linked Glycosylation의 기능
1. Quality Control Tag
- Glucose의 presence/absence가 folding state 표시
- calreticulin recruitment
- ER retention of misfolded proteins ⇒ proper protein folding in ER
2. Protein Stability and Solubility
3. Cell-Cell Recognition
4. 필수성
일부 단백질에서:
- Proper folding에 필수적
- 위치는 중요하지 않음 (어느 Asn-X-Ser/Thr이든 가능)
- Glycosylation 자체가 중요
vs O-linked glycosylation
주요 차이점 비교 테이블
| 특징 | N-연결 당화 (N-linked) | O-연결 당화 (O-linked) |
|---|---|---|
| 결합 아미노산 | **아스파라긴(Asn, N)**의 측쇄 질소() | 세린(Ser, S) 또는 **트레오닌(Thr, T)**의 수산기 산소() |
| 발생 장소 | **소포체(ER)**에서 시작 (골지에서 수정) | 주로 **골지체(Golgi)**에서 발생 |
| 전달 방식 | 14개의 당 덩어리를 한꺼번에 전달 | 당을 하나씩 차례대로 붙임 |
| 지질 운반체 | 돌리콜(Dolichol) 사용 | 사용 안 함 |
| 인식 서열 | Asn-X-Ser/Thr (X는 Pro 제외) | 특정 공통 서열이 명확하지 않음 |
O-연결 당화 (O-linked Glycosylation)
단백질의 소수성 부위나 특정 구조가 완성된 후, 골지체에서 당 전이효소(Glycosyltransferase)들이 하나씩 당을 추가합니다.
- 특징: 주로 **뮤신(Mucin)**과 같은 점액 성분 단백질이나 프로테오글리칸 형성에 중요합니다. 당 사슬이 짧은 경우도 있지만, 매우 길고 복잡하게 자라나기도 합니다.
관련 개념
- Glycosylation
- Oligosaccharides
- Dolichol
- Oligosaccharyl transferase
- Calnexin and Calreticulin
- Quality control of ER protein folding
- Sec61 complex
Footnotes
-
2023 중간 19번 — ① 틀림: glycosylation은 세포 인식(lectin binding, receptor recognition)을 촉진하며 신호전달을 차단하지 않음. ② 틀림: oligosaccharide는 입체 장애(steric hindrance)로 protease 접근을 차단하여 분해를 억제함. ③ 틀림: N-linked glycosylation은 aggregation을 방지하여 folding을 보조함. ↩ ↩2 ↩3