Chapter 13-1: Intracellular Membrane Traffic 정리본
5주차 강의노트 기반 | 출처: chapter 13 강의 I 2026.pdf
1. Intracellular Membrane Traffic 개요
Intracellular membrane traffic은 세포 내 막으로 둘러싸인 구획들 사이에서 일어나는 물질 이동 체계이다. 크게 세 방향으로 나뉜다:
- Secretory (biosynthetic) pathway: ER → Golgi → plasma membrane / 분비 / lysosome
- Endocytic pathway: Plasma membrane → endosome → lysosome
- Retrieval pathway: 잘못 운반된 단백질을 원래 compartment로 되돌리는 경로
- Autophagy: 세포 자신의 성분을 lysosome으로 분해
모든 경로는 transport vesicle을 통해 이루어진다. Vesicle은 donor membrane에서 budding하여 target membrane과 fusion한다.
2. Vesicle Transport의 3단계
Vesicle transport는 다음 세 단계로 구성된다:
- Budding (출아): Coat protein이 donor membrane에서 vesicle을 형성
- Transport: Vesicle이 cytoskeleton을 따라 target compartment로 이동
- Fusion (융합): Vesicle이 target membrane과 융합하여 cargo 전달
Coated Vesicle의 종류
| Coat | 위치 | 방향 |
|---|---|---|
| Clathrin | Plasma membrane, TGN | Endocytosis, TGN→endosome |
| COPI | Golgi | Retrograde (Golgi→ER) |
| COPII | ER | Anterograde (ER→Golgi) |
3. Clathrin Coat
Clathrin은 가장 잘 알려진 coat protein이다.
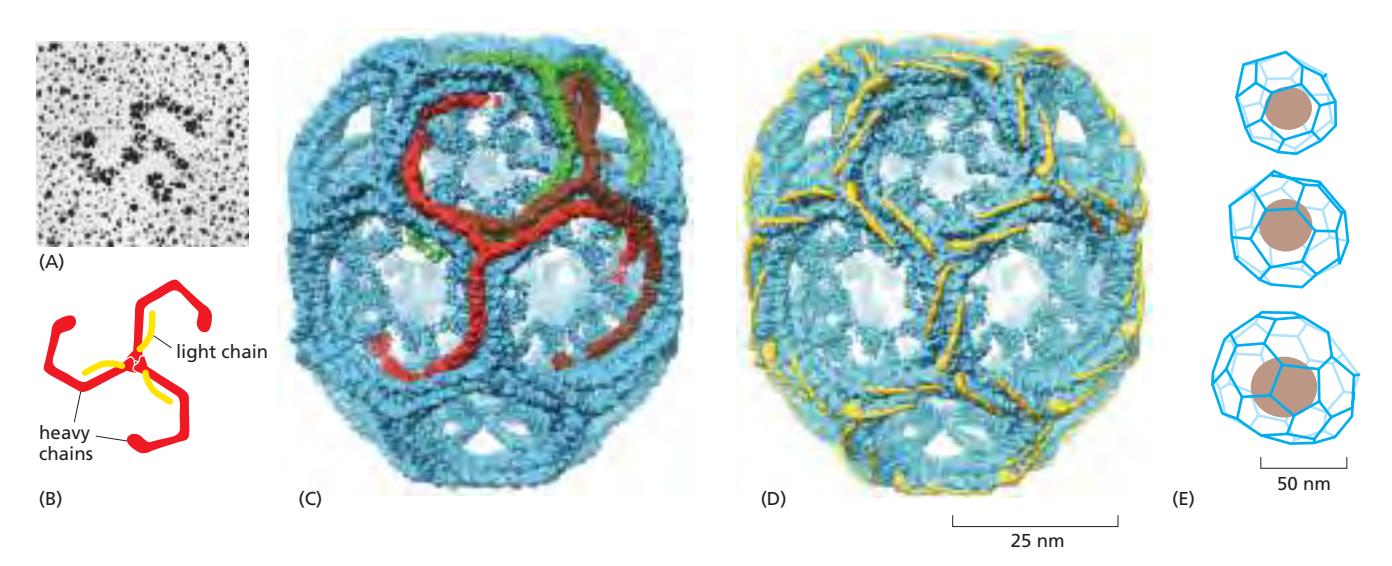
구조: Triskelion
- Triskelion: 3개의 heavy chain + 3개의 light chain으로 구성
- Heavy chain은 세 방향으로 뻗은 삼각형 구조
- 여러 triskelion이 모여 hexagon과 pentagon으로 구성된 polyhedral cage 형성 (축구공 모양)
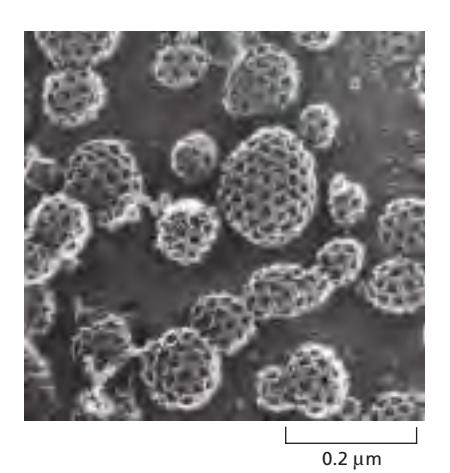
조립과 분해 (Assembly/Disassembly)
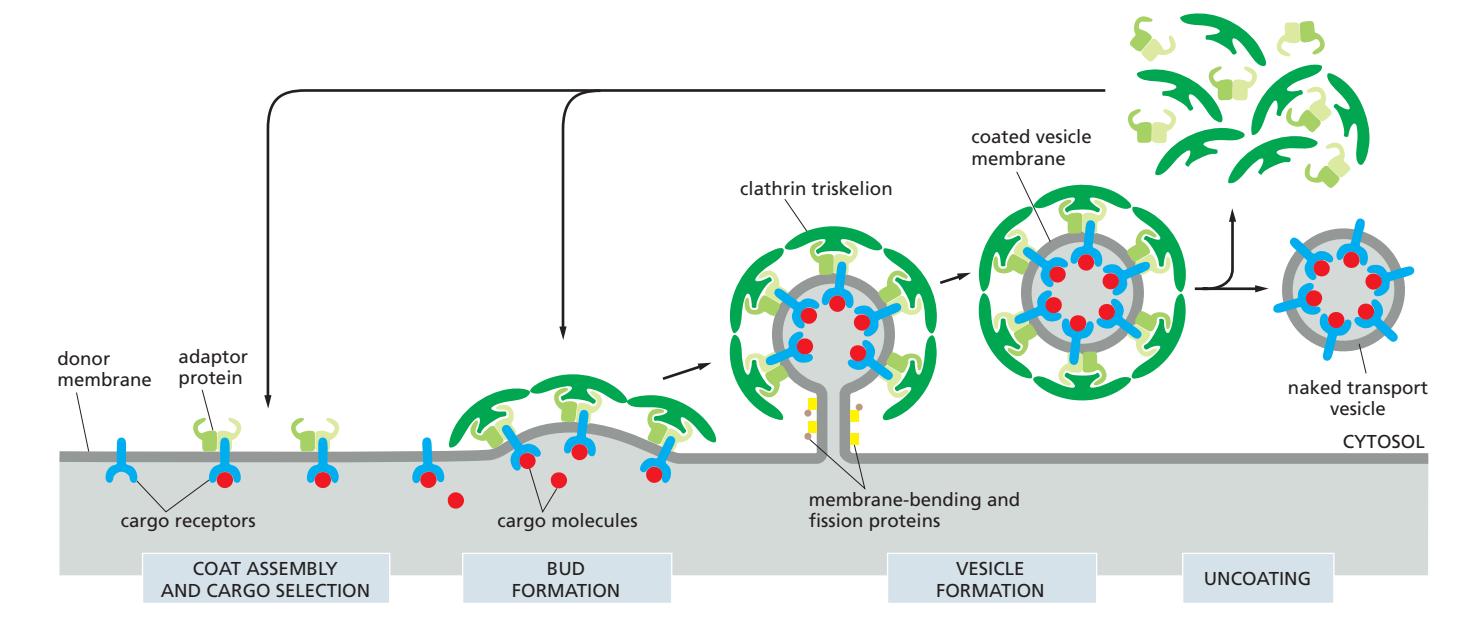
Coat assembly:
- AP2 adaptor protein이 membrane에 결합
- Adaptor가 cargo receptor와 상호작용
- Clathrin triskelion이 recruit되어 coat 형성
- Membrane curvature 증가하며 coated pit 형성
- Membrane-bending protein과 fission protein (dynamin) recruit → pinch off
Coat disassembly:
- Vesicle이 budding된 직후 발생 (목적지 도달 후가 아님)
- hsp70 chaperone이 ATP hydrolysis 에너지로 clathrin coat를 물리적으로 제거
- Phosphoinositide phosphatase가 PI(4,5)P₂를 분해하여 adaptor protein의 막 결합 약화
4. AP2 어댑터 단백질
AP2는 clathrin coat 형성의 핵심 어댑터 단백질이다.
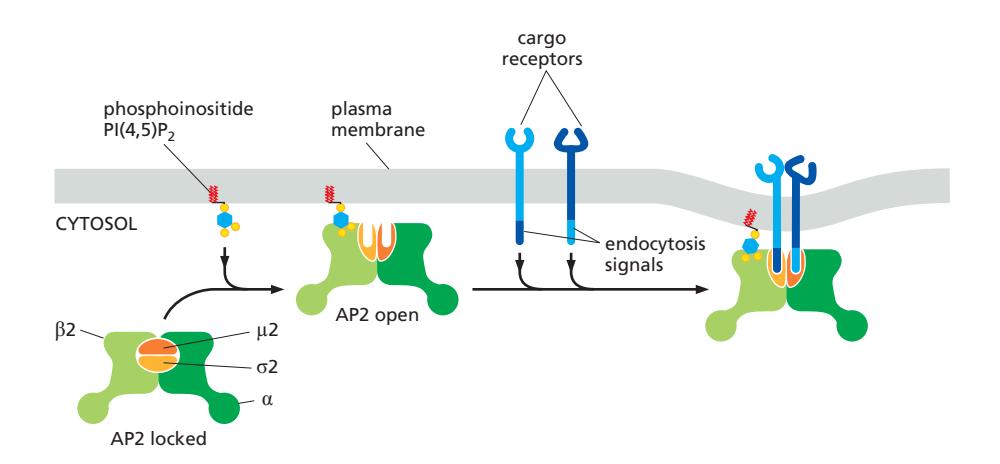
활성화 메커니즘
- 초기 상태 (locked): Cargo binding site가 차단된 비활성 구조
- PI(4,5)P₂에 결합 → conformational change → cargo binding site 노출
- Cargo motif 인식:
- YXXφ (tyrosine-based)
- dileucine motif ([DE]XXXL[LI])
5. Phosphoinositides (PIPs): Organelle Identity Marker
Phosphoinositides (PIPs)는 막 지질의 소수 성분(<10%)이지만 organelle identity를 결정하는 핵심 marker이다.
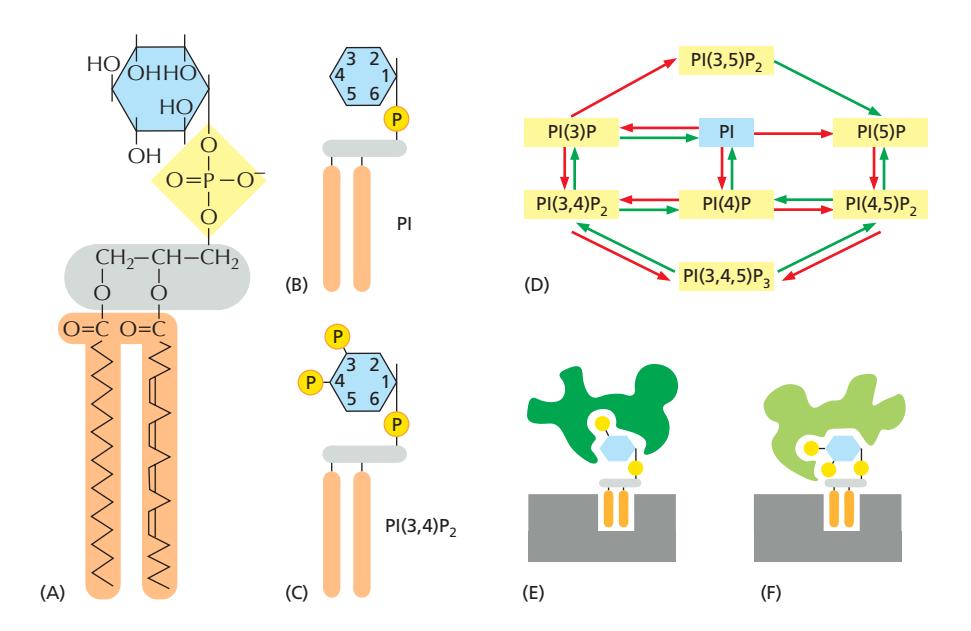
구조
- PI (phosphatidylinositol): inositol sugar head group 보유
- Inositol ring의 3’, 4’, 5’ position의 hydroxyl group이 인산화되어 다양한 PIP 생성
Compartment별 분포
| Compartment | 주요 PIP |
|---|---|
| Plasma membrane | PI(4,5)P₂ |
| Early endosome | PI(3)P |
| Late endosome | PI(3)P + PI(3,5)P₂ |
| Golgi | PI(4)P |
| ER | PI |
- 모두 cytosolic leaflet에 위치
- 각 organelle에 특이적인 kinase와 phosphatase의 분포가 PIP 특이성 결정
- PIP-binding domain을 가진 단백질이 특정 organelle로 선택적으로 recruit됨
6. Membrane-bending Proteins
Membrane-bending protein은 vesicle budding 시 막을 구부리는 역할을 한다.
BAR Domain Dimers
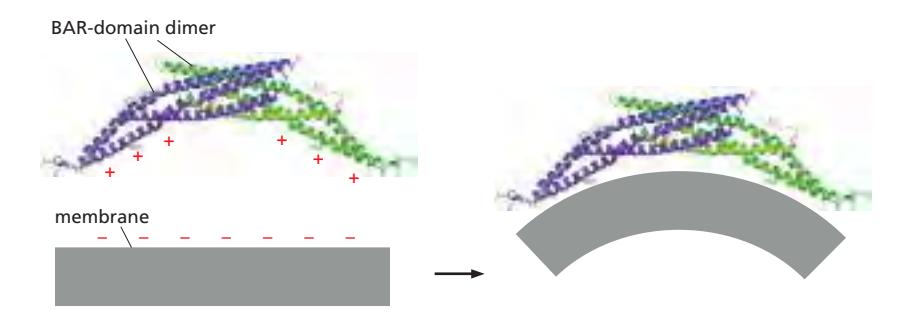
- 두 개의 subunit이 crescent-shaped dimer 형성
- Positively charged inner surface가 negatively charged lipid head group과 상호작용 → membrane을 구부림
- 굽어진 내면이 tube 형태의 membrane에 결합
- 결합 자체가 membrane에 curvature 부여
- 이미 구부러진 막에 preferential하게 결합하여 곡률 증폭
- 일부 BAR-domain protein: PIP-binding domain 보유 → 특정 membrane으로 targeting
Vesicle Neck에서의 기능
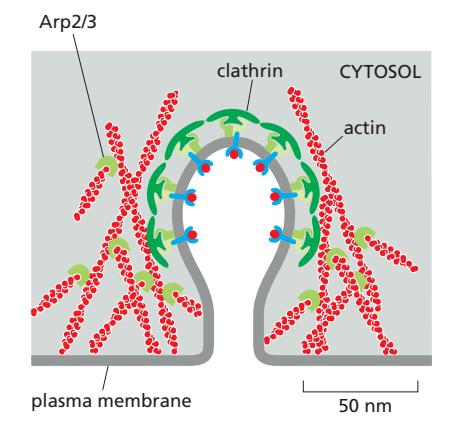
Budding vesicle neck에서:
- Sharp membrane bend 안정화
- Clathrin machinery와 함께 local actin assembly 자극
- Growing actin filament이 vesicle 주변 membrane을 push
- Vesicle이 membrane으로부터 propelled됨
7. Dynamin: Vesicle Fission
Dynamin은 budding vesicle을 donor membrane으로부터 분리(pinch off)하는 GTPase이다.
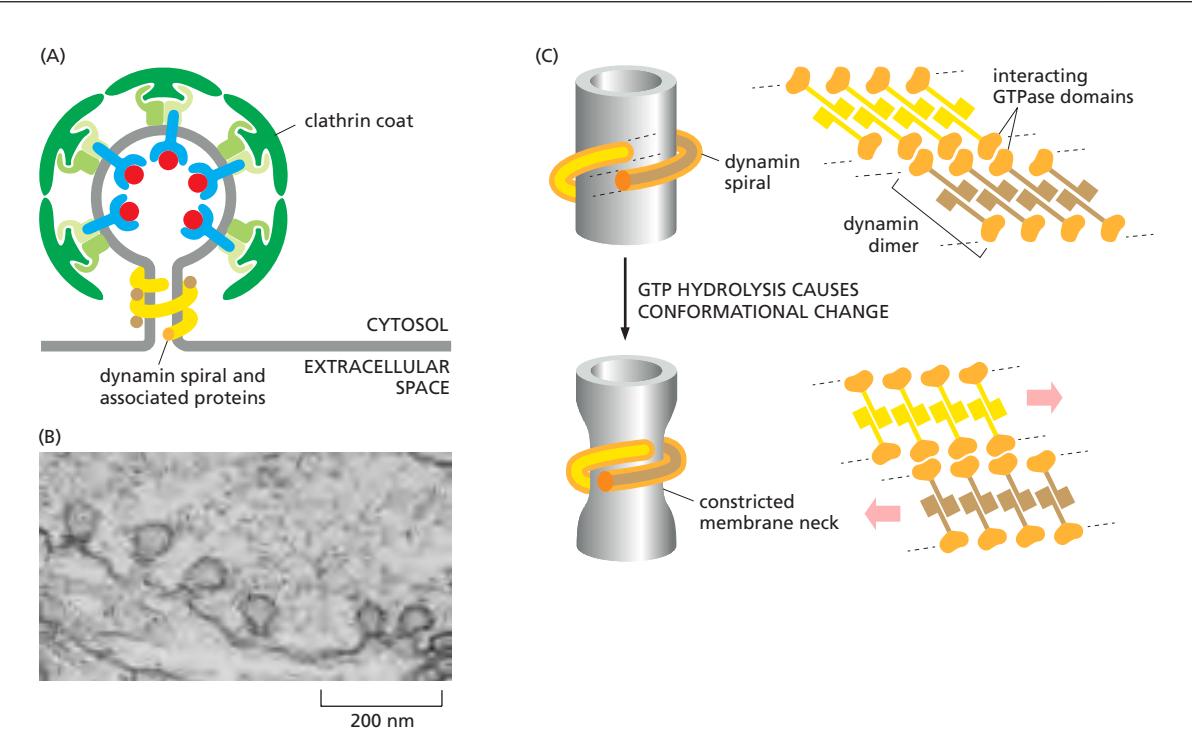
구조
- GTPase domain: GTP hydrolysis 조절
- PH domain (PI(4,5)P₂-binding domain): 막의 PI(4,5)P₂에 결합
- Middle domain/stalk: oligomerization 담당
작동 메커니즘
Assembly:
- Dynamin이 PI(4,5)P₂에 결합하여 vesicle neck 주위에 ring 형성
- Ring이 spiral structure로 조립 (polymer 형성)
Constriction:
- Bound GTP hydrolysis
- Dynamin의 conformational change
- Dynamin ring constriction → underlying membrane neck constrict
- Fission 완성
Dynamin dimer: G-domain이 adjacent rung의 G-domain과 dimerize → GTPase 활성화 → conformational change → constriction
8. Monomeric GTPases: Coat Assembly 조절
Coat-recruitment GTPase는 특정 compartment에서만 coat assembly를 활성화하는 분자 스위치이다.
종류와 역할
| GTPase | 작동 위치 | 조절하는 coat |
|---|---|---|
| Sar1 | ER membrane | COPII coat |
| ARF proteins | Golgi membrane | COPI coat, Clathrin coat |
GDP/GTP Cycle
- GEF (Guanine nucleotide exchange factor): GDP → GTP 교환 촉매 → 활성화
- GAP (GTPase-activating protein): GTP hydrolysis 촉진 → 불활성화
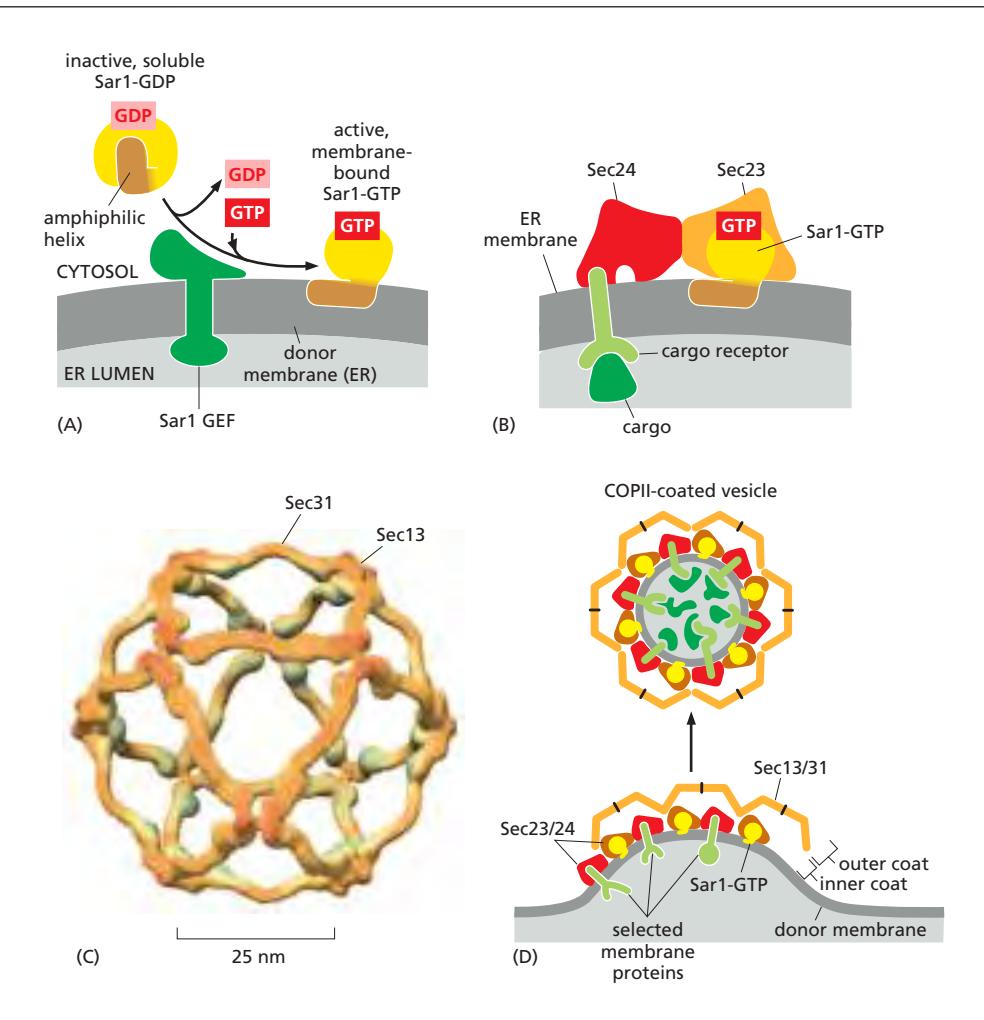
Sar1에 의한 COPII Coat Assembly
- ER membrane embedded Sar1 GEF(Sec12)가 세포질의 Sar1-GDP 활성화
- GEF가 GDP를 방출 → 세포질의 GTP가 결합 → Sar1-GTP 형성
- Sar1의 N-terminal amphiphilic helix 노출 → ER membrane cytoplasmic leaflet에 wedge처럼 삽입
- Sar1-GTP가 Sec23/Sec24 (inner coat, adaptor) 모집
- Sec23/Sec24 위에 Sec13/Sec31 (outer coat) 조립
- Vesicle budding 완성
ARF도 같은 원리: Golgi membrane의 ARF GEF에 의해 활성화 → lipid anchor로 Golgi membrane에 삽입 → COPI/clathrin coat 모집
9. Rab Proteins: 수송 정확도의 핵심
Rab GTPase는 vesicle의 tethering, docking, fusion의 정확도를 담당한다.
Rab의 작동 원리
| 상태 | 결합 분자 | 위치 |
|---|---|---|
| GTP-bound (활성) | Rab effectors | Target membrane |
| GDP-bound (비활성) | GDI | 세포질 |
Rab cycle:
- **GDI (GDP Dissociation Inhibitor)**가 GDP-Rab을 세포질에 유지
- Membrane의 GEF가 GDI로부터 Rab을 떼어내고 GTP와 교환
- GTP-Rab이 membrane에 결합 및 effector 모집
- Effector: tethering factor, motor protein, SNARE 조절인자 등
- GTP 가수분해 후 GDI가 GDP-Rab을 다시 세포질로 추출
Rab5 Domain 형성
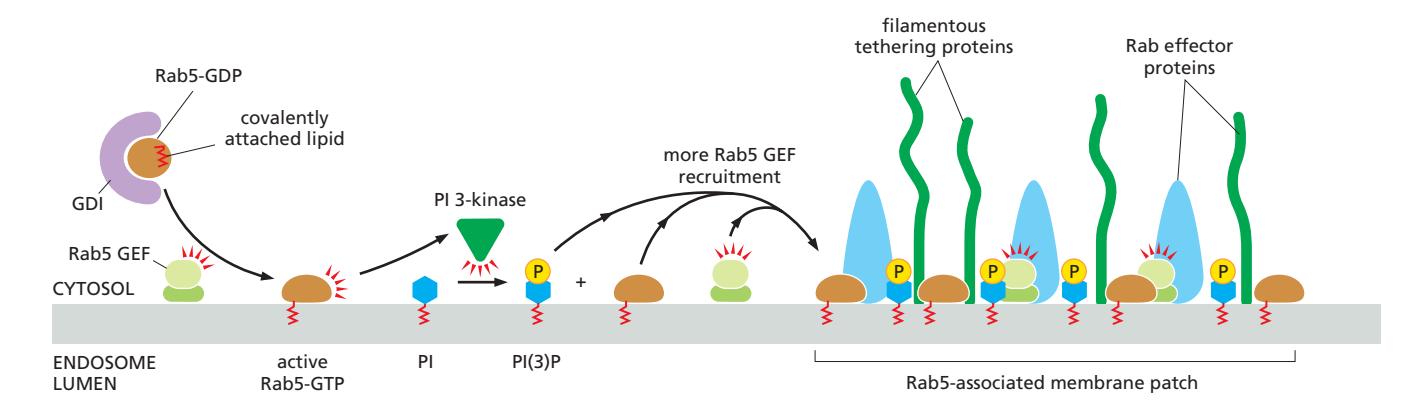
- Rab5가 **PI3K (PI 3-kinase)**를 effector로 모집
- PI3K가 PI(3)P 생성 → PI(3)P-binding protein 추가 모집
- Self-amplifying loop: Rab5-GTP가 더 많은 Rab5-GTP를 모집
- PI(3)P enrichment가 early endosome의 identity 정의
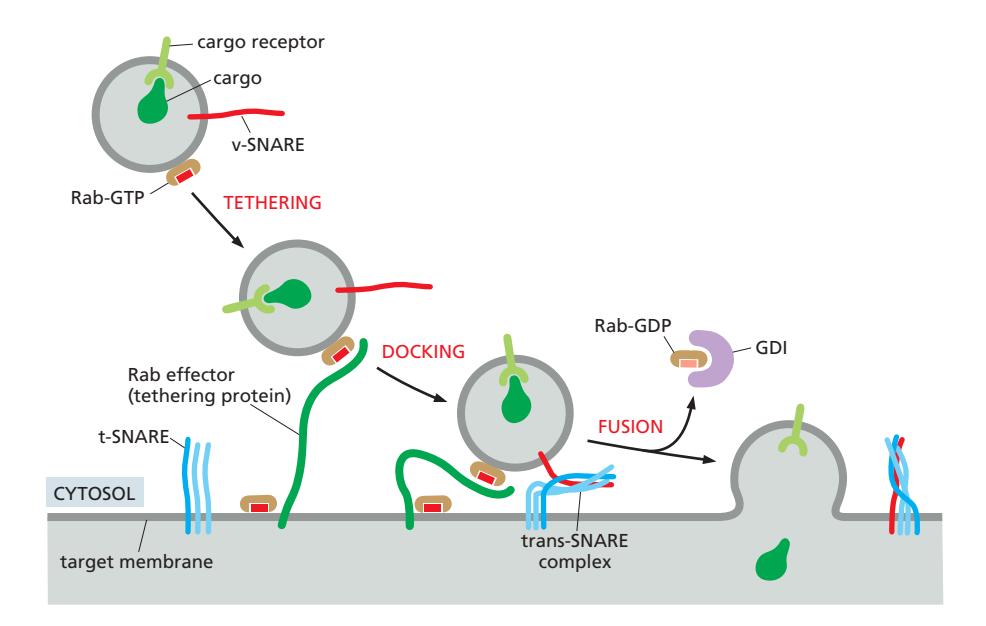
Vesicle Tethering과 Docking

Long-range tethering:
- Rab effector (filamentous protein)가 target membrane에서 vesicle을 먼 거리(200 nm)에서 포착
- Vesicle의 Rab-GTP와 target membrane의 Rab effector가 상호작용
- 이때 vesicle의 Rab과 target membrane의 Rab은 같은 종류여야 함
SNARE-mediated docking:
- Rab effector가 SNARE를 선택적으로 결합
- v-SNARE와 t-SNARE pairing 촉진 → membrane fusion 유도
Rab inactivation:
- Fusion 후 Rab GAP가 Rab-GTP를 가수분해 → Rab-GDP
- GDI가 Rab-GDP를 membrane에서 추출 → cytosol로 복귀
Rab5→Rab7 Cascade
- Rab5-associated membrane patch가 시간이 지나면서 Rab7-associated patch로 교체
- 이 전환이 일방향적이고 비가역적: early endosome → late endosome 성숙
- Rab5→Rab7 전환 실패 시 cargo가 lysosome에 도달 불가
10. SNARE Proteins: Membrane Fusion
SNARE protein은 vesicle과 target membrane의 융합을 직접 촉매한다.
분류
- v-SNARE (vesicle-SNARE): transport vesicle membrane에 위치. Single polypeptide
- 대표 예: Synaptobrevin
- t-SNARE (target-SNARE): target membrane에 위치. 보통 3개 protein으로 구성
- 대표 예: Syntaxin (1 helix) + SNAP25 (2 helices)
Fusion 5단계
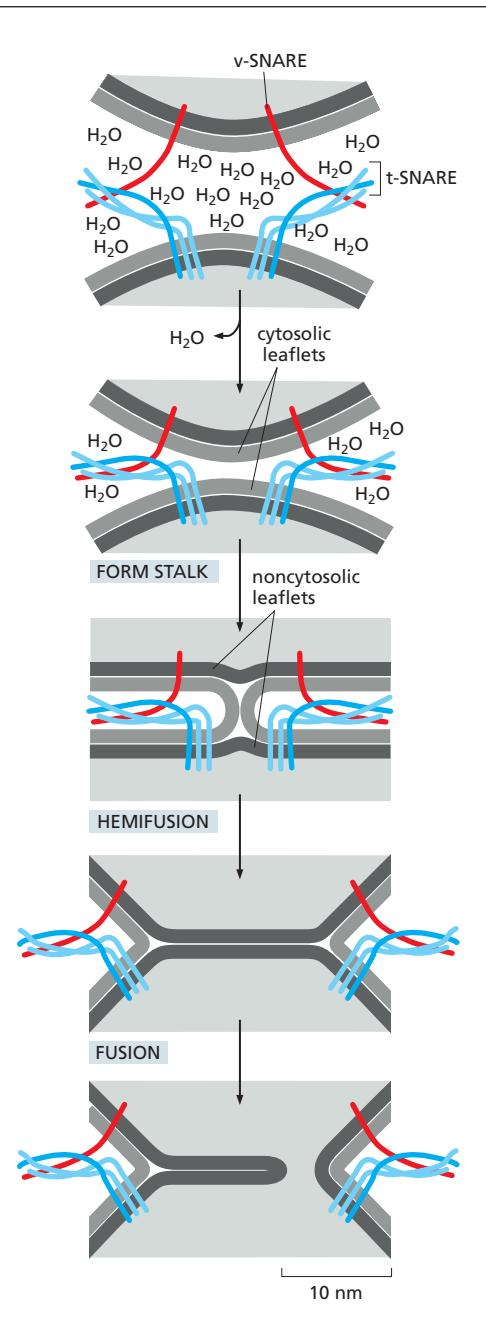
- Membrane Apposition: 두 membrane이 tight하게 lock
- Expels water molecules
- SNARE pairing의 stability가 energy 제공
- Stalk Formation:
- Hemifusion:
- New bilayer 형성 (hemifusion 또는 half-fusion)
- New bilayer rupture:
- Complete fusion reaction
SNARE-mediated fusion의 에너지는 궁극적으로 NSF의 ATP hydrolysis에서 유래. NSF가 SNARE를 분리하는 데 ATP 소비 → 분리된 SNARE가 다시 assembly하며 fusion을 drive하는 cycle.
Homotypic vs Heterotypic Fusion
- Heterotypic fusion (대부분의 경우): 서로 다른 compartment의 membrane이 융합. v-SNARE + t-SNARE pairing
- Homotypic fusion: 같은 종류의 membrane끼리 융합. 양쪽 membrane에 v-SNARE와 t-SNARE 모두 존재
- 예: ER-derived vesicle끼리 융합하여 VTC 형성, endosome끼리 융합
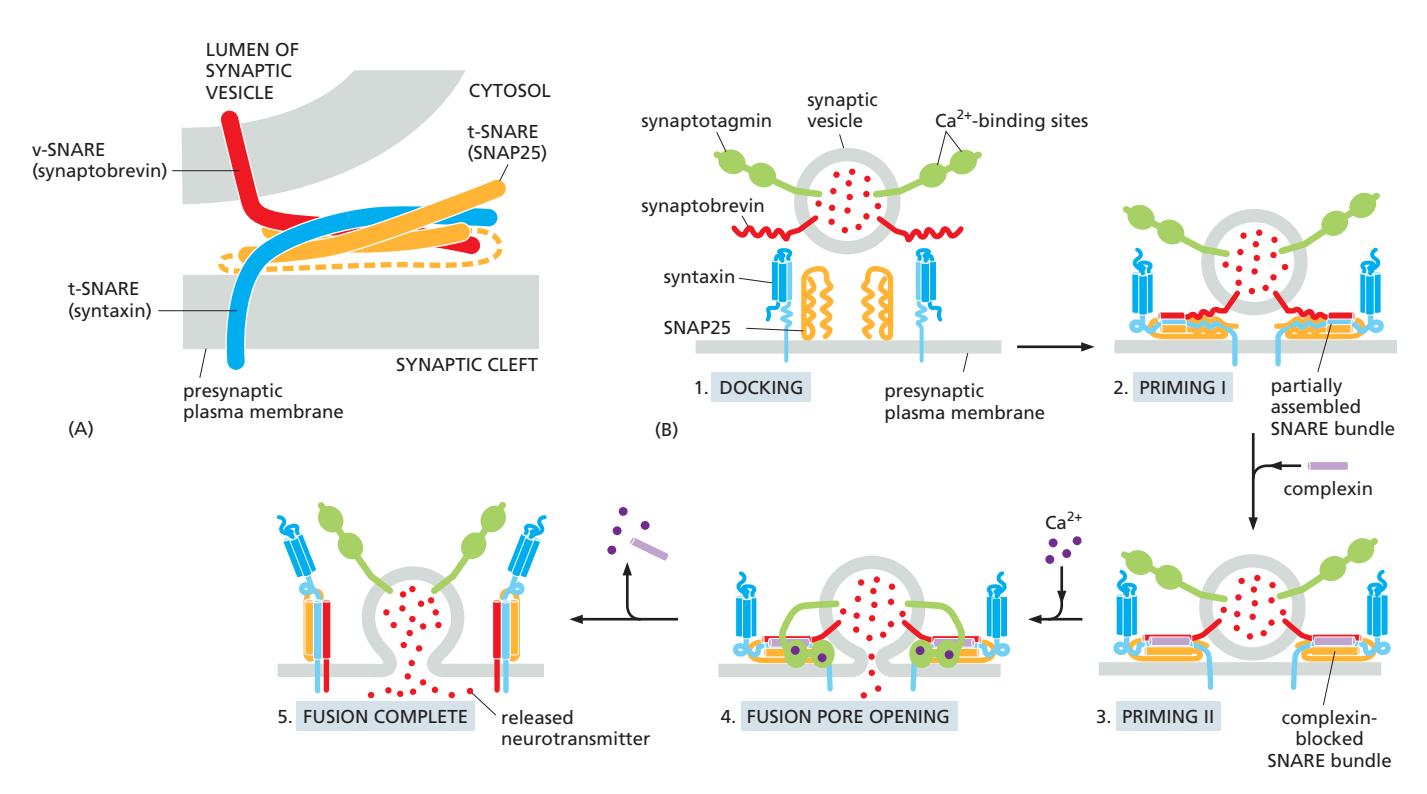
Synaptic Vesicle의 특수한 SNARE
Component:
- v-SNARE: Synaptobrevin (transmembrane)
- t-SNARE: Syntaxin (transmembrane, 1 helix) + SNAP25 (peripheral, 2 helices)
조절 메커니즘 (Complexin + Synaptotagmin):
- SNARE partially assemble → primed state
- Complexin이 premature fusion 방지 (metastable state로 freeze)
- Ca²⁺ influx → Synaptotagmin (Ca²⁺ sensor) 활성화
- Complexin release
- SNARE fully zipper → rapid fusion
- Neurotransmitter release (millisecond scale)
11. ER-to-Golgi Transport
ER에서 Golgi로의 수송은 COPII vesicle을 통해 이루어진다.
12. Vesicular Tubular Cluster (VTC)
VTC는 ER에서 Golgi로 이동하는 중간 수송 구획이다.
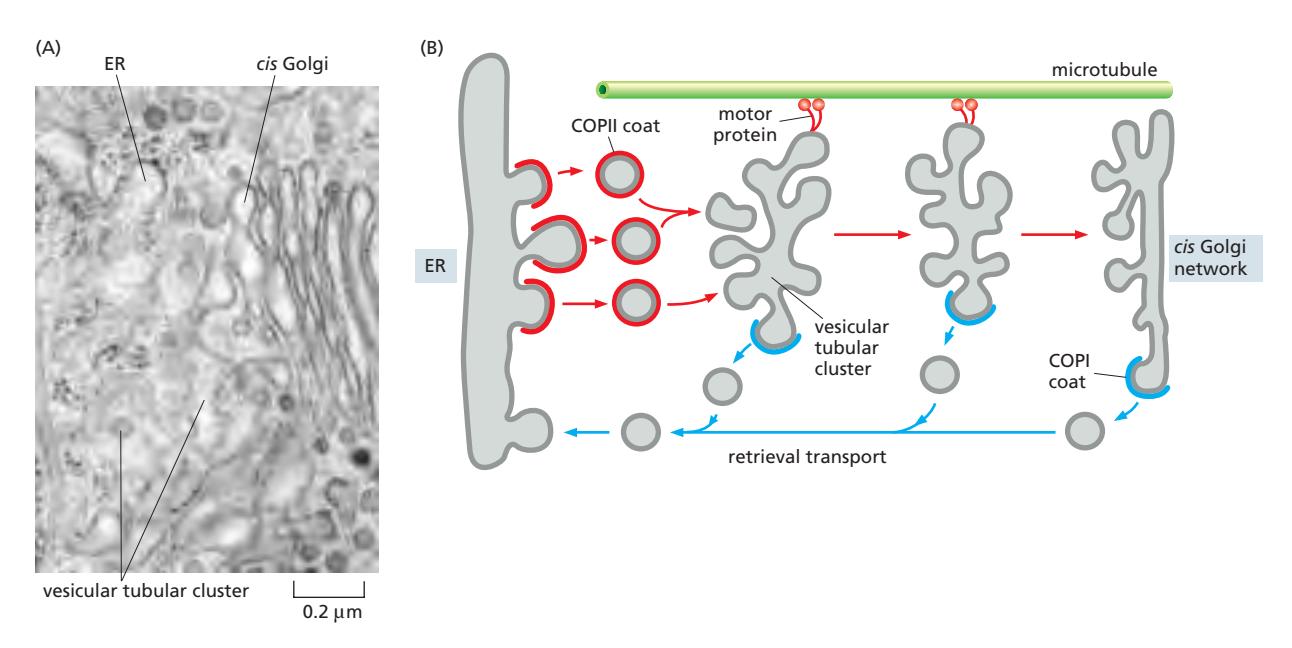
형성
- COPII-coated vesicle이 coat를 shed한 후 homotypic fusion (SNARE mediated)
- Convoluted 모양의 vesicular tubular cluster 형성
- 지속적으로 새로 생성되어 ER → Golgi로 material 운반
Golgi로의 이동
- Microtubule을 따라 motor protein에 의해 Golgi로 이동
- VTC가 Golgi와 fusion하여 cargo 전달
13. Retrieval Pathway: ER Resident Protein 회수
Retrieval pathway는 실수로 ER을 떠난 단백질을 되돌리는 경로이다.

COPI-coated Vesicle
- VTC에서 즉시 COPI-coated vesicle budding 시작
- COPI coat의 특징: inner + outer coat가 coatomer라는 preassembled complex로 한 번에 recruit
ER Retrieval Signal
막 단백질 신호: KKXX
- C-terminal에 two lysine + any two amino acid: KKXX sequence
- COPI coat에 직접 결합 → COPI vesicle로 ER 귀환
- ER-Golgi interface에서 기능하는 SNARE, cargo receptor에서 발견
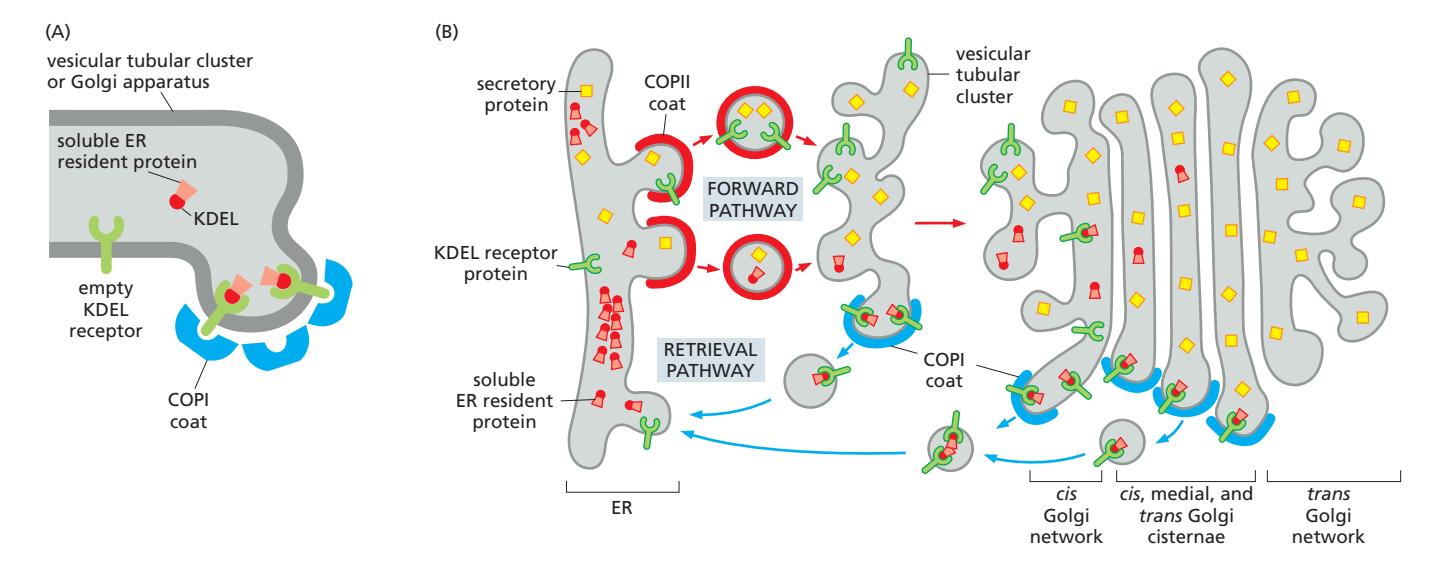
가용성 단백질 신호: KDEL

- C-terminal의 KDEL sequence (Lys-Asp-Glu-Leu)
- BiP 등 soluble ER resident protein이 보유
- KDEL receptor (multipass transmembrane protein)가 인식 → COPI vesicle로 packaging
KDEL receptor cycling:
- Golgi (pH ~6.5–6.7): KDEL sequence에 강하게 결합 → COPI vesicle로 ER 귀환
- ER (pH ~7.2): 약한 결합 → KDEL-bearing protein 방출
- Critical histidine: Golgi의 낮은 pH에서 protonated → KDEL과의 interaction 강화
- KDEL receptor가 ER↔Golgi 사이를 shuttle하며 escaped protein 회수
14. Golgi Apparatus
Golgi apparatus는 secretory pathway의 중심 processing 기관이다.
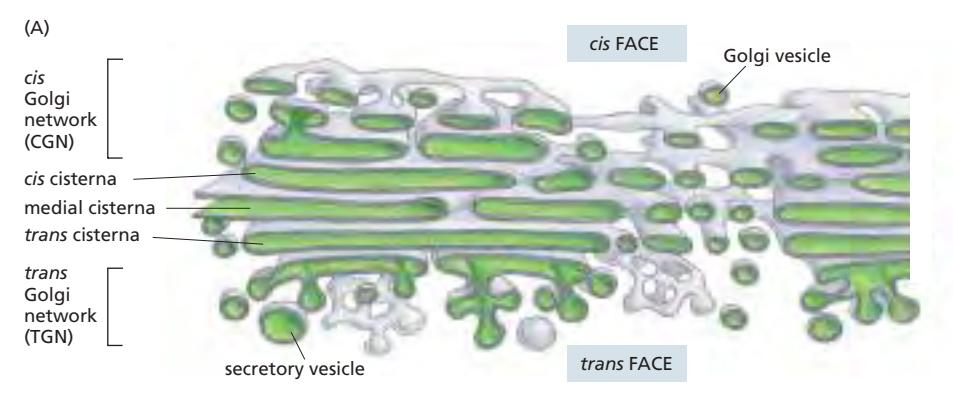
Cis/Medial/Trans 구획
| 구획 | 위치 | 주요 기능 |
|---|---|---|
| Cis Golgi | ER에 가장 가까운 면 | M6P tagging, 초기 processing |
| Medial cisternae | 중간 | 중간 단계 glycosylation |
| Trans Golgi | ER에서 먼 면 | 최종 glycosylation 완성 |
| TGN | Trans cisterna와 연속 | 단백질 sorting 및 발송 |
- 초기 작용 효소: 주로 cis cisternae
- 나중 작용 효소: 주로 trans cisternae
- 효소 분포는 stack 전체에 graded 방식으로 분포
N-linked Oligosaccharide Processing
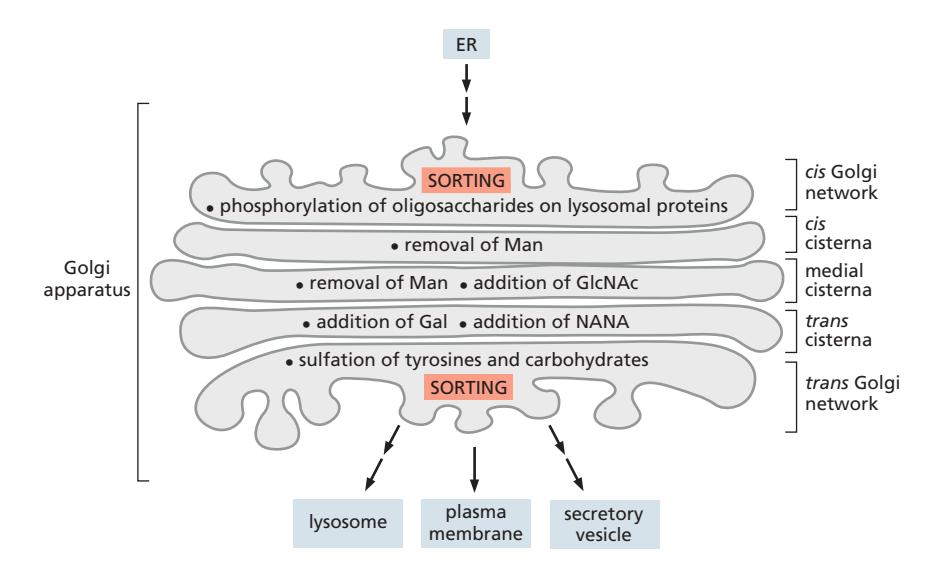
| 구획 | 가공 |
|---|---|
| Cis + Medial | Mannose 제거, N-acetylglucosamine 추가 |
| Trans + TGN | Galactose 추가, Sialic acid 추가 |
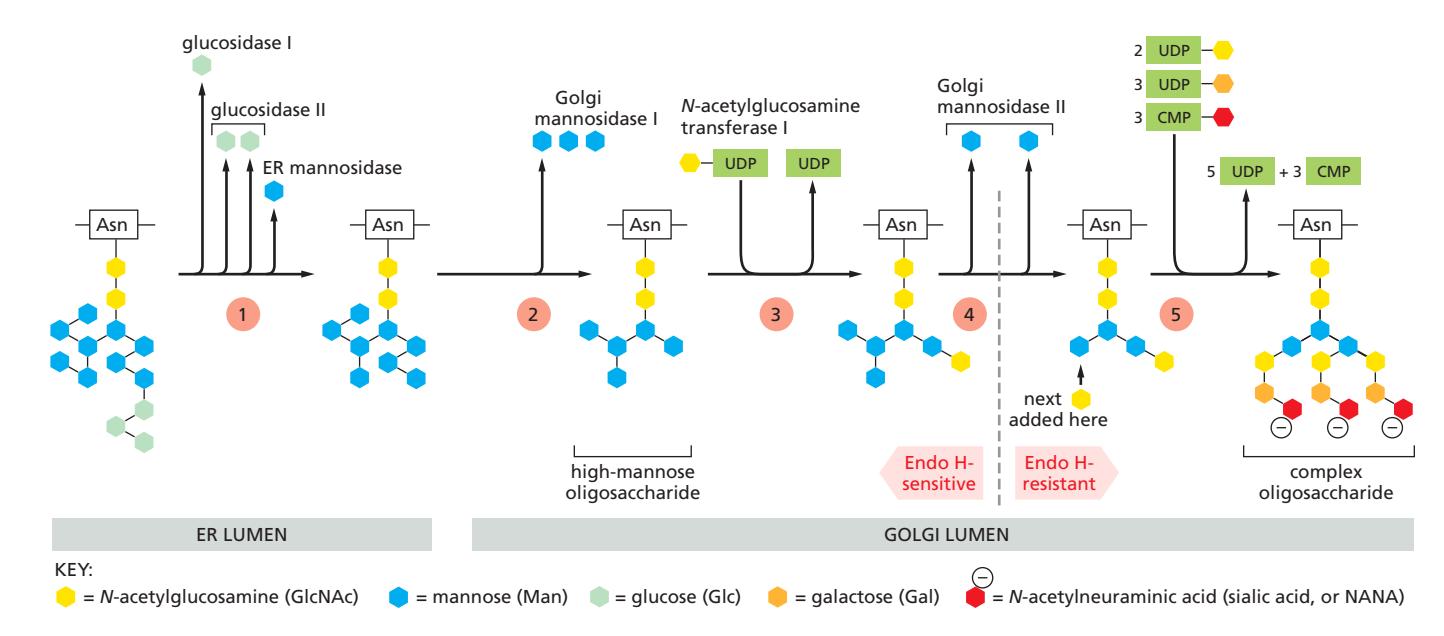
- 모든 Golgi glycosidase/glycosyl transferase: single-pass transmembrane protein
- 기질: 활성화된 sugar nucleotide (UDP-GlcNAc, UDP-Gal, CMP-NANA)
Cisternal Maturation Model vs. Vesicle Transport Model
| 모델 | 특징 |
|---|---|
| Vesicle transport model | Cisternae는 고정. Cargo가 vesicle로 앞 방향 이동 |
| Cisternal maturation model | Cisternae 자체가 cis→trans로 이동하며 성숙. Golgi enzyme은 COPI vesicle로 역행 이동하여 위치 유지 |
Cisternal maturation model이 지지되는 이유:
- Procollagen처럼 vesicle에 포장하기 너무 큰 cargo의 이동이 관찰됨
- COPI vesicle은 Golgi enzyme의 역행 수송 담당 (cargo는 남고 enzyme이 이동)
- organelle identity가 순차적으로 변화
요약 흐름도
ER exit site
↓ (COPII vesicle)
Vesicular Tubular Cluster (VTC)
↓ (microtubule transport)
Cis Golgi → Medial → Trans → TGN
↑
COPI retrograde vesicle (Golgi enzyme 역행, ER retrieval)
↑
KKXX / KDEL signal로 회수
관련 내용 노트
- Vesicle transportation 개요
- Clathrin coat 구조와 기능
- AP2 어댑터 단백질
- PIP — organelle identity marker
- Dynamin에 의한 vesicle fission
- ARF GTPase — coat assembly 조절
- Rab GTPase cycle
- Rab cascade — Rab5→Rab7
- SNARE protein — membrane fusion
- SNARE에 의한 vesicle fusion 메커니즘
- ER-Golgi transport
- VTC
- ER retrieval pathway
- Golgi 기능적 구획화