세포생물학 10과 — Membrane Structure 정리본 (2주차)
슬라이드 기반 핵심 정리 | 관련 노트: 000_Ch10_Membrane Structure_정리본 · 001_Chapter10_MOC
1. Membrane Structure 개요 (슬라이드 2)
Major lipids in cell membrane · Lipid bilayer 참조
세포막은 phospholipid bilayer를 기본 골격으로 한다.
주요 구성 성분
| 성분 | 역할 |
|---|---|
| Phospholipid | bilayer의 기본 골격 형성 (cylinder-shaped → bilayer 자발 형성) |
| Cholesterol | 막 유동성 완충 조절 (고온: 유동성 ↓ / 저온: 결정화 방지) |
| Glycolipid | noncytosolic leaflet에만 분포; 세포 인식·신호 수용체 역할 |
| Membrane protein | 막 기능 담당; 전체 genome 단백질의 약 30% |
| Phospholipid중 |
<span class="text-highlight">[[Phospholipid#phosphoglyceride|phosphoglyceride]]는 다른 지질보다 유동적.</span>
<span class="text-highlight">그 중 phosphatidylserine(PS)는 음전하</span>
<span class="text-highlight">sphingolipid는 콜레스테롤과 결합력이 좋아 lipid raft 생성 관여.</span>
Protein : Lipid 질량비 ≈ 1 : 1 → protein 1개당 약 50개의 lipid molecule
Phospholipid의 구조
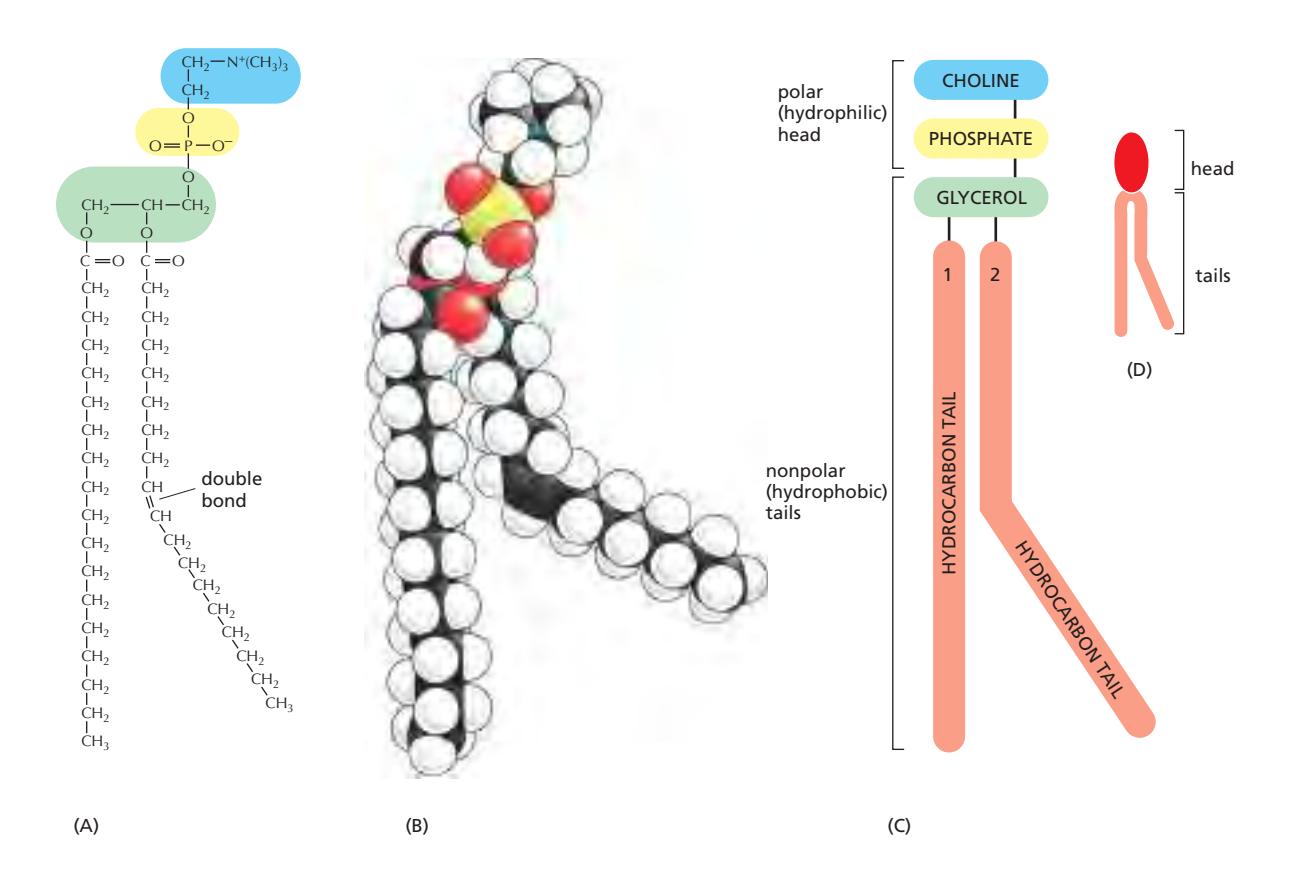
- Hydrophilic head: phosphate + head group (charged/polar) → 물과 전정기적 상호작용 및 수소결합
- Hydrophobic tail: 2개의 fatty acid hydrocarbon chain → 물과 favorable interaction 불가
Phospholipid 중 phosphoglyceride
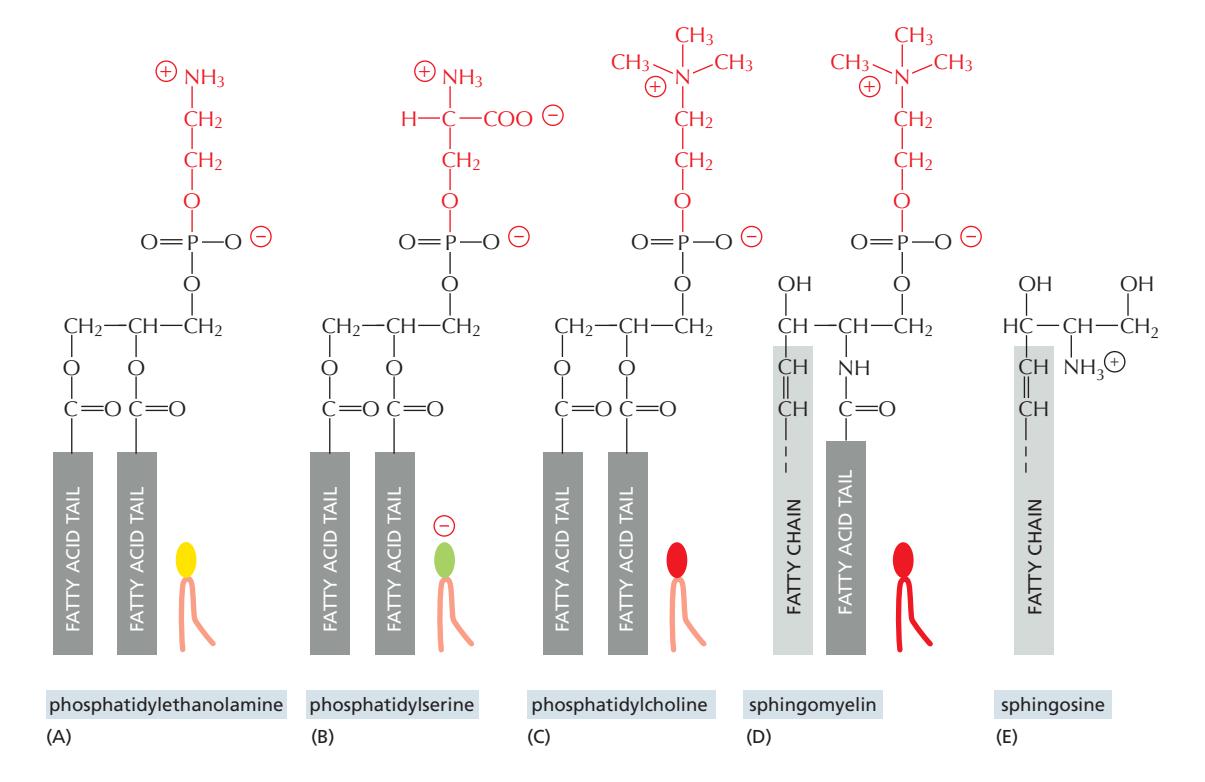 이 중 PE, PS, PC.
sphingolipid 보다 유동적이다.
PS만 음전하.
이 중 PE, PS, PC.
sphingolipid 보다 유동적이다.
PS만 음전하.
Phospholipid 중 spingolipid
위에서 D. 한쪽 chain이 fatty chain인 sphingosine을 전구체로 삼음 sphingosine은 이후 Glycolipid의 전구체이기도 함. sphingolipid는 cholesterol과 결합력이 좋아 lipid raft 형성에 관여함.
cholesterol
Glycolipid
Glycolipid는 sugar를 포함하는 lipid molecule이다. 모든 진핵세포 plasma membrane의 표면에서 발견되며, membrane 분포에서 가장 극단적인 asymmetry를 보인다.
주요 수업 내용
phospholipid만큼 비율이 높지는 않다. spingosine 기반
- galactocerebrocide
- ganglioside(slalic acid가 붙어 음전하)
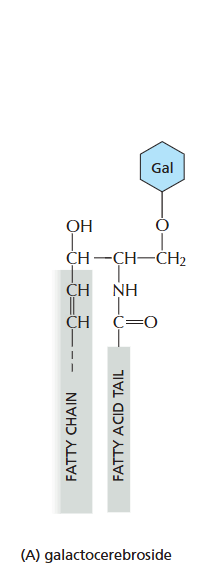
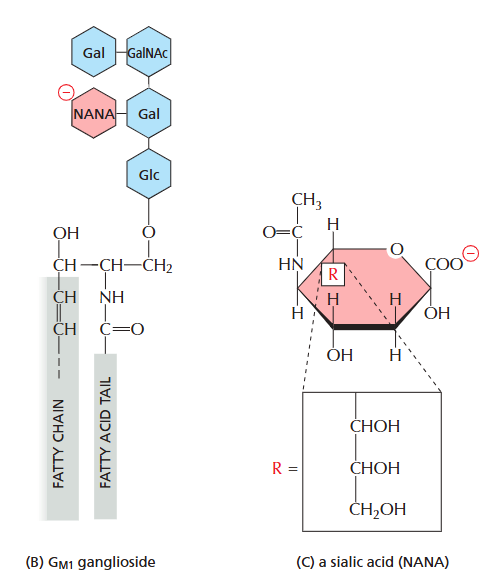
2. Amphiphilic Molecules (슬라이드 5)
Amphiphilic molecule · Micelle 참조
수용액에서의 자발적 배열 — Hydrophobic Effect
물속에서 hydrophobic tail이 노출되면 인접 water molecule이 icelike cage 구조로 재배열 → entropic free energy 증가 → 자발적 clustering
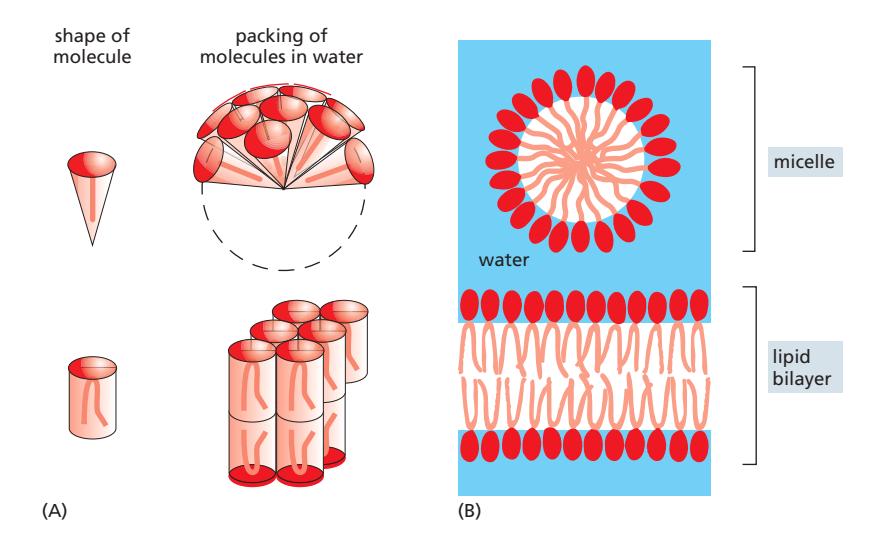
| 분자 모양 | 형성 구조 | 예시 |
|---|---|---|
| Cone-shaped (head > tail) | Micelle | Detergent |
| Cylinder-shaped (head ≈ tail) | Lipid bilayer | Phospholipid |
Self-sealing 특성
Bilayer에 tear 발생 → free edge에서 hydrophobic tail 노출 (energetically unfavorable) → 자발적으로 닫혀 sealed compartment 형성 → 생명의 compartmentalization 기반
3. Lipid Bilayer Properties (슬라이드 3)
Fluidity of a lipid bilayer · Asymmetry of the lipid bilayer 참조
3.1 유동성 (Fluidity)
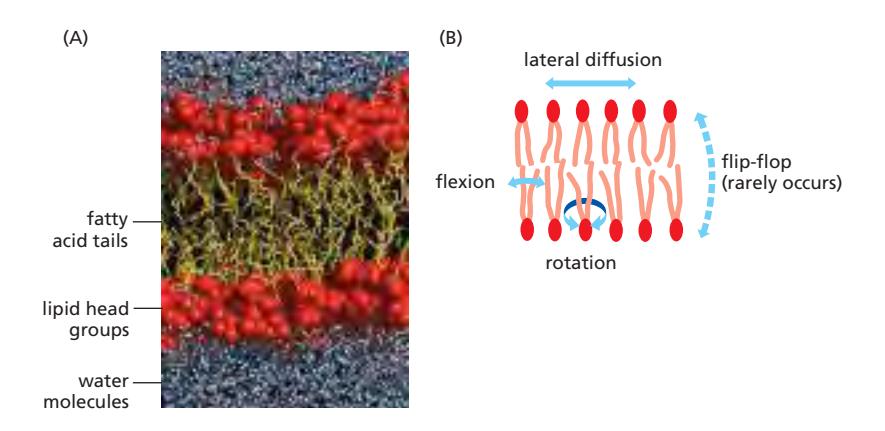 지질 분자의 4가지 운동:
지질 분자의 4가지 운동:
- Lateral diffusion — 같은 monolayer 내에서 빠른 위치 교환 (~10⁷/sec)
- Rotational diffusion — 긴 축 중심 회전
- Flexion — 꼬리 부분의 유연한 굽힘
- Flip-flop — 반대편 monolayer로 이동 (수 시간 단위; hydrophilic head가 hydrophobic core 통과 필요 → 매우 드묾)
Phase transition 온도를 낮추는 조건 (유동성 증가)
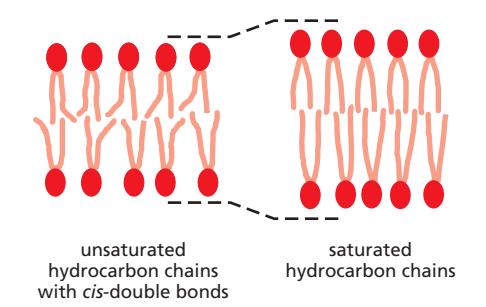
- Hydrocarbon chain이 짧을 때 (van der Waals 상호작용 감소)
- Chain에 cis-double bond 존재 시 → kink 형성 → chain packing 방해
Cholesterol의 역할 (유동성 완충)
| 조건 | 효과 |
|---|---|
| 고온 | Hydrocarbon chain 이동성 억제 → mobility ↓, permeability ↓ |
| 저온 | 결정화(crystallization) 방지 → fluid 상태 유지 |
→ Cholesterol은 체온 완충제: 막이 너무 딱딱해지거나 너무 유동적이 되는 것 모두 방지
온도 적응 (단세포 생물)
온도 하락 시 → cis-double bond를 더 많이 가진 fatty acid 합성 → 유동성 저하 방지
지질 조성 성분 특성
| Percentage of total lipid by weight | ||||||
|---|---|---|---|---|---|---|
| Lipid | Liver cell plasma membrane | Red blood cell plasma membrane | Myelin | Mitochondrion (inner and outer membranes) | Endoplasmic reticulum | Escherichia coli bacterium |
| Cholesterol | 17 | 23 | 22 | 3 | 6 | 0 |
| Phosphatidylethanolamine | 7 | 18 | 15 | 28 | 17 | 70 |
| Phosphatidylserine | 4 | 7 | 9 | 2 | 5 | Trace |
| Phosphatidylcholine | 24 | 17 | 10 | 44 | 40 | 0 |
| Sphingomyelin | 19 | 18 | 8 | 0 | 5 | 0 |
| Glycolipids | 7 | 3 | 28 | Trace | Trace | 0 |
| Others | 22 | 14 | 8 | 23 | 27 | 30 |
| 이렇게 나와있지만 실제로 E.coli의 세포막 외측에는 others에 속하는 다른 음전하 인지질이 있음. |
막단백질 이동성 실험적 증명
- Frye-Edidin Experiment (1970): 마우스(초록 형광) + 인간(빨강 형광) 세포 융합 → 37°C, 40분 후 완전 혼합 → 막단백질의 lateral diffusion 확인
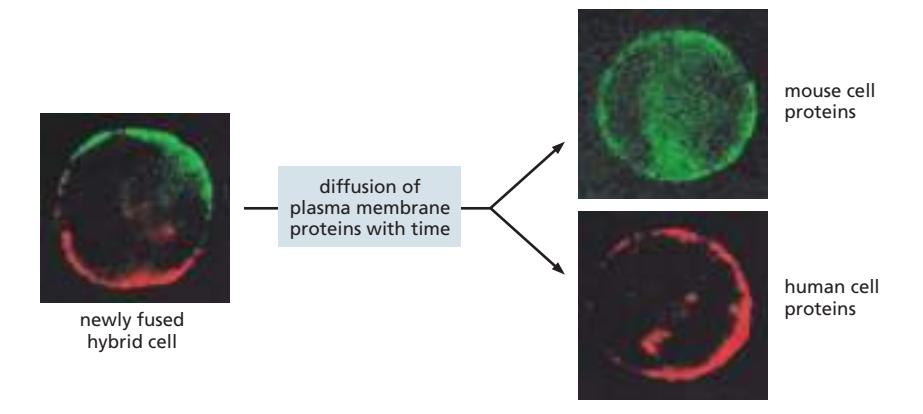
- FRAP (Fluorescence Recovery After Photobleaching): lateral diffusion rate 정량 측정
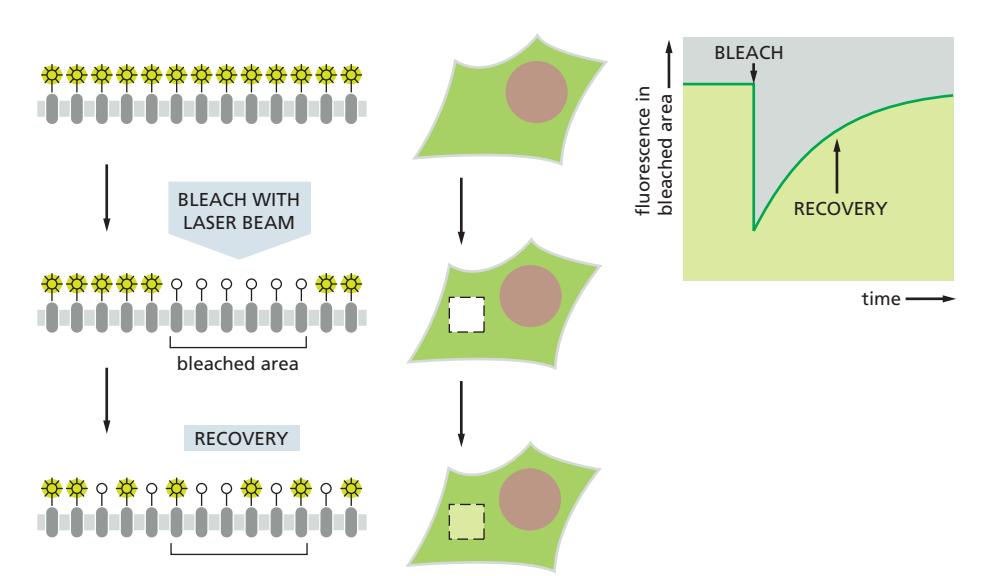
3.2 비대칭성 (Asymmetry)
Human RBC의 lipid 비대칭 분포:
| Leaflet | 주요 지질 |
|---|---|
| Noncytosolic (outer) | PC (Phosphatidylcholine), SM (Sphingomyelin), Glycolipid |
| Cytosolic (inner) | PE (Phosphatidylethanolamine), PS (Phosphatidylserine) |
- PS: 유일하게 net negative charge → cytosolic leaflet 집중
- Glycolipid: noncytosolic monolayer에만 독점 분포 (가장 극단적 asymmetry)
- Golgi lumen에서 sugar group 추가 → 세포 외부와 topologically equivalent → plasma membrane 전달 시 cell surface 노출
Flippase & Scramblase
- Flippase (ATP 필요): PS, PE를 outer → inner leaflet으로 능동 수송 → asymmetry 유지
- Scramblase: 양방향 무작위 flip-flop → asymmetry 파괴
Apoptosis와 PS 노출
- Flippase 비활성화
- PS → outer (extracellular) monolayer로 translocation
- Cell surface에 PS 노출 → eat-me signal
- Macrophage가 인식 → phagocytosis (정상 apoptosis)
4. Raft Domain
Raft domain 참조
4.1 Lipid Raft 형성 원리
 Artificial bilayer 실험:
Artificial bilayer 실험:
- PC + SM (1:1) → 균일한 bilayer
- PC + SM + Cholesterol (1:1:1) → 두 개의 phase 분리 → Cholesterol이 sphingolipid-rich ordered phase 안정화
- 살아있는 세포에서는 일시적이고 동적인 방식으로 형성/해체
4.2 Lipid Raft 구성 성분
- Cholesterol 농축
- Sphingolipid 농축
- Glycolipid 농축
- GPI-anchored protein 농축
- 일부 transmembrane protein
Sphingolipid가 raft에 집중되는 이유:
- 포화 탄화수소 사슬 → 직선형 구조 → 밀착 packing 가능
- Cholesterol과 소수성 결합이 좋음
- van der Waals 상호작용으로 raft 형성 유리
4.3 Lipid Raft의 특성
| 특성 | 내용 |
|---|---|
| 일시적 (Transient) | 필요에 따라 형성/해체 |
| 동적 (Dynamic) | Protein-protein interaction으로 조절 |
| 작은 규모 (Nanoscale) | 수 nm ~ 수백 nm |
| 기능 특화 | 특정 cellular process 조직화 |
4.4 기능
- 신호전달 (Cell Signaling): signaling protein 집중 → extracellular signal의 intracellular signal 변환 효율화
- Membrane Traffic: vesicle에서 protein 조직화 및 transport 촉진
- Cell Adhesion: GPI-anchored protein localization 조절
5. Membrane Protein
Membrane protein · α-helical Conformation in Membrane Proteins · β-Barrels Forming Large Channels 참조
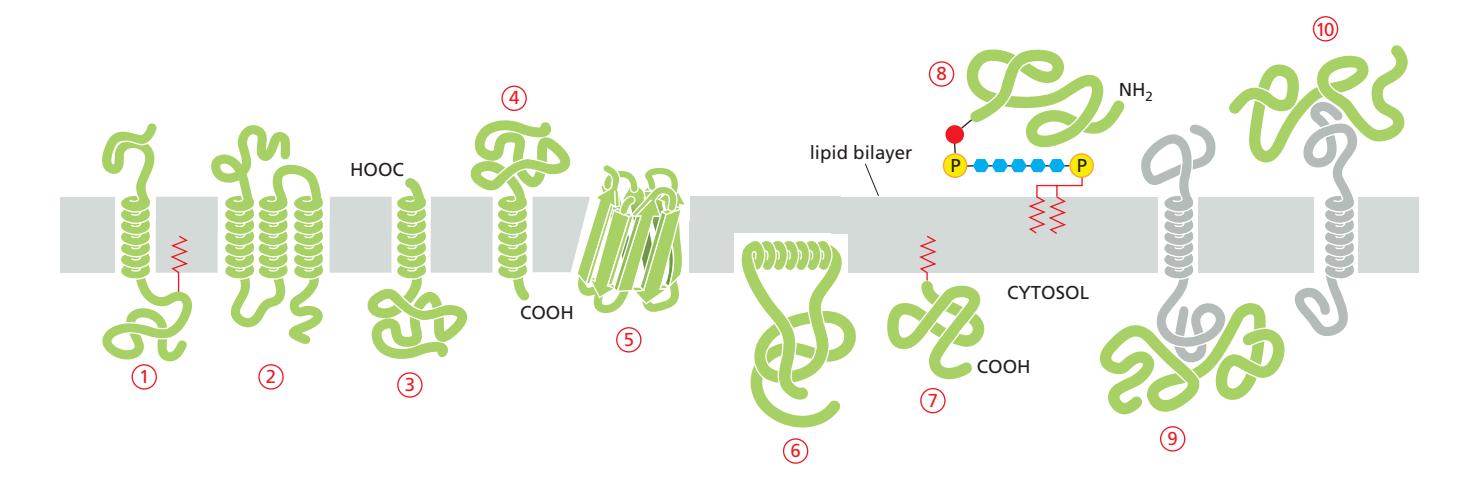 Fig 7. Membrane protein이 lipid bilayer와 결합하는 다양한 방식 (1~10)
Fig 7. Membrane protein이 lipid bilayer와 결합하는 다양한 방식 (1~10)
결합 방식
| 유형 | 설명 | 예시 번호 |
|---|---|---|
| Single-pass transmembrane | 단일 α-helix로 bilayer 횡단 | 1 |
| Multipass transmembrane | 다중 α-helix로 bilayer 횡단 | 2 |
| β-barrel transmembrane | Rolled-up β sheet로 bilayer 횡단 | 5 |
| Lipid-anchored (cytosolic) | Amphiphilic α-helix 또는 fatty acid/prenyl chain으로 고정 | 6, 7 |
| GPI-anchored (noncytosolic) | Oligosaccharide linker를 통해 phosphatidylinositol에 부착 | 8 |
| Membrane-associated | 다른 membrane protein과 noncovalent interaction으로 결합 | 9, 10 |
Transmembrane α-Helix 구조
- 약 20-30개의 소수성 아미노산으로 구성
- Peptide bond 자체는 극성이지만 연속적 소수성 배치로 lipid 환경에 삽입 가능
- **Hydropathy plot**에서 positive값(+)으로 확인 가능
- Pore 형성 시 amphiphilic helix: 한쪽 면은 친수성 (pore 안쪽), 반대쪽은 소수성 (lipid 접촉)
- 이때 모든 아미노산이 소수성일 필요 없음 → hydropathy plot으로 TM 개수 측정 불가
- 여러 helix가 인접할 때도 맞닿는 면은 소수성일 필요 없음
- 3
4개를 주기로 친수성, 소수성이 교대로 나타나면, 헬릭스가 계속 돌아가더라도 특정 각도 범위(예: 0°180°)에는 친수성 아미노산만, 나머지 각도(180°~360°)에는 소수성 아미노산만 모일 수 있음.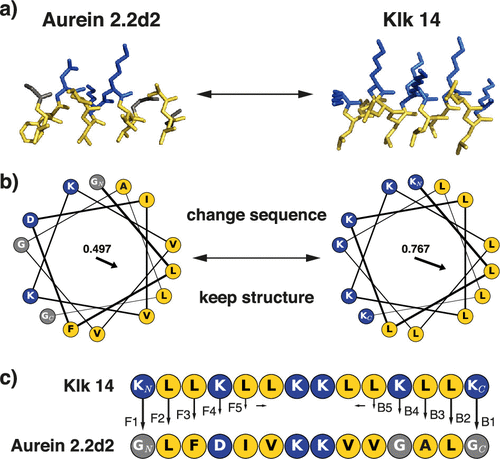
- 친소소친소소친친소소 이런식
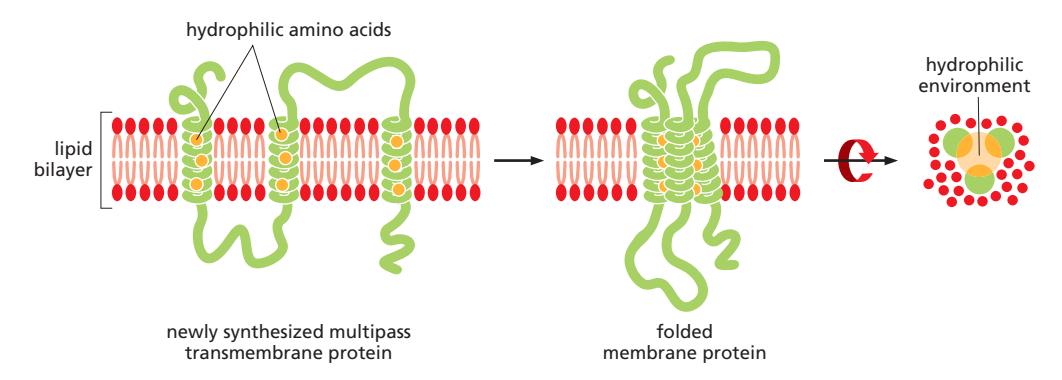 Fig 8. 여러 TM α-helix가 모여 기능하는 예: domain/protein이 유동적으로 움직이다가 신호를 받아 결합
Fig 8. 여러 TM α-helix가 모여 기능하는 예: domain/protein이 유동적으로 움직이다가 신호를 받아 결합
Transmembrane β-Barrel 구조
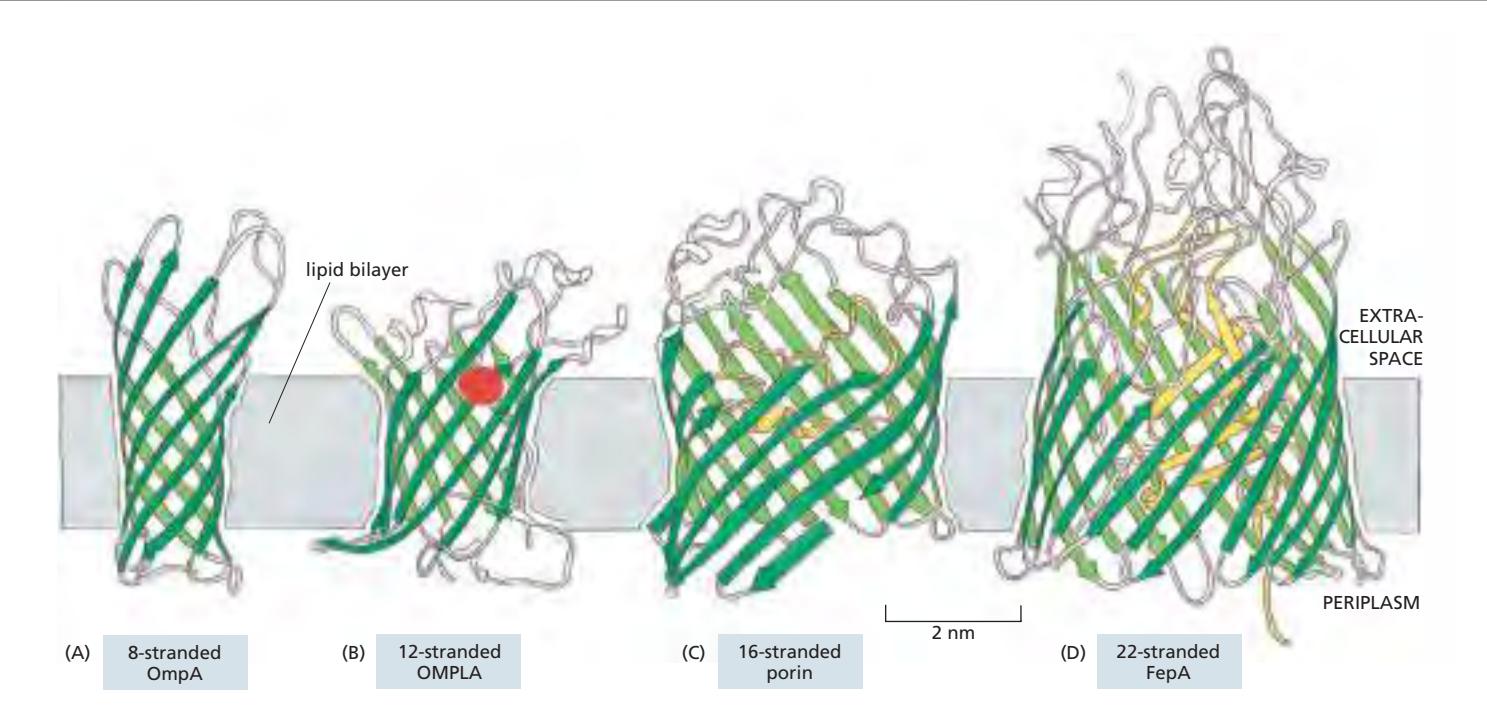 Fig 9. β-barrel transmembrane protein (porin 등) - 주로 박테리아, 미토콘드리아에 존재
Fig 9. β-barrel transmembrane protein (porin 등) - 주로 박테리아, 미토콘드리아에 존재
- Multiple β-strand가 rolled-up β sheet (β barrel) 형성
- 막 횡단에 10개 이하의 아미노산으로 충분 (extended β strand)
- 격번 아미노산의 side chain만 소수성이면 됨
- Porin 등에서 발견 (주로 박테리아, 미토콘드리아)
Lipid anchor
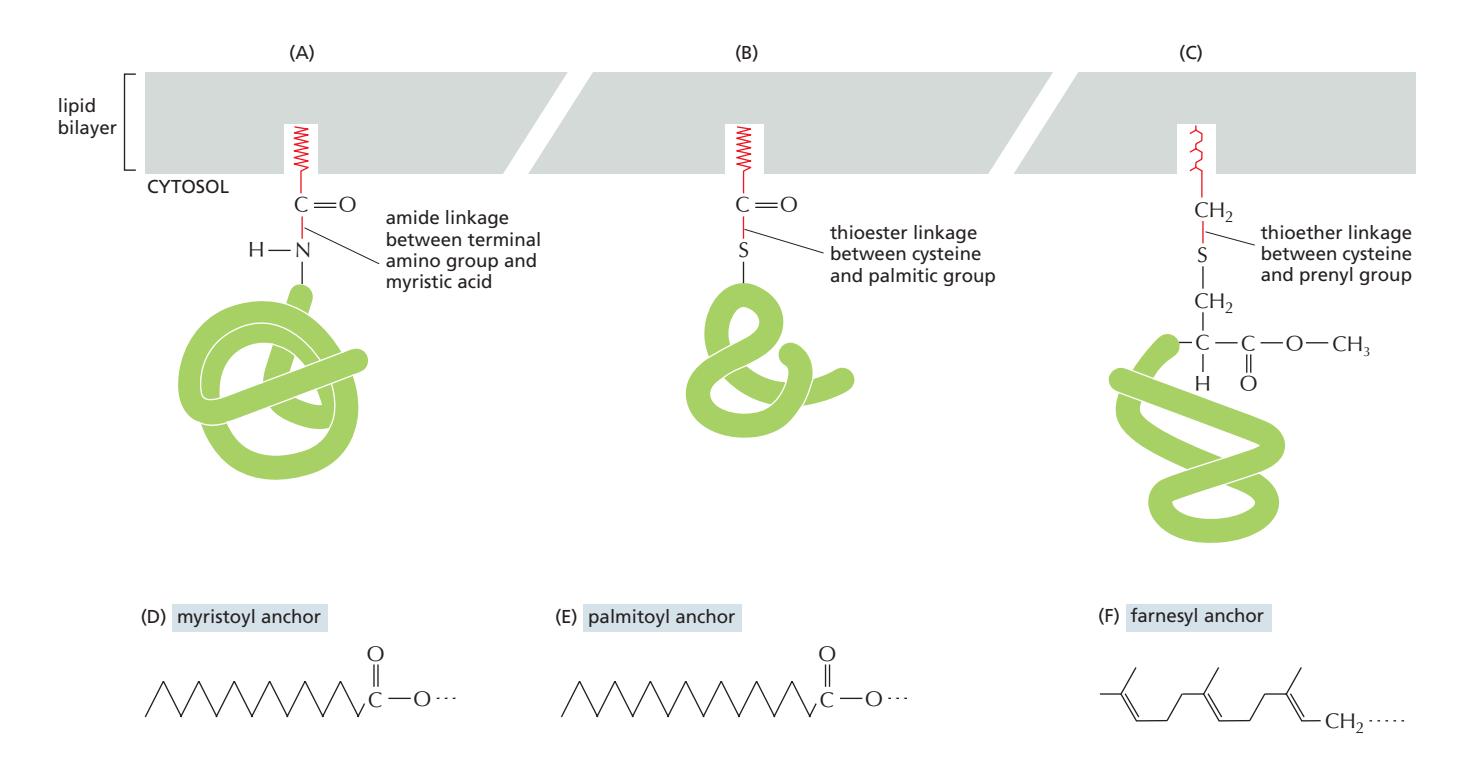 단백질이 palmitoylation, 혹은 farnesylation되어야 cytosolic protein이 membrante protein이 되면서 기능하기 시작함.
단백질이 palmitoylation, 혹은 farnesylation되어야 cytosolic protein이 membrante protein이 되면서 기능하기 시작함.
Glycosylation
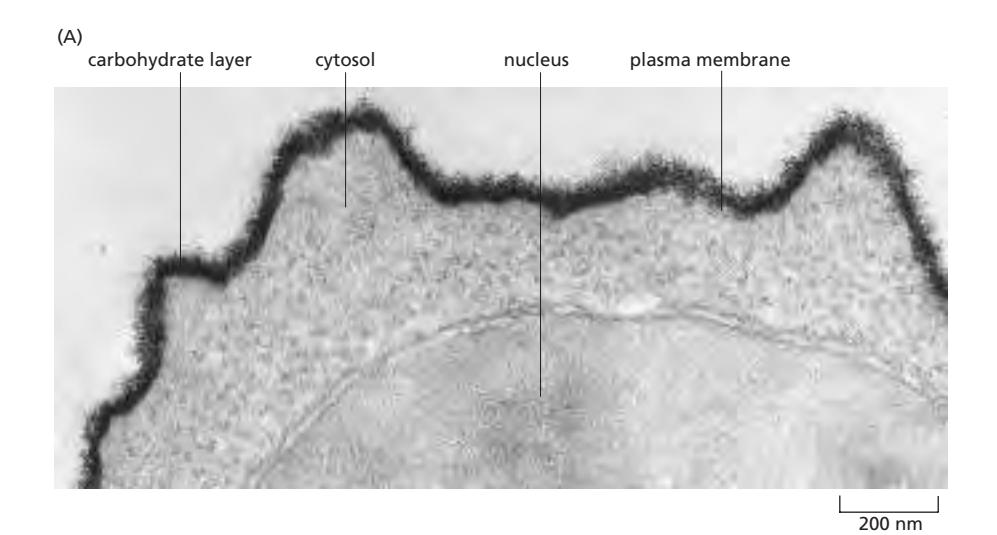 Fig 10. Carbohydrate layer (glycocalyx): glycolipid와 glycoprotein의 oligosaccharide가 cell surface를 덮음
Fig 10. Carbohydrate layer (glycocalyx): glycolipid와 glycoprotein의 oligosaccharide가 cell surface를 덮음
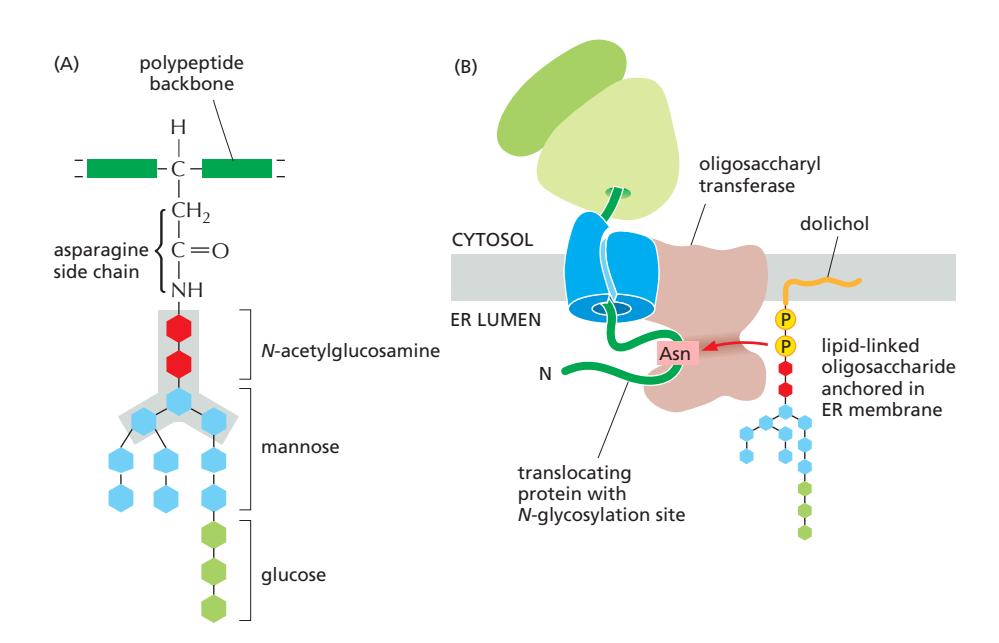
- Sugar residue가 ER과 Golgi lumen에서 추가 (oligosaccharyl transferase에 의해 asparagine으로)
- Oligosaccharide chain이 항상 membrane의 noncytosolic side에 존재
- Disulfide bond도 noncytosolic surface에만 위치
- Cytosol은 reducing environment → cytosolic domain의 sulfhydryl group은 disulfide bond 형성 안 함
이동성 제한
- Membrane protein은 lateral diffusion과 rotational diffusion이 가능하지만,
- 세포는 특정 membrane protein을 고정시키거나 특정 domain에 국한시키는 방법을 보유
- Restricting domain of membrane protein 참조 (cortical cytoskeleton 등)
단백질 고정법 4가지
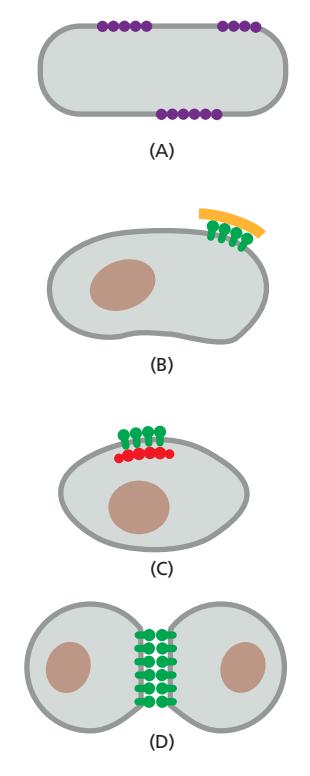
- (A) 막단백질끼리 고정
- (B) extracellular 거대 분자 assembly를 이용해 고정
- (C) 내부의 cytoskeleton같은 거대 분자 assembly에 의한 고정
- (D) 다른 세포 표면의 단백질과 상호작용
막단백질의 자유 확산만 제한하는 정도
Cortical cytoskeleton
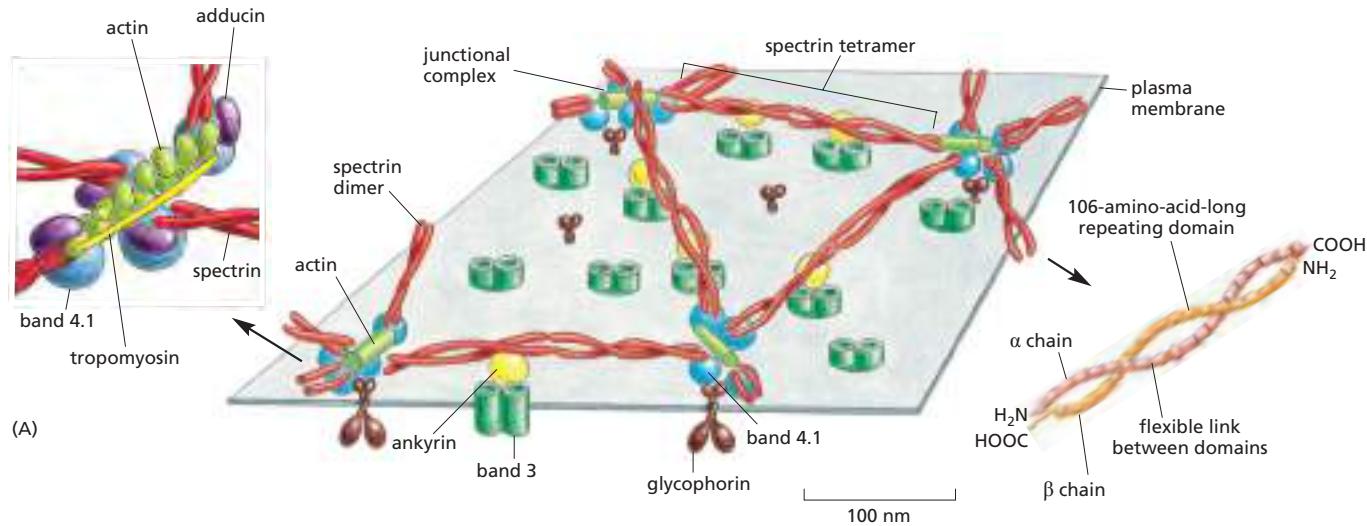 인간 red blood cell(RBC)는 세포막 바로 아래의 cortical cytoskeleton의 spectrin의 탄성으로 모세혈관을 드나들 때 접힘에도 형태를 복구할 수 있음.
인간 red blood cell(RBC)는 세포막 바로 아래의 cortical cytoskeleton의 spectrin의 탄성으로 모세혈관을 드나들 때 접힘에도 형태를 복구할 수 있음.
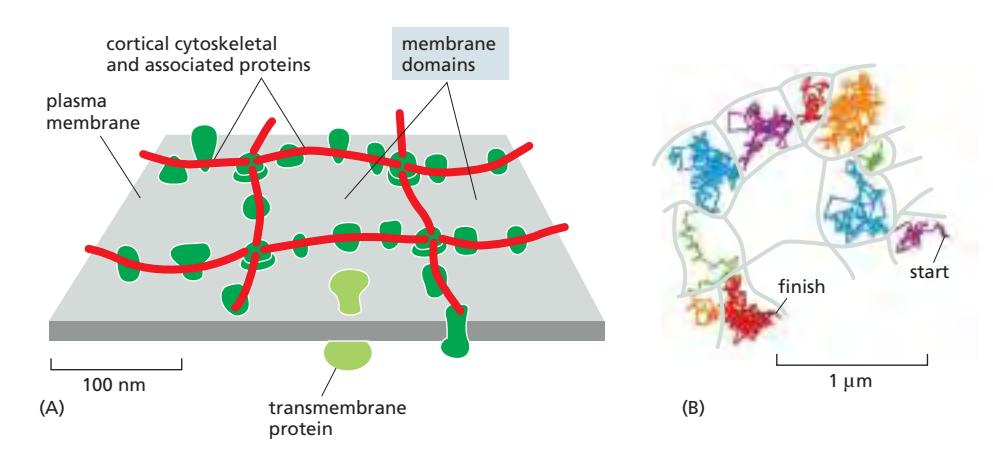 이 cortical cytoskeleton의 coralling으로 막단백질의 이동성이 제한받음. 그렇다 해도 아얘 불가능한 diffusion은 아니라 구역 안에서 움직이다가 뛰어넘고, 또 그 안에서 움직이기도 함.
이것이 hop diffusion.
이 cortical cytoskeleton의 coralling으로 막단백질의 이동성이 제한받음. 그렇다 해도 아얘 불가능한 diffusion은 아니라 구역 안에서 움직이다가 뛰어넘고, 또 그 안에서 움직이기도 함.
이것이 hop diffusion.
완전히 제한된 구역을 만드는 경우
epithelial cells
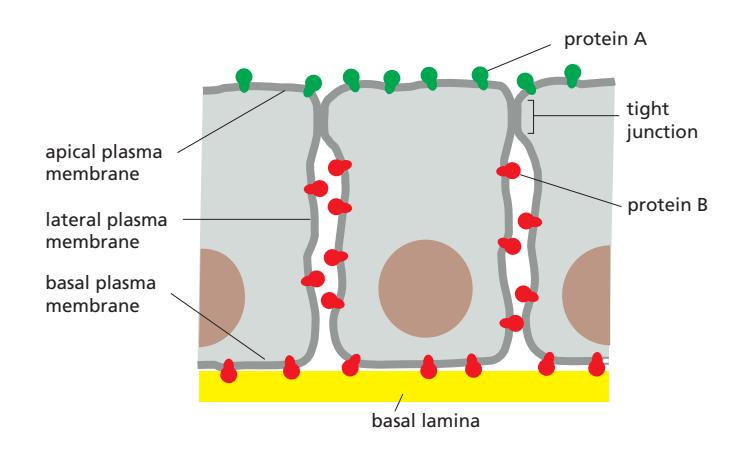 Epithelial cell (장이나 신장 tubule을 lining):
Epithelial cell (장이나 신장 tubule을 lining):
- 특정 plasma membrane enzyme과 transport protein이 apical surface에 국한됨
- 다른 것들은 basal과 lateral surface에 국한됨
- outer lipid monolayer도 예외가 아님. tight junction에 의한 domain 격리의 영향을 받음 Inner (cytosolic) monolayer의 lipid는 확산 가능
Spermatozoon의 Domain
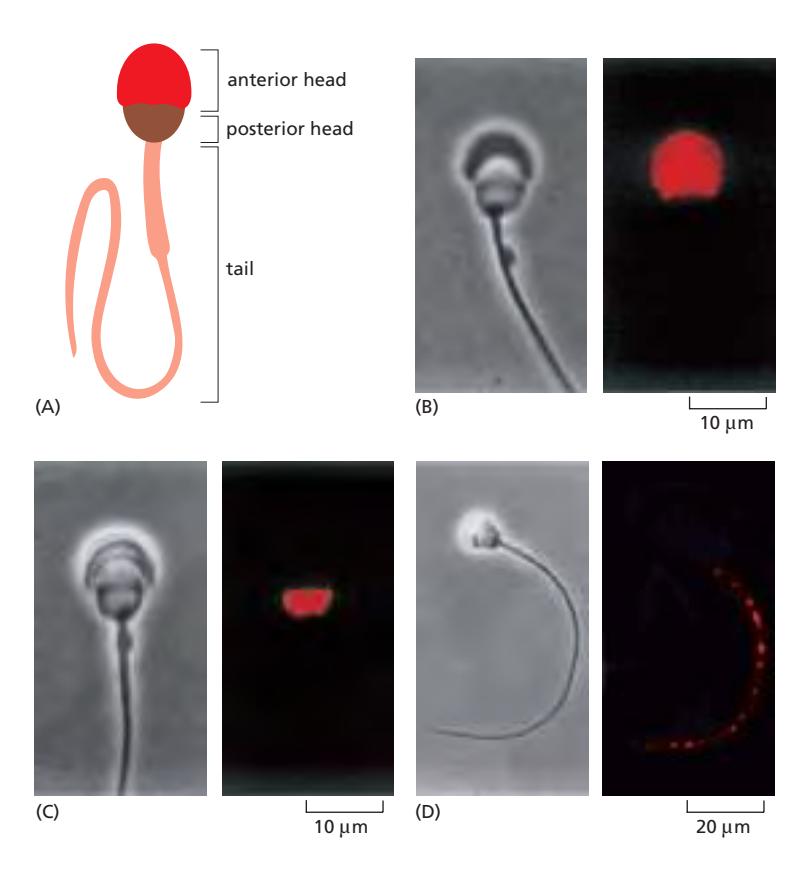
포유류 정자세포:
- 단일 세포가 여러 구조적, 기능적으로 구별되는 부분으로 구성됨
6. Hydropathy Plot
Hydropathy plot: Protein의 amino acid sequence로부터 membrane-spanning segment를 예측하는 방법
원리
- 고정 크기의 segment(보통 10-20 AA)를 polypeptide chain을 따라 이동시키며
- 각 segment를 nonpolar solvent → 물로 transfer하는 free energy 계산
- Positive값 = transfer에 free energy 필요 = 해당 segment가 hydrophobic (TM 영역 예측)
예시
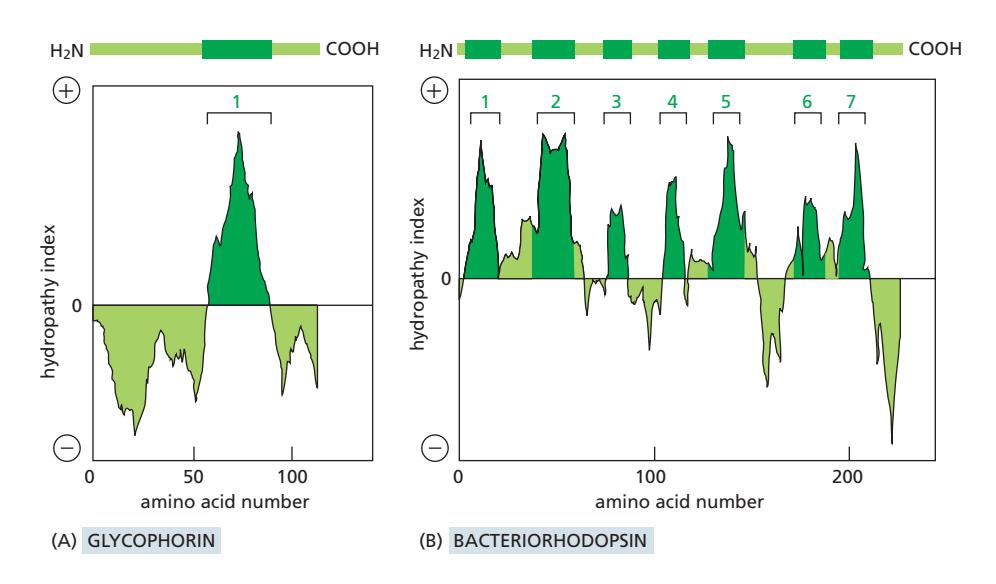
| 단백질 | TM helix 수 | Hydropathy plot 특징 |
|---|---|---|
| Glycophorin | 1개 | Peak 1개 |
| Bacteriorhodopsin | 7개 | Peak 7개 |
한계
| 상황 | 이유 | 결과 |
|---|---|---|
| β-barrel | 10개 이하 AA로 막 횡단 가능, 격번 AA만 소수성이면 됨 | Peak 식별 불가 |
| 여러 helix가 인접 (끼어있는 helix) | 모든 AA가 소수성일 필요 없음 | TM 개수 측정 불가 |
| Partial membrane insertion | Bilayer를 완전히 span하지 않는 region 존재 | 식별 불가 |
7. Detergents
Detergent는 hydrophobic association을 파괴하고 lipid bilayer를 disassemble하여 Membrane protein을 가용성 형태로 방출할 수 있는 유일한 agent이다. 이는 small amphiphilic molecule로 가변적인 구조를 가진다.
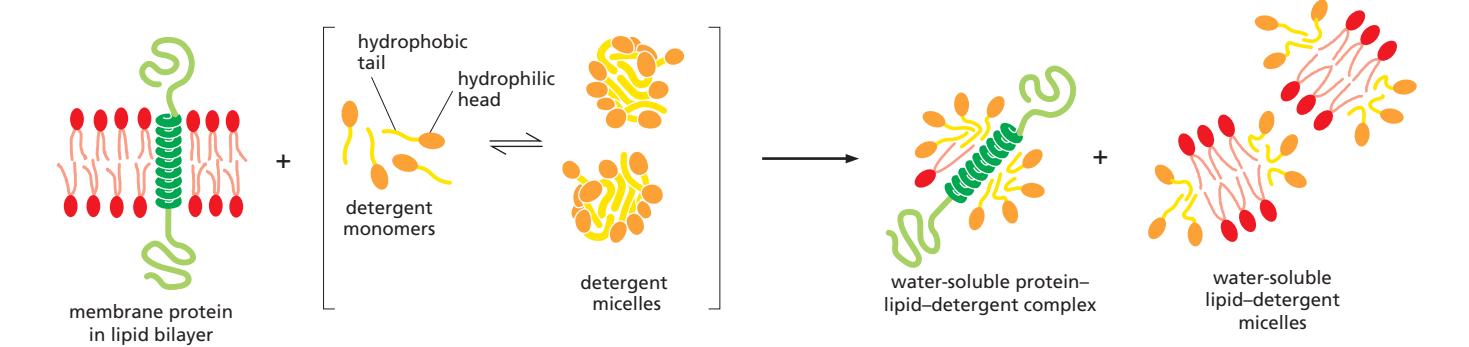 위는 detergent가 membrane protein과 lipid bilayer를 파괴하여 분리하는 메커니즘.
위는 detergent가 membrane protein과 lipid bilayer를 파괴하여 분리하는 메커니즘.
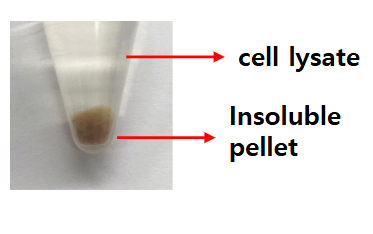 세포를 파괴하면, free soluble protein은 쉽게 추출 가능하나, membrane과 membrane protein은 녹지 않고 insoluble pellet으로 남는다.
세포를 파괴하면, free soluble protein은 쉽게 추출 가능하나, membrane과 membrane protein은 녹지 않고 insoluble pellet으로 남는다.
종류
SDS
- 가장 강함. 단백질을 선형 chain으로 풀어버림. 3차구조 없어짐.
- ionic. 강한 음전하
- protein의 존재만 알 수 있음(SDS-PAGE 기법). 성질은 잃음
triton x-100
- 약함. protein을 선형으로 파괴하지는 않지만 insoluble pellet에서 완전히 꺼내기 힘들어 검출할 수 없다.
β-octylglucoside
- 나머지 둘의 중간정도로, membrane protein을 soluble하게 만들고 구조도 잘 파괴하지 않아 membrane protein 연구에 좋다.
8. Membrane Bending Protein
0. 기본상태

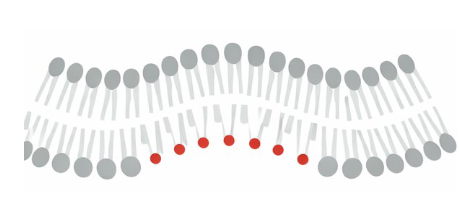
1. Hydrophobic Domain Insertion
 일부 protein이 hydrophobic protein domain 또는 attached lipid anchor를 bilayer의 한 leaflet에 삽입
일부 protein이 hydrophobic protein domain 또는 attached lipid anchor를 bilayer의 한 leaflet에 삽입
- cytosolic leaflet에서 주로 형성
2. Rigid Scaffold Formation
 일부 membrane-bending protein이 rigid scaffold 형성
일부 membrane-bending protein이 rigid scaffold 형성
- cytosolic leaflet에서 주로 형성
- F-Bar domain이 그 예.
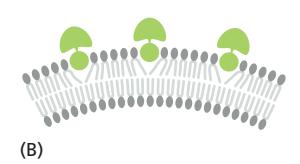
3. Lipid Clustering
위 그림 (D)는 protein이 큰 head group을 가진 lipid(sphingomyelin이 그 예시)에 결합하고 cluster하여 membrane을 bend하는 것을 보여준다.
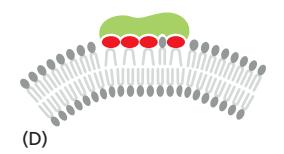
4. head group을 없애 음의 곡률 만들기
- phospholipase가 PIP2의 Lipid head group 제거=
- Negative curvature induce
관련 노트
- Phospholipid · Cholesterol · Glycolipid · Major lipids in cell membrane
- Amphiphilic molecule · Micelle · Lipid bilayer
- Fluidity of a lipid bilayer · Asymmetry of the lipid bilayer
- Membrane protein · Hydropathy plot · Lipid anchor
- α-helical Conformation in Membrane Proteins · β-Barrels Forming Large Channels
- Raft domain · Lipid droplet
- Cortical cytoskeleton · Restricting domain of membrane protein · Membrane bending protein